人教版初中化学学生分组实验报告Word下载.doc
《人教版初中化学学生分组实验报告Word下载.doc》由会员分享,可在线阅读,更多相关《人教版初中化学学生分组实验报告Word下载.doc(8页珍藏版)》请在冰点文库上搜索。
。
文字表达式:
5、收:
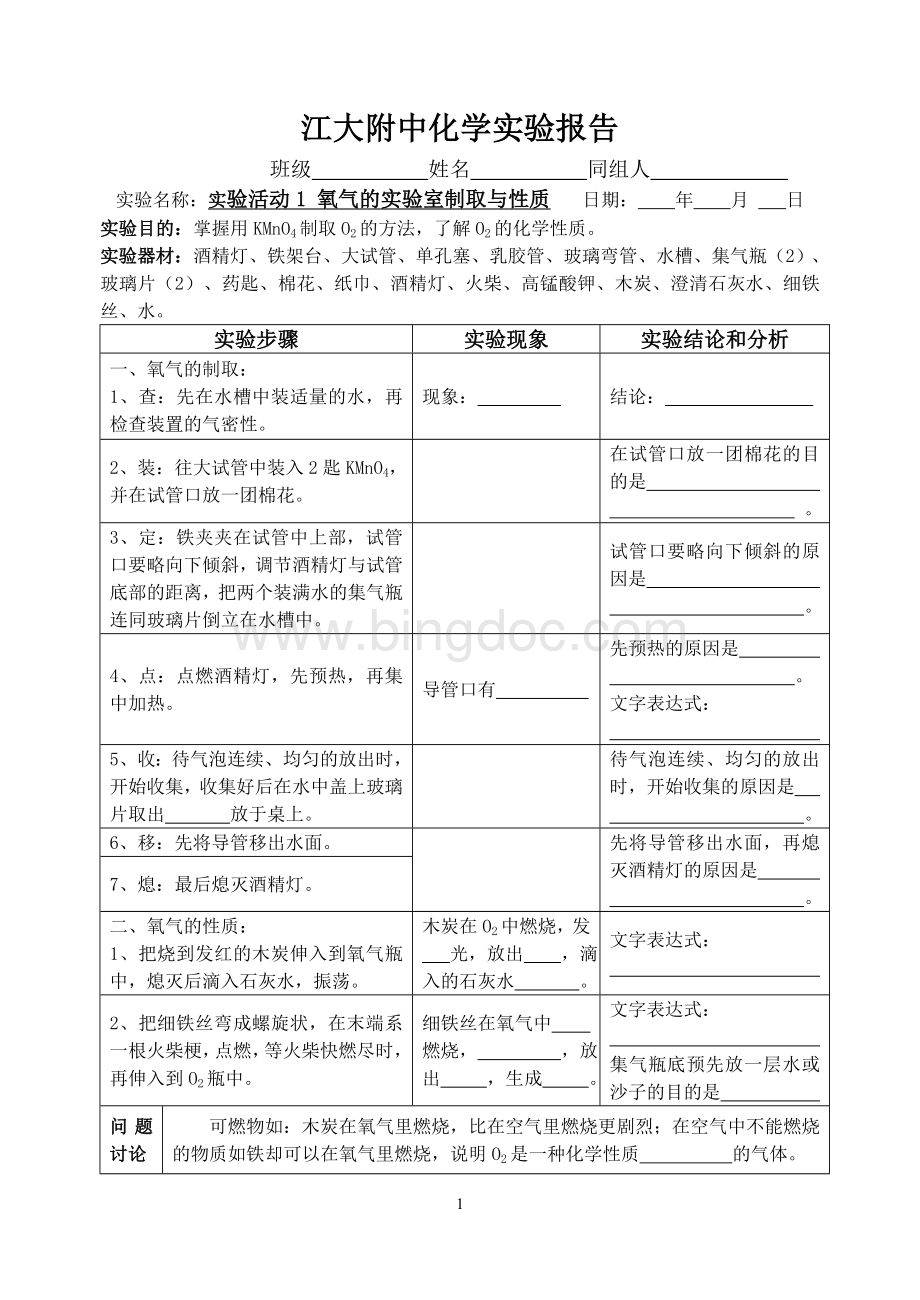
待气泡连续、均匀的放出时,开始收集,收集好后在水中盖上玻璃片取出放于桌上。
待气泡连续、均匀的放出时,开始收集的原因是
6、移:
先将导管移出水面。
先将导管移出水面,再熄灭酒精灯的原因是
7、熄:
最后熄灭酒精灯。
二、氧气的性质:
1、把烧到发红的木炭伸入到氧气瓶中,熄灭后滴入石灰水,振荡。
木炭在O2中燃烧,发
光,放出,滴入的石灰水。
2、把细铁丝弯成螺旋状,在末端系一根火柴梗,点燃,等火柴快燃尽时,再伸入到O2瓶中。
细铁丝在氧气中
燃烧,,放
出,生成。
集气瓶底预先放一层水或沙子的目的是
问题讨论
可燃物如:
木炭在氧气里燃烧,比在空气里燃烧更剧烈;
在空气中不能燃烧的物质如铁却可以在氧气里燃烧,说明O2是一种化学性质的气体。
实验活动2二氧化碳的实验室制取与性质日期:
年月日
练习在实验室里制取CO2,加深对二氧化碳性质的认识。
大试管、小试管、单孔塞、胶皮管、玻璃弯管、集气瓶、玻璃片、烧杯、量筒、试管夹、稀盐酸、石灰石(或大理石)、澄清石灰水、紫色石蕊溶液、蜡烛、木条、蒸馏水、火柴。
实验步骤:
实验内容和步骤
实验记录
1、制取二氧化碳
(1)连接装置:
取一试管,用一带有导管的橡皮塞塞紧。
(2)检查装置气密性。
(3)在试管里放入3小块大理石,然后小心倒入15mL的稀盐酸,立即用带有导管的橡皮塞塞住管口,观察试管里发生的现象以及反应中产生气体的颜色。
化学方程式:
(4)用向上排空气法收集气体,瓶口盖上玻片。
用向上排空气法收集CO2的原因是
(5)用燃着的木条检查集气瓶中是否已集满二氧化碳。
(备用)
2、二氧化碳的性质
(1)在一支试管中装入石灰水,通入二氧化碳,观察现象。
(2)向二支试管中分别加入2mL蒸馏水,然后各滴入1-2滴石蕊溶液,向其中一支试管中通入二氧化碳,对比观察现象。
将通入二氧化碳的试管用酒精灯加热,观察现象。
(3)把一支蜡烛放入烧杯中,点燃,向烧杯内慢慢倾倒一瓶二氧化碳,观察现象。
1、实验室制取气体应先考虑哪些因素:
(1)选择适当的反应。
(2)发生装置:
考虑反应物的和反应的。
(3)收集装置:
气体的和。
2、怎样用实验证明汽水中含有二氧化碳?
。
实验活动3燃烧的条件日期:
1、加深对燃烧条件的认识,进一步了解灭火的原理。
2、体验实验探究的过程。
酒精灯、烧杯(250ml)、镊子、三角架、坩埚钳、薄铜片、酒精、棉花、滤纸碎片、乒乓球碎片、蜡烛、火柴。
1、两团棉花,一团蘸酒精,另一团蘸水(把棉花浸没透了),用坩埚钳夹住,同时把它们放在酒精灯上加热片段。
燃烧的条件之一:
2、
(1)分别用坩埚钳夹住一小块滤纸碎片和乒乓球碎片,放在酒精灯上加热,观察现象。
(2)将一小块滤纸碎片和乒乓球碎片分开放在一块薄铜片的两侧,加热铜片的中部,观察现象。
3、利用蜡烛和烧杯,设计一个简单的实验,说明燃烧的条件之一:
需要有氧气(或空气)。
你的设计方案:
1、上述实验步骤1中,如果在酒精灯上加热时间较长,会发生什么现象?
你能解释原因吗?
2、如果将实验步骤2
(2)中的滤纸碎片和乒乓球碎片换成木屑和煤粉进行实验,会有什么现象发生?
说明了什么?
实验活动4金属的物理性质和某些化学性质日期:
1、巩固和加深对金属性质的认识。
2、培养实验设计能力。
仪器:
试管(7)、试管夹、坩埚钳、镊子、小木条、酒精灯、火柴、电池、导线、小灯泡。
药品:
镁条、锌粒、铝片、铁片、铁粉、铜片、黄铜片(或白铜片)、稀盐酸、稀硫酸、硫酸铜溶液、硝酸银溶液。
实验结论
1、金属的物理性质
(1)观察并描述镁、铝、铁、铜的颜色和光泽。
镁、铝、铁:
铜:
(2)采用相互刻画的方法,比较铜片和铝片、铜片和黄铜片的硬度。
表面有刻痕
硬度:
铜片铝片
铜片黄铜片
(3)请你设计并进行实验,证明金属具有导电性(或导热性、延展性)
金属具有性
2、金属的化学性质
(1)用坩埚钳夹取一块铜片,放在酒精灯火焰上加热,观察铜片表面的变化。
铜片表面变成色。
(2)金属与酸反应
①分别在5支试管中装入5ml稀盐酸(或稀硫酸)。
②分别投入少量的Mg、Al、Zn、Fe、Cu。
③用燃着的木条放于试管口。
Mg:
Al:
Zn:
Fe:
Cu:
排在前面的金属能与酸反应,生成。
(3)请你设计并进行实验,比较铁、铜、银的金属活动性强弱。
三种金属的活动性顺序为:
FeCuAg
问题
讨论
铁是银白色金属。
上述实验中,你观察到的铁片和铁粉是什么颜色的?
你有什么问题?
查阅资料,与同学交流。
江南大学附属实验中学化学实验报告
实验活动5一定溶质质量分数的氯化钠溶液的配制
日期:
年月日
1、练习配制一定溶质质量分数的溶液。
2、加深对溶质的质量分数概念的理解。
实验用品:
托盘天平、药匙、烧杯(100ml)、量筒(50ml)、玻璃棒、胶头滴管。
氯化钠、蒸馏水。
1、配制质量分数为6%的氯化钠溶液
⑴计算:
配制50g质量分数为6%的NaCl溶液所需氯化钠和水的质量。
NaCl________g,水________g。
⑵称量:
用托盘天平称取所需的NaCl,倒入烧杯中。
⑶量取:
把水的密度近似看作1g/cm3。
用量筒量所取需的水,倒入盛有NaCl的烧杯中。
水________mL
⑷溶解:
用玻璃棒搅拌,使氯化钠溶解。
玻璃棒的作用
2、配制质量分数为3%的氯化钠溶液
配制50g质量分数为3%的NaCl溶液所需质量分数为6%的氯化钠溶液(密度约为1.04g/cm3)和水的质量。
6%的氯化钠溶液________g(体积为
mL)和水________g。
⑵量取:
用量筒量所取需的水和氯化钠溶液,倒入烧杯中。
⑶混匀:
用玻璃棒搅拌,使溶液混合均匀。
3、把配好的上述两种氯化钠溶液分别装入试剂瓶中,盖好瓶塞并贴上标签(标签中应包括药品名称和溶液中溶质的质量分数),放入试剂柜中。
问题与交流
1、用托盘天平称量氯化钠时,有哪些注意事项?
2、用量筒量取液体,读数时应注意什么?
3、准确配制一定溶质质量分数的溶液,在实际应用中有什么重要意义?
请举例说明。
实验活动6酸、碱的化学性质日期:
年月日
1、加深对酸和碱的主要性质的认识。
2、通过实验解释生活中的一些现象。
点滴板、滴管、试管、药匙、镊子、蒸发皿、铁架台(带铁圈)、玻璃棒、酒精灯、火柴。
稀HCl、稀H2SO4、NaOH溶液、Ca(OH)2溶液、硫酸铜溶液、氢氧化钙粉末、石蕊溶液、酚酞溶液、锈铁钉。
1、在点滴板上分别滴2滴稀HCl、稀H2SO4、NaOH溶液和Ca(OH)2溶液,在其中滴入石蕊、酚酞试液。
酸溶液
碱溶液
HCl
H2SO4
NaOH
Ca(OH)2
石蕊
酚酞
酸溶液能使石蕊,酚酞;
碱溶液能使石蕊,酚酞。
2、取2根锈铁钉放入两个试管中,然后加入约2mL稀盐酸,观察现象。
等锈除尽后,将其中一个试管中铁钉取出,洗净。
继续观察另一支试管中的现象,过一段时间将铁钉取出,洗净。
比较两支铁钉。
,方程式:
。
酸能与反应,酸能与反应。
3、在试管中加入约2mL硫酸铜溶液,然后滴加几滴氢氧化钠溶液,观察现象。
然后再向试管中加入稀盐酸,观察现象。
碱能与反应,碱能与反应。
4、在试管中加入约1mL氢氧化钠溶液,滴入几滴酚酞溶液。
然后边用滴管慢慢加入稀盐酸,边不断振动试管,至溶液颜色恰好变成无色为止。
取该无色溶液约1mL,置于蒸发皿中加热,使液体蒸干,观察现象。
,分析:
。
酸能与反应,生成和。
5、向两支试管中各加入相同的氢氧化钙粉末(用药匙的柄把一端挑一点),然后各加入1mL水,振荡;
再各滴入1-2滴酚酞溶液,观察现象。
继续向其中一支试管加入约1mL水,振荡;
向另一支试管加入约1mL稀盐酸,振荡;
比较两支试管中的现象。
,分析:
问题与交流:
通过实验步骤5,可以验证氢氧化钙的哪些性质?
物理性质:
化学性质:
实验活动7溶液酸碱性的检验日期:
1、初步学会用酸碱指示剂检验溶液的酸碱性。
2、初步学会用pH试纸测定溶液的酸碱度。
玻璃片、玻璃棒、胶头滴管、镊子、点滴板、研钵、纱布、烧杯。
蒸馏水、酒精溶液、酚酞溶液、石蕊溶液、pH试纸、植物的花瓣或果实、土壤样品。
你还需要的实验室用品:
你还需要的生活用品:
1、自制酸碱指示剂:
自己选择植物的花瓣或果实,在研钵中捣烂,加入5ml酒精溶液浸泡;
用纱布将浸出的汁液过滤或挤出。
2、选择实验室或生活中的几种溶液,进行下列实验:
⑴分别用酚酞溶液和石蕊溶液检验溶液的酸碱性;
⑵用pH试纸测定溶液的酸碱度;
⑶试验自制的指示剂在溶液中颜色的变化。
实验现象:
选择的
溶液
加入石蕊溶液后的颜色变化
加入酚酞溶液后的颜色变化
溶液的
酸碱性
pH
加入自制指示剂后的颜色变化
3、在校园或农田里取少量土壤样品。
将土壤样品与蒸馏水按1:
5的质量比在烧杯中混合,充分搅拌后静置。
用pH试纸测澄清液体的酸碱度。
pH=。
土壤样品显性。
1、你自制的指示剂检验溶液酸碱性的效果如何?
了解其他同学自制的指示剂的检验效果,哪种植物的花瓣或果实制成的指示剂检验效果好?
2、归纳自制的指示剂在酸、碱溶液中的颜色变化情况,与同学交流。
实验活动8粗盐中难溶性杂质的去除日期:
年月日实验目的:
1、体验固体混合物初步提纯的实验过程。
2、学习蒸发操作技能,巩固溶解、过滤操作技能。
托盘天平、药匙、铁架台(带铁圈)、烧杯、玻璃棒、漏斗、滤纸、
量筒(10mL)、酒精灯、坩埚钳、石棉网、蒸发皿、火柴、纸巾。
水、粗盐。
实验结论或分析
1、溶解:
用天平称取粗盐5g,用药匙将该粗盐逐渐加入盛有10mL水的烧杯中,边加边用玻璃棒搅拌,一直加到粗盐不再溶解为止,称出剩余粗盐的质量。
称取粗盐质量为
剩余粗盐质量为
玻璃棒的作用
溶解粗盐质量为
2、过滤:
过滤食盐水1~2次,直到滤液澄清。
滤纸上有。
3、蒸发:
将滤液倒入蒸发皿中,加热,结晶。
蒸发皿中有。
玻璃棒的作用
待时停止加热,用余热蒸干。
4、计算产率:
用玻璃棒将蒸发皿中的食盐转移到称量纸上,称重,计算产率。
精盐质量为
精盐产率=
1、制取粗盐时,晒盐和煮盐的目的都是通过蒸发盐溶液中的水分使之浓缩。
想一想:
能否采用降低溶液温度的方法来达到同一目的?
2、本实验中采用的方法利用了氯化钠的哪些性质?
考虑到粗盐的来源,你判断这样提纯的盐是否为纯净物,并设计实验验证你的判断。
8