北京义教版九年级上学期期末化学试题练习.docx
《北京义教版九年级上学期期末化学试题练习.docx》由会员分享,可在线阅读,更多相关《北京义教版九年级上学期期末化学试题练习.docx(12页珍藏版)》请在冰点文库上搜索。
北京义教版九年级上学期期末化学试题练习
北京义教版九年级上学期期末化学试题
姓名:
________班级:
________成绩:
________
一、单选题
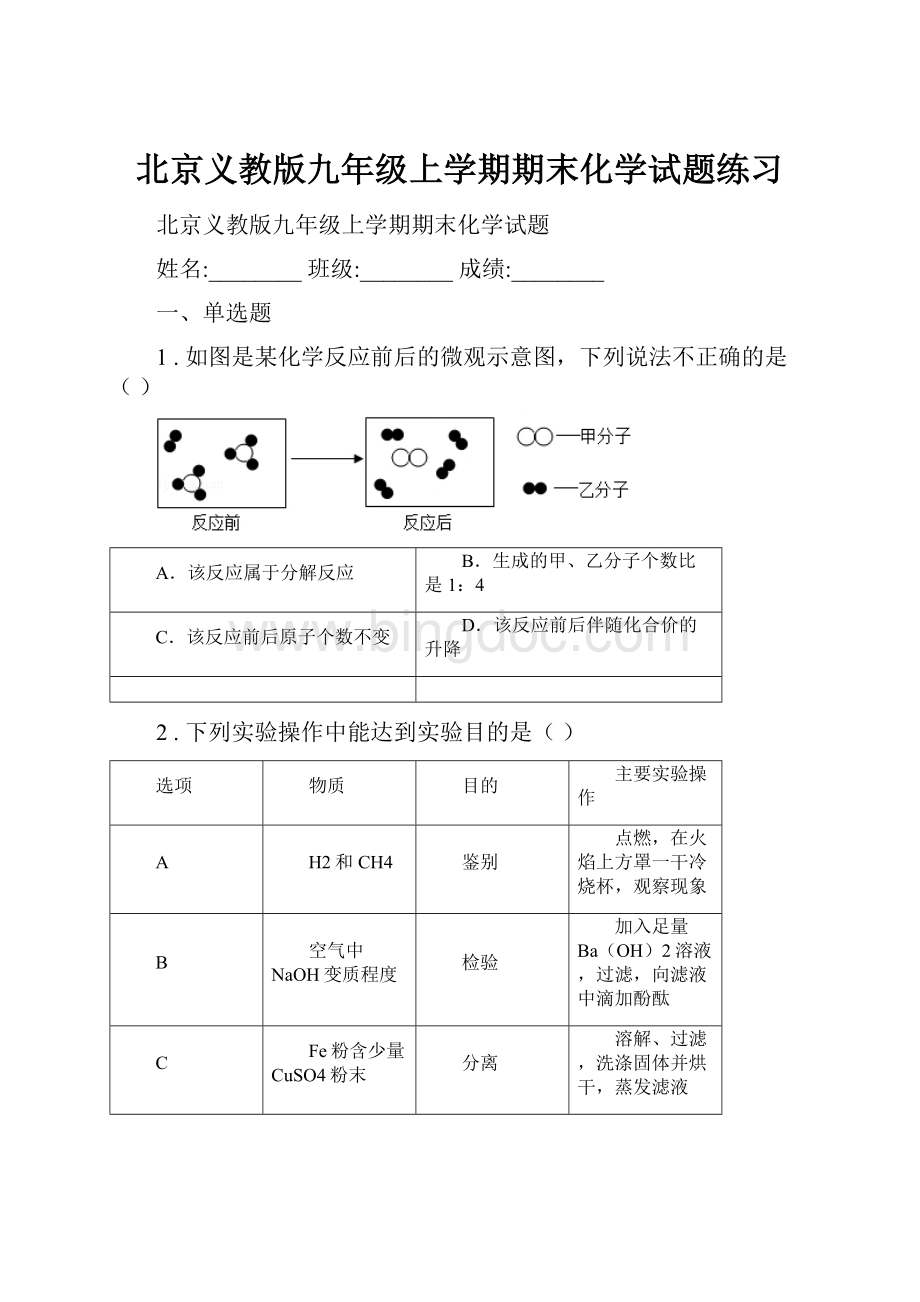
1.如图是某化学反应前后的微观示意图,下列说法不正确的是()
A.该反应属于分解反应
B.生成的甲、乙分子个数比是1:
4
C.该反应前后原子个数不变
D.该反应前后伴随化合价的升降
2.下列实验操作中能达到实验目的是()
选项
物质
目的
主要实验操作
A
H2和CH4
鉴别
点燃,在火焰上方罩一干冷烧杯,观察现象
B
空气中NaOH变质程度
检验
加入足量Ba(OH)2溶液,过滤,向滤液中滴加酚酞
C
Fe粉含少量CuSO4粉末
分离
溶解、过滤,洗涤固体并烘干,蒸发滤液
D
BaCl2溶液混有Ba(NO3)2杂质
除杂
先加入过量Na2CO3溶液,过滤、洗涤;再向所得固体中加入适量稀盐酸
A.A
B.B
C.C
D.D
3.有关反应2Mg+O2
2MgO的说法正确的是
A.镁加氧气在点燃条件下生成氧化镁
B.每3克镁和2克氧气在点燃条件下生成5克氧化镁
C.每2克镁和3克氧气在点燃条件下生成5克氧化镁
D.每2份镁和1份氧气在点燃条件下生成2份氧化镁
4.下列变化中,前者是化学变化,后者是物理变化的是()
A.矿石粉碎 食物腐烂
B.牛奶变酸 高粱酿酒
C.火药爆炸 海水晒盐
D.冰雪融化 酒精挥发
5.下表中列出了除去物质中所含少量杂质的方法,其中正确的是
选项
物质
杂质
除去杂质的方法
A
CO2
H2O
NaOH固体干燥
B
CuO粉末
Cu粉
加入足量的稀硫酸,过滤
C
KCl粉末
MnO2
加水溶解,过滤,洗涤,烘干
D
CaCl2溶液
HCl
加入过量的CaCO3,过滤
A.A
B.B
C.C
D.D
6.下列实验方案错误的是()
A.通过用磁铁吸引区别粉末状的铁和四氧化三铁
B.按溶解、过滤、蒸发的操作顺序分离NaCl和泥沙
C.通过观察在空气中的变化区别氢氧化钠和氢氧化钙固体
D.用高锰酸钾溶液检测二氧化碳中是否含有二氧化硫气体
7.下列离子组合能在pH=1的溶液中大量共存的是
A.K+、Ag+、NO3-、Cl-
B.K+、Na+、CO32-、Cl-
C.Ba2+、Na+、OH-、SO42-
D.K+、Na+、SO42-、Cl-
8.下列有关材料的说法正确的是
A.玻璃——无机非金属材料
B.有机玻璃——复合材料
C.玻璃钢——无机材料
D.棉花——合成纤维
9.向盛有一定量锌粒的烧杯中逐滴加入稀硫酸至过量。
在该过程中,下列图像不能正确反映烧杯内物质的某些物理量变化趋势的是
A.
B.
C.
D.
10.物质性质决定用途,下列说法不正确的是
A.甲醛能使蛋白质变性,可用于海鲜等水产品的防腐
B.不锈钢具有较强的耐腐蚀性,可用于制作医疗器械
C.Ca(OH)2具有碱性,可用于改良酸性土壤
D.食醋具有酸性,可除去玻璃水壶中的水垢
11.甲、乙物质的溶解度曲线如图,下列叙述正确的是()
A.甲、乙两种物质都属于微溶性物质
B.t1℃时,甲、乙溶液恒温蒸发等质量的水时,甲、乙析出固体质量相等
C.甲中含有少量乙时,可用蒸发结晶的方法得到乙
D.t2℃时,分别取100g甲、乙物质的饱和溶液,将其降温至t1℃时,所得溶液质量甲小于乙
12.下列食物中主要为人体提供糖类的是()
A.蔬菜
B.大米
C.牛奶
D.花生
13.如下图所示的有关二氧化碳性质的实验中,只能证明二氧化碳的物理性质的是
A.A
B.B
C.C
D.D
14.下列说法正确的是 ()
A.纯碱不是碱
B.食盐不是盐
C.烧碱不是碱
D.盐酸不是酸
15.下列图像不能正确反映其对应操作中各量变化关系的是
A.
高温煅烧一定质量的石灰石
B.
在密闭容器内加热一定质量的铜粉
C.
将一定质量的KNO3饱和溶液恒温蒸发水分
D.
向一定质量部分变质的NaOH溶液中滴加稀盐酸
二、实验题
16.如图是某化学学习小组设计的用一氧化碳还原氧化铜的实验装置。
请回答以下问题:
(1)实验过程中,图中A处能观察到的实验现象是______________发生反应的化学方程式为_____________该化学反应________(填“是”或“不是”)置换反应。
(2)该装置存在的一个主要问题是____________;你的改进方法是_____________。
三、流程题
17.某兴趣小组的同学从实验室收集到一桶含有FeSO4、CuSO4的废液,他们想从中回收金属铜和硫酸亚铁晶体,设计了如下操作方案,结合方案回答下列问题:
(1)固体A中含有______
(2)步骤①中反应的化学方程式为_________________
(3)操作a的名称为______
(4)理论上所得硫酸亚铁晶体的质量______(填“>”“<”或“=”)原废液中硫酸亚铁的质量。
四、科学探究题
18.小敏研究影响锌与盐酸反应快慢的因素。
序号
盐酸溶液浓度
2分钟内产生氢气的体积
1
5%
10mL
2
15%
28mL
(1)写出该反应的化学方程式。
(2)图中A、B仪器可以组装一套测量气体体积的装置,利用该装置时A中的_____(a或b)管接c。
(3)他选用2克完全相同的锌片分别和同体积5%、15%的稀盐酸进行实验。
获得表格数据。
由此推断实验是通过_________来体现反应快慢的。
(4)小敏分析数据得到如下结论:
锌与盐酸反应快慢与盐酸浓度有关,盐酸浓度越大反应越快。
其他同学认为结论不可靠,他们的依据是:
______________。
(5)实验中小敏发现锌与盐酸反应时,一开始产生氢气速度并没有随盐酸浓度的减少而减慢,查阅资料得知化学反应中往往伴随着能量变化。
由此作出猜想:
锌与盐酸反应快慢还与_______有关。
五、计算题
19.我国民间有端午挂艾草的习俗。
艾草含有丰富的黄酮素(化学式为C15H10O2),有很高的药用价值。
请回答:
(1)黄酮素含有_____种元素,碳、氢的原子个数比是_____(最简整数比)。
(2)黄酮素的相对分子质量是_____。
(3)黄酮素中碳、氢、氧元素的质量比为_____。
(4)黄酮素分子中碳元素的质量分数是为_____(计算结果精确到0.1%)。
六、综合题
20.
(1)按要求从盐酸、氢氧化钠、氧化钙、氢氧化钙、硫酸、氮气、碳酸钠中选择合适的物质,将其化学式填写在横线上。
①一种空气中大量存在的气体________
②一种能用于食品干燥的氧化物________
③一种人体内消化食物的酸_______
④一种能改良酸性土壤的碱________
(2)今年4月16日,美国宣布制裁我国最大的国有控股通信设备公司一中兴通讯公司,制裁内容包括未来7年内禁止美国公司向中兴通讯销售手机芯片在内的各种部件、软件和技术。
美国此举意在遏制中国产业技术的转型,阻碍中国的崛起。
事件虽令人愤慨,但也折射出我国半导体芯片技术的落后,习主席曾强调“核心技术靠化缘是要不来的,我们仍要继续自力更生”。
硅(Si)是一种半导体,高纯度单质硅是制造高性能芯片的重要材料。
在工业上,可在1200℃的高温条件下用氢气还原三氯氢硅(SiHCl3)得到单质硅和氯化氢气体。
①在三氯氢硅中,所占质量分数最大的元素是_______(填元素符号);
②写出氢气在髙温条件下还原三氯氢硅的化学方程式_________________________;
③在三氯氢硅中,氯元素为-1价,则上述反应前、后,硅元素的化合价分别为__________;
④关于工业上用氢气还原三氯氢硅的反应过程,下列说法不正确的是________(填序号)。
A该化学反应属于复分解反应 B反应过程中若引入氧气,易引发氢气燃烧爆炸
C生成的氯化氢气体可用氢氧化钠溶液吸收D反应后得到的炽热的单质硅需隔绝氧气
21.普通干电池在生活中的用途很广。
(1)普通干电池照明时化学能转化为____。
(2)目前,废旧电池对环境的污染已越来越引起人们的重视。
为了实现可持续发展的战略目标,许多有识之士正在研究废旧电池的有效回收再利用技术。
如图为普通电池(锌锰电池)示意图,请你根据图示分析:
将回收的废旧电池进行分离,可以得到的金属单质有(用化学式表示,下同)____,氧化物有___,盐有____,有机物有__(写名称)。
(3)小明同学想得到⑤中纯净干燥的二氧化锰和氯化铵溶液,并检验氯化铵中的铵根离子。
设计了如下实验步骤,请你帮他完成。
实验步骤
实验现象
结论或解释
①剥开干电池,取出碳棒周围的黑色粉末
②溶解、___(填操作名称)、洗涤
得到黑色粉末和无色澄清液体
黑色粉末的成分为__。
③对黑色粉末进行__
得到纯净的MnO2固体
④检验第②步中得到的无色澄清液体中是否含铵根离子的方法是:
_____
_____
化学方程式为:
______
(4)对分离回收的铜帽净化处理,放入硝酸银溶液中,一段时间以后,可观察到的现象是__,反应的化学方程式是_____,其基本反应类型为___反应。
22.正常情况下人的胃液pH为0.8—1.5,相应含氯化氢的质量分数为0.2%—0.4%,胃液中氯化氢过多过少都不利于健康。
某人出现反胃、吐酸水的症状,经检查其胃液中氯化氢的质量分数为1.495%(胃液密度约为1g/cm3)。
(1)正常情况下,人的胃液显_________性。
(2)若人的胃液总量为100mL,正常胃液中HCl的质量范围为___________________g。
(3)服用碱性物质可以治疗胃液中HCl含量过多,你认为该患者 ___________ (填能或不能)服用熟石灰来治疗胃酸过多,理由是______________________________________。
(4)医生给患者开的药是胃舒平[有效成分是Al(OH)3],每片胃舒平含Al(OH)3的质量为0.39g。
请根据化学方程式计算该患者至少服用________片胃舒平,胃液才能恢复正常?
(请写出计算过程)
参考答案
一、单选题
1、
2、
3、
4、
5、
6、
7、
8、
9、
10、
11、
12、
13、
14、
15、
二、实验题
1、
三、流程题
1、
四、科学探究题
1、
五、计算题
1、
六、综合题
1、
2、
3、