微生物限度检查记录(内包材).doc
《微生物限度检查记录(内包材).doc》由会员分享,可在线阅读,更多相关《微生物限度检查记录(内包材).doc(2页珍藏版)》请在冰点文库上搜索。
微生物限度检查记录文件编码:
RD/QC-082-04
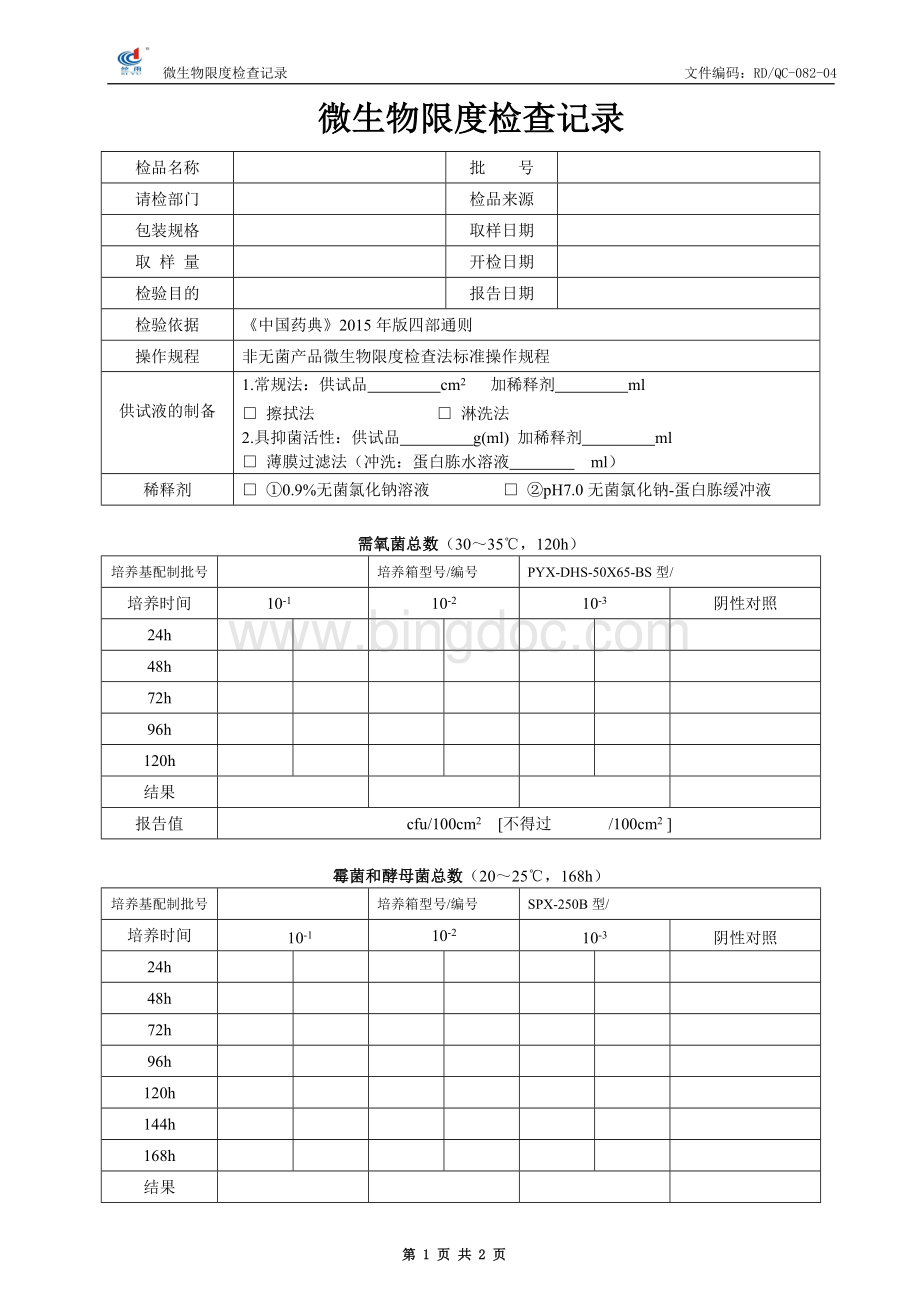
微生物限度检查记录
检品名称
批号
请检部门
检品来源
包装规格
取样日期
取样量
开检日期
检验目的
报告日期
检验依据
《中国药典》2015年版四部通则
操作规程
非无菌产品微生物限度检查法标准操作规程
供试液的制备
1.常规法:
供试品cm2加稀释剂ml
□擦拭法□淋洗法
2.具抑菌活性:
供试品g(ml)加稀释剂ml
□薄膜过滤法(冲洗:
蛋白胨水溶液ml)
稀释剂
□①0.9%无菌氯化钠溶液□②pH7.0无菌氯化钠-蛋白胨缓冲液
需氧菌总数(30~35℃,120h)
培养基配制批号
培养箱型号/编号
PYX-DHS-50X65-BS型/
培养时间
10-1
10-2
10-3
阴性对照
24h
48h
72h
96h
120h
结果
报告值
cfu/100cm2[不得过/100cm2]
霉菌和酵母菌总数(20~25℃,168h)
培养基配制批号
培养箱型号/编号
SPX-250B型/
培养时间
10-1
10-2
10-3
阴性对照
24h
48h
72h
96h
120h
144h
168h
结果
报告值
cfu/100cm2[不得过/100cm2]
控制菌检查记录
大肠埃希菌
试验名称
培养基配制批号
阳性对照
供试品
阴性对照
胰酪大豆胨液体
麦康凯液体
麦康凯琼脂平板
分离、纯化、鉴定试验
结果判定:
□检出□未检出(规定:
不得检出/10cm2)
结果判定:
本品按《中国药典》2015年版四部通则检验,结论为:
□合格□不合格
检验人:
复核人:
第2页共2页