药品不良反应报告表填写示例及填写说明.doc
《药品不良反应报告表填写示例及填写说明.doc》由会员分享,可在线阅读,更多相关《药品不良反应报告表填写示例及填写说明.doc(4页珍藏版)》请在冰点文库上搜索。
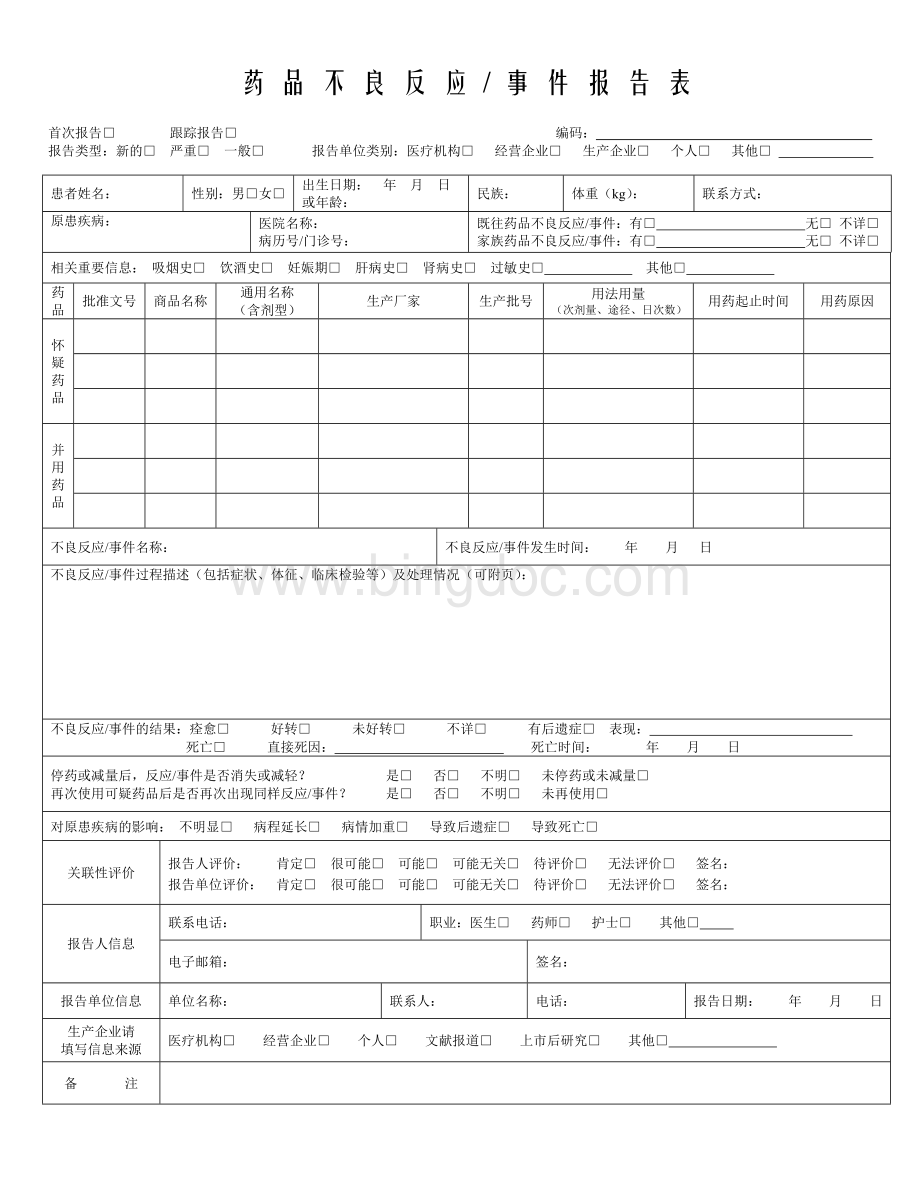
药品不良反应/事件报告表
首次报告□跟踪报告□编码:
报告类型:
新的□严重□一般□报告单位类别:
医疗机构□经营企业□生产企业□个人□其他□
患者姓名:
性别:
男□女□
出生日期:
年 月 日
或年龄:
民族:
体重(kg):
联系方式:
原患疾病:
医院名称:
病历号/门诊号:
既往药品不良反应/事件:
有□无□不详□
家族药品不良反应/事件:
有□无□不详□
相关重要信息:
吸烟史□饮酒史□妊娠期□肝病史□肾病史□过敏史□其他□
药品
批准文号
商品名称
通用名称
(含剂型)
生产厂家
生产批号
用法用量
(次剂量、途径、日次数)
用药起止时间
用药原因
怀疑药品
并用药
品
不良反应/事件名称:
不良反应/事件发生时间:
年 月 日
不良反应/事件过程描述(包括症状、体征、临床检验等)及处理情况(可附页):
不良反应/事件的结果:
痊愈□好转□未好转□不详□有后遗症□表现:
死亡□直接死因:
死亡时间:
年月日
停药或减量后,反应/事件是否消失或减轻?
是□否□不明□未停药或未减量□
再次使用可疑药品后是否再次出现同样反应/事件?
是□否□不明□未再使用□
对原患疾病的影响:
不明显□病程延长□病情加重□导致后遗症□导致死亡□
关联性评价
报告人评价:
肯定□ 很可能□ 可能□ 可能无关□ 待评价□ 无法评价□ 签名:
报告单位评价:
肯定□ 很可能□ 可能□ 可能无关□ 待评价□ 无法评价□ 签名:
报告人信息
联系电话:
职业:
医生□ 药师□ 护士□其他□
电子邮箱:
签名:
报告单位信息
单位名称:
联系人:
电话:
报告日期:
年 月 日
生产企业请
填写信息来源
医疗机构□经营企业□个人□文献报道□上市后研究□其他□
备注
药品不良反应/事件报告表示例
首次报告□跟踪报告□编码:
报告类型:
新的□严重□一般□报告单位类别:
医疗机构□经营企业□生产企业□个人□其他□
患者姓名:
×××
性别:
男□女□
出生日期:
年 月 日
或年龄:
××
民族:
××
体重(kg):
××
联系方式:
××××××
原患疾病:
指患者此次入院或就诊的主要疾病(如果有多种慢性疾病可以补充在相关重要信息或
是备注里面),不能写字母缩写。
医院名称:
三亚市中医院
病历号/门诊号:
××××(务必填写)
既往药品不良反应/事件:
有□需提供药品通用名称及具体反应无□不详□
家族药品不良反应/事件:
有□需提供药品通用名称及具体反应无□不详□
相关重要信息:
吸烟史□饮酒史□妊娠期□肝病史□肾病史□过敏史□此处是提供有否食物等过敏史其他□
药品
批准文号
商品名称
通用名称
(含剂型)
生产厂家
生产批号
用法用量
(次剂量、途径、日次数)
用药起止时间
用药原因
怀疑药品
国药准字
此处填写药品的通用名称。
注射剂包含注射液和粉针剂,请认真选择正确剂型
本次使用药物的生产批号
包括每次用药剂量、给药途径、每日给药次数,例如,5mg,口服,每日2次。
指使用药品的同一剂量的开始时间和停止时间
填写使用该药品的原因,应详细填写。
例如:
患者高血压病史,此次因肺部感染而注射氨苄青霉素引起不良反应,用药原因栏应填写肺部感染
并用药
品
同上
不良反应/事件名称:
应填写不良反应中最主要、最明显的症状。
不良反应/事件发生时间:
×年 ×月×日(应填写发生不良反应/事件的确切时间)
不良反应/事件过程描述(包括症状、体征、临床检验等)及处理情况(可附页):
一般格式为:
患者因×××疾病于×××月×××日(必要时应详细到×××时分)以×××途径给予×××药品,×××剂量,用药×××时间出现×××反应(反应描述须明确、具体),×××时间后给予是否停药及×××处理(包括以×××途径给予×××药品及×××剂量,和其他处理措施),处理后×××时间患者转归情况。
不良反应/事件的结果:
痊愈□好转□未好转□不详□有后遗症□表现:
死亡□直接死因:
死亡时间:
×年×月×日
停药或减量后,反应/事件是否消失或减轻?
是□否□不明□未停药或未减量□
再次使用可疑药品后是否再次出现同样反应/事件?
是□否□不明□未再使用□
对原患疾病的影响:
不明显□病程延长□病情加重□导致后遗症□导致死亡□
关联性评价
报告人评价:
肯定□ 很可能□ 可能□ 可能无关□ 待评价□ 无法评价□ 签名:
×××
报告单位评价:
肯定□ 很可能□ 可能□ 可能无关□ 待评价□ 无法评价□ 签名:
×××
报告人信息
联系电话:
务必正确填写
职业:
医生□ 药师□ 护士□其他□
电子邮箱:
签名:
×××
报告单位信息
单位名称:
×××
联系人:
×××
电话:
×××
报告日期:
年 月 日
生产企业请
填写信息来源
医疗机构□经营企业□个人□文献报道□上市后研究□其他□
《药品不良反应/事件报告表》填写说明
1.《药品不良反应/事件报告表》应填写真实事件,报表所列患者信息及怀疑药品信息项目必须真实、完整、准确。
2.《药品不良反应/事件报告表》填写字迹要清晰,其中选择项画“√”,叙述项应准确、简明,不得有缺漏项。
3.新的□ 严重□ 一般□
(1)新的药品不良反应:
是指药品说明书中未载明的不良反应。
说明书中已有描述,但不良反应发生的性质、程度、后果或者频率与说明书描述不一致或者更严重的,按照新的药品不良反应处理。
根据不良反应/事件损害的严重程度,不良反应/事件可能是新的严重的,也可能是新的一般的。
(2)严重药品不良反应,是指因使用药品引起以下损害情形之一的反应:
1)导致死亡;
2)危及生命;
3)致癌、致畸、致出生缺陷;
4)导致显著的或者永久的人体伤残或者器官功能的损伤;
5)导致住院或者住院时间延长;
6)导致其他重要医学事件,如不进行治疗可能出现上述所列情况的。
(3)一般:
指新的、严重的药品不良反应以外的所有不良反应。
4.单位名称:
必须填写单位的完整全称,如日照市人民医院。
5.部门:
应填写科室的标准全称,如:
消化内科、普外三科等。
6.电话:
填写报告部门(即科室)的电话。
7.报告日期:
指上交不良反应/事件报告的时间。
新的或严重的药品不良反应/事件应于发现之日起15日内报告,其中死亡病例须立即报告,其他药品不良反应应30日内报告。
有随访信息的,应当及时报告。
8.患者姓名:
填写患者真实全名。
9.体重:
以千克为单位。
如果不知道准确体重,请做一个最佳的估计。
10.联系方式:
最好填写患者的联系电话,也可填写患者的通信地址。
11.家族药品不良反应/事件及既往药品不良反应/事件情况:
请选择正确选项。
如果选择“有”,则在报告的空白处清晰叙述。
12.不良反应/事件名称:
应填写不良反应中最主要、最明显的症状。
13.不良反应/事件发生时间:
应填写发生不良反应/事件的确切时间。
14.病历(门诊)号:
请如实填写,便于查找病例,具体分析不良反应/事件。
15.不良反应/事件过程描述(包括症状、体征、临床检验等)及处理情况:
不良反应过程描述应具体、规范,须体现出“3个时间、3个项目和2个尽可能”。
*3个时间:
①不良反应发生的时间;②采取措施干预不良反应的时间;③不良反应终结的时间;
*3个项目:
①第一次药品不良反应出现时的相关症状、体征和相关检查;②药品不良反应动态变化的相关症状、体征和相关检查;③发生药品不良反应后采取的干预措施结果;
*2个尽可能:
①不良反应/事件的表现填写时要尽可能明确、具体。
如为过敏型皮疹,要填写皮疹的类型、性质、部位、面积大小等;如为上消化道出血,有呕血者需估计呕血量的多少等;严重病例应注意生命体征指标(体温、血压、脉搏、呼吸)的记录。
②与可疑不良反应/事件有关的辅助检查及临床检验(血常规、肝功能、肾功能、血脂分析、血气、心脏功能等)结果要尽可能明确填写。
如怀疑某药引起血小板减少症,应填写病人用药前的血小板记数情况及用药后的变化情况。
如怀疑某药引起的药物性肝损害,应填写用药前后的肝功变化。
所有检查要注明检查日期。
一般格式为:
患者因×××疾病于×××月×××日(必要时应详细到×××时分)以×××途径给予×××药品,×××剂量,用药×××时间出现×××反应(反应描述须明确、具体),×××时间后给予是否停药及×××处理(包括以×××途径给予×××药品及×××剂量,和其他处理措施),处理后×××时间患者转归情况。
16.商品名称:
如果确定该药品无商品名,填写无。
17.通用名称:
填写完整的药品通用名称,不可使用简称。
18.生产厂家:
填写药品说明书上的药品生产企业的全称,如“山东鲁抗医药股份有限公司”。
19.药品批号及药品批准文号:
区别药品批号和批准文号的概念。
药品批号:
在规定限度内具有同一性质和质量,并在同一连续生产周期中生产出来的一定数量的药品。
药品批号是指用于识别“批”的一组数字或者字母加数字。
用以追溯和审查该批药品的生产历史(如0912001或2009120001)。
药品批号一般和药品的有效期、生产日期在同一位置。
药品批准文号是药品生产合法性的标志,生产药品必须经过国务院药品管理部门批准,并发给药品批准文号(如国药准字H44021518、国药准字Z10890019)等。
2012年新版ADR报表需要正确填写药品批号及药品批准文号。
20.用法用量:
包括每次用药剂量、给药途径、每日给药次数,例如,5mg,口服,每日2次。
21.用药起止时间:
指使用药品的同一剂量的开始时间和停止时间。
22.用药原因:
填写使用该药品的原因,应详细填写。
例如:
患者高血压病史,此次因肺部感染而注射氨苄青霉素引起不良反应,用药原因栏应填写肺部感染。
23.怀疑药品:
是指患者使用的怀疑与不良反应发生有关的药品。
并用药品:
指发生此药品不良反应时患者除怀疑药品外的其他用药情况,包括患者自行购买的药品或中草药等。
24.不良反应/事件结果:
本次不良反应/事件经采取相应的医疗措施后的结果,不是指原患疾病的结果。
患者因不良反应/事件导致死亡时,应指出直接死因和死亡时间。
对于不良反应/事件结果为有后遗症或死亡的病例,应附补充报告(病历资料)。
25.原患疾病:
即病例中的诊断,疾病诊断应写标准全称。
26.对原患疾病的影响:
对原患疾病的影响是指药品不良反应对原患疾病的影响。
27.国内、外有无类似的不良反应:
国内外若有类似的不良反应报道,请简述。
28.关联性评价:
只需填写报告人评价并签名。
29.不良反应分析:
请根据自己的判断在相应方框内打对√。
30.报告人职业和报告人签名:
请按要求填写。
31.备注:
填写以上栏目未能说明的问题。
如有后遗症和死亡病例应在备注中附补充报告(病历资料)。