碳及其化合物课件Word格式.docx
《碳及其化合物课件Word格式.docx》由会员分享,可在线阅读,更多相关《碳及其化合物课件Word格式.docx(28页珍藏版)》请在冰点文库上搜索。
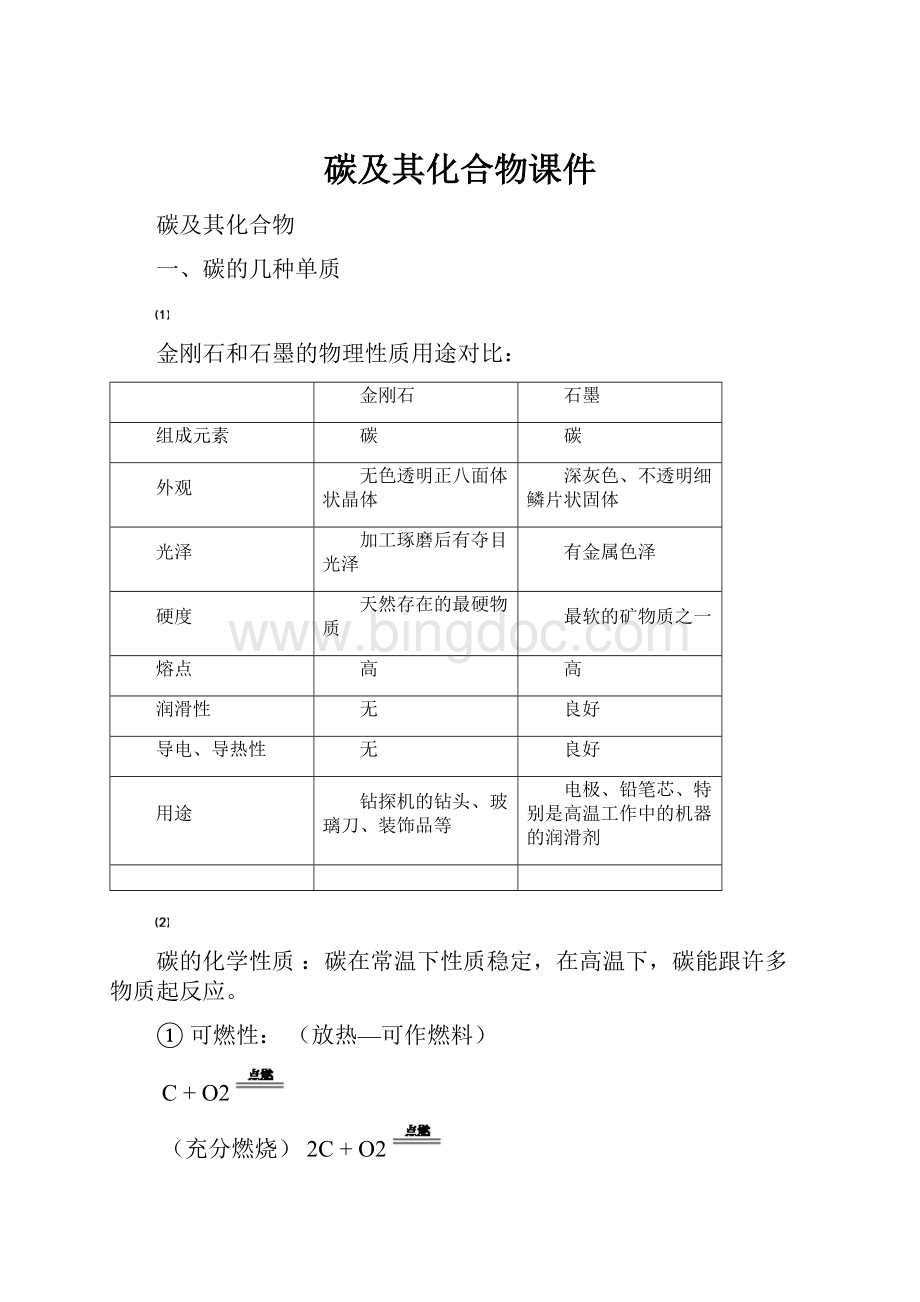
②还原性——冶炼金属
CO+CuO
现象:
黑色氧化铜变成红色,同时生成能使澄清石灰水变浑浊的气体。
③毒性一氧化碳易与血液中的血红蛋结合,使血红蛋白丧失了与氧结合的能力。
(CO排放到空气中会造成空气污染,一半以上的CO来自汽车排放的废气,其余主要来自煤等燃料的燃烧和石油炼制、钢铁冶炼等,森林火灾、海洋和陆地生物的腐烂过程也能产生CO)
2、二氧化碳
、CO2的化学性质
①CO2不能燃烧,不支持燃烧,也不能供给呼吸。
(但CO2是无毒的)
②CO2跟水反应生成碳酸CO2+H2O===碳酸能使紫色石蕊试液变红,
碳酸不稳定,很易分解成水和二氧化碳。
H2CO3===
③CO2能使澄清石灰水变浑浊CO2+Ca(OH)2==
、二氧化碳的重要用途
①灭火②工业原料可制纯碱、尿素和汽水③干冰可作致冷剂、可用于人工降雨④温室肥料。
三、二氧化碳的制法
1.实验室制取气体的思路:
(原理、装置、检验)
(1)发生装置:
由反应物状态及反应条件决定:
反应物是固体,需加热,制气体时则用高锰酸钾或氯酸钾制O2的发生装置。
反应物是固体与液体,不需要加热,制气体时则用过氧化氢制O2的发生装置。
(2)收集方法:
气体的密度及溶解性决定:
难溶于水用排水法收集CO只能用排水法
密度比空气大用向上排空气法CO2只能用向上排空气法
密度比空气小用向下排空气法H2
2.二氧化碳的实验室制法药品:
大理石或石灰石、稀盐酸
(1)原理:
用石灰石和稀盐酸反应:
CaCO3+HCl==
(2)选用和制过氧化氢制取O2相同的发生装置实验操作步骤:
查、装、定、加、收。
(3)气体收集方法:
向上排空气法
(4)验证方法:
将制得的气体通入澄清的石灰水,如能浑浊,则是二氧化碳。
验满方法:
用点燃的木条,放在集气瓶口,木条熄灭。
证明已集满二氧化碳气体。
3.二氧化碳的工业制法:
煅烧石灰石:
CaCO3高温CaO+
生石灰和水反应可得熟石灰:
CaO+H2O=
四、一氧化碳
1.物理性质:
无色,无味的气体,密度比空气略小,难溶于水
2.有毒:
吸进肺里与血液中的血红蛋白结合,使人体缺少氧气而中毒。
3.化学性质:
(H2、CO、C具有相似的化学性质:
①可燃性②还原性)
(1)可燃性:
2CO+O2点燃2CO2(可燃性气体点燃前一定要检验纯度)
H2和O2的燃烧火焰是:
发出淡蓝色的火焰。
CO和O2的燃烧火焰是:
发出蓝色的火焰。
CH4和O2的燃烧火焰是:
发出明亮的蓝色火焰。
鉴别:
H2、CO、CH4可燃性的气体:
看燃烧产物(不可根据火焰颜色)
(水煤气:
H2与CO的混合气体C+H2O高温H2+CO)
(2)还原性:
CO+CuO△Cu+CO2(非置换反应)应用:
冶金工业
现象:
黑色的氧化铜逐渐变成光亮红色,石灰水变浑浊。
Fe2O3+CO高温2(现象:
红棕色粉末逐渐变成黑色,石灰水变浑浊。
)
除杂:
CO[CO2]通入石灰水或氢氧化钠溶液:
CO2+2NaOH==Na2CO3+H2O
CO2[CO]通过灼热的氧化铜CO+CuO△Cu+CO2
CaO[CaCO3]只能煅烧(不可加盐酸)CaCO3高温CaO+CO2↑
注意:
检验CaO是否含CaCO3加盐酸:
CaCO3+2HCl==CaCl2+H2O+CO2↑
(CO32-的检验:
先加盐酸,然后将产生的气体通入澄清石灰水。
五、H2、CO、C还原CuO实验的比较
H2还原CuO
CO还原CuO
C还原CuO
化学方程式
H2+CuO
Cu+H2O
CO+CuO
Cu+CO2
C+2CuO
2Cu+CO2↑
装置图
装置特点
①试管口略向___倾斜;
②通H2的导管伸至试管底部于CuO上方
因CO有____,增加对尾气处理装置,防止CO污染空气
①试管口略向下倾斜;
②反应需高温;
操作步骤
反应前需检验气体纯度。
还原过程分四步:
一通,二点,三撤,四停
①检查气密性;
②装药品固定试管;
③点燃;
④移导管,熄灭酒精灯。
实验现象
①黑色CuO变成___色;
②试管口有___生成
②生成的气体使澄清石灰水变浑浊
①黑色固体逐渐减少;
②有光亮红色固体生成;
③生成的气体使澄清石灰水变浑浊
六、O2、H2、CO2的实验室制法比较
氧气(O2)
氢气(H2)
二氧化碳(CO2)
反应原理
2KClO32KCl+3O2↑
2KMnO4
K2MnO4+MnO2+O2↑
Zn+H2SO4==ZnSO4+H2↑
Zn+2HCl=ZnCl2+H2↑
CaCO3+2HCl==CaCl2+H2O+CO2↑
发生装置
收置方法
①向上排空气法(密度比空气大);
②排水法(不易溶于水)
①向下排空气法(密度比空气小);
②排水法(难溶于水)
只能用向上排空气法(密度比空气大,能溶于水)
①组装仪器②检查装置的气密性③装药品④固定装置⑤加热⑥收集气体⑦把导管撤出水槽⑧熄灭酒精灯。
①组装仪器②检查装置的气密性③加药品④验纯⑤收集气体
①组装仪器②检查装置的气密性③加入大理石④从漏斗注入稀盐酸⑤收集气体
验满
向上排空气法收集时,用带火星的木条放在集气瓶口,木条复燃,说明收集已满。
排水法收集时,气泡往集气瓶外冒时,收集已满。
用排水法收集时,当气泡往外冒时,说明收集已满。
用燃着的木条放在集气瓶口,若木条熄灭,说明收集已满。
检验或验纯
验证:
用带火星木条伸入集气瓶内,木条复燃,说明是氧气
验纯:
收集一试管氢气,用大拇指堵住,管口向下,移近酒精灯火焰,若发出微弱的“噗”的一声,说明氢气已纯,若发出尖锐的爆鸣声,说明氢气不纯,应再收集再检验。
通入澄清石灰水,石灰水变浑浊,说明是二氧化碳。
[CO2+Ca(OH)2==CaCO3↓+H2O]
注意事项
试管口应略向下倾斜,以防水倒流至试管底部,使试管炸裂;
排水法收集时当气泡连续均匀冒出时开始收集,以免收集气体不纯;
排水法收集完后,先将导管移出水槽,再停止加热,以免水槽中的水倒流至热试管,使试管炸裂。
长颈漏斗下端应伸入液面以下,以免生成的气体从长颈漏斗中逸出;
用排空气法收集时,导管应伸入集气瓶底部;
验纯时,浓盐酸有挥发性,浓硫酸、硝酸具有强氧化性,Cu等金属不与稀酸反应,所以都不宜用来制氢气。
不能用稀H2SO4代替稀盐酸,因为稀H2SO4与CaCO3反应生成微溶性的CaSO4覆盖在CaCO3表面,从而阻止反应的进一步进行。
例1、如何证明金刚石和石墨都是由碳元素组成的?
既然金刚石和石墨都是由碳元素组成的,为什么它们的物理性质差别很大?
它们应有怎样的化学性质呢?
石墨和金刚石之间的转化属于什么变化?
例2、某物质经分析测定后得知仅含一种元素,则此物质()
A.一定是一种单质B.一定是一种纯净物
C.一定是一种混合物D.可能是混合物,也可能是纯净物。
例3、将下列各种物质及其对应的用途连接起来
【例4、】请设计一个个方案,证明足球烯和碳纳米管都是由碳元素组成的(以足球烯为例,用文字叙述)。
【例5、】由碳、氧两种元素组成的气体中,碳与氧的质量比为35,则该项气体可能是()
A.由CO或CO2单独组成的纯净物B.由CO和CO2共同组成的混合物
C.由CO和O2共同组成的混合物D.由CO2和O2共同组成的混合物
【例6、】
1请区别H2、CO、CO2三种无色气体。
②CO和CO2的组成元素相同,为什么性质差别很大?
怎样除去CO2中少量CO?
如何除去CO中少量的CO2?
③某混合气体可能含有CO、CO2、H2和N2,将混合气体依次通过炽热的焦炭、澄清石灰水、灼热的氧化铜和无水氯化钙(假设每通过一种物质,参与反应的气体都反应完全),最后得到的气体是________。
【例7、】为什么不用碳酸钙和稀盐酸制取CO2?
为什么不用石灰石与稀硫酸反应制CO2?
【例8、】在做氢气还原氧化铜实验中,出现下列三种异常现象:
①事先已检验证明,通入盛CuO试管中的H2是纯净的,在加热时试管中出现了爆呜声,②在试管中有亮红色物质出现时,试管底部出现破裂现象,③试管中CuO变红后又渐渐变成黑色。
试从操作和装置等方面分析出现上述现象原因:
【例9、】在日常生活中我们常听说开门七件事:
①柴;
②米;
③油;
④盐;
⑤酱;
⑥醋;
⑦茶,你认为其中所指物质属于有机物的是()
A、①②③④⑤⑥B、④C、除④以外D、都不是
【例10、】能源可划分为一级能源和二级能源。
自然界里能直接提提供的是一级能源,需要消耗其他能源间接获取的能源为二级能源。
根据上述的判断,下列物质中属于一级能源的有________,属于二级能源的是__________。
(填序号)
1氢气②天然气③煤、石油④煤气⑤酒精⑥太阳能、风能⑦核能
【例11、】石灰石是我省的主要矿产之一。
学校研究性学小组为了测定当地矿山石灰石中碳酸钙的质量分数。
取来了矿石样品,并取稀盐酸200g,平均分成4份,进行实验,结果如下:
实验
1
2
3
4
加入样品的质量/g
5
10
15
20
生成CO2的质量/g
1.76
3.52
4.4
m
⑴哪几次反应中矿石有剩余?
⑵试计算这种石灰石中碳酸钙的质量分数。
⑶上表中m值是。
【例12、】无色气体A是O2、H2、CO、CO2中的一种或两种还原性气体,黑色固体粉末B是氧化铜粉或木炭粉中的一种或两种。
请回答:
(用化学式表示)
(1)当B为纯净物时,将无色气体A通入黑色粉末B,在加热的条件下发生反应,有无色液体产生,将反应后的气体通入澄清的石灰水中,能使石灰水变浑浊。
由此推断无色气体A是,黑色粉末B是。
(2)当A为纯净物时,将无色气体A通入黑色粉末B,在高温下发生反应,有无色液体产生,将反应后的气体通入澄清的石灰水中,能使石灰水变浑浊。
由此推断无色气体A一定是,黑色粉末B是。
【例13、】、一氧化碳中混有少量二氧化碳,可以让混和气体通过____除去二氧化碳。
氯化亚铁溶液中混有氯化铜可用与____反应除去氯化铜,然后再进行操作。
【例14、】某同学去我市的石树风景区游玩时,取回了若干块矿石样品,他对样品中的碳酸钙的质量分数进行检测,采用了以下的办法:
取用这种石灰石样品,把40g盐酸分四次加入,测量过程所得数据见下表(巳知石灰石样品中含有的杂质不溶于水,不与盐酸反应)。
请计算:
(1)8g的石灰石样品中含有杂质多少克?
(2)样品中碳酸钙的质量分数是多少?
(3)下表中,m的数值应为多少?
(4)要得到280kg的CaO,需要质量分数为80%的石灰石多少千克?
(化学方程式为CaCO3
CaO+CO2↑)
序号
加入稀盐酸的质量(g)
剩余固体的质量(g)
第1次
5.5
第2次
第3次
1.2
第4次
针对性练习
1.下列对a、b、c、d四套装置中,在注入酸起反应后对气球的变化情况作出正确分析的是()
A.气球①不胀大,②-④都能迅速胀大
B.气球②逐渐胀大,气球④迅速胀大
C.气球②逐渐胀大,气球③缓缓膨胀后停止,气球④迅速胀大
D.以上都不正确
2.以下是化学实验室内几种常用的实验装置,请回答:
(1)某同学用
装置制取并用
收集一瓶氧气,反应的化学反应方程式为
,采用排水集气法收集氧气不纯原因可能是
.
(2)若要制取二氧化碳,在C装置中装有石灰石,那么a中应加入
(填写试剂名称),反应的化学方程式是
.用
装置收集该气体.
(3)在加热的条件下,用固体碱石灰和无水醋酸钠制取甲烷气体,甲烷是不易溶于水、密度比空气小的无色无味的气体,应选用的发生装置是
;
收集装置是
.
3.今有A、B、C、D、E五种装置如图所示
按下列要求回答问题(所选装置用其代号字母表示)
(1)实验室用高锰酸钾的加热分解来制取氧气时,发生装置选用
,收集装置选用
,该装置制取氧气的化学方程式为
(2)实验室用大理石和稀盐酸来制取二氧化碳时,发生装置选用
,收集装置选用
,该制取二氧化碳的化学方程式为
(3)硫化氢是一种无色且有臭鸡蛋气味的气体,能溶于水,可形成一种酸溶液--氢硫酸.实验室用硫化亚铁跟稀硫酸反应制取硫化氢气体.试回答:
①硫化氢气体具有臭鸡蛋气味,这是硫化氢的
(填“物理”或“化学”)性质.
②硫化氢的水溶液能使石蕊试液变
色.
③实验室制取H2S气体时,发生装置应选用
,收集装置应选用
(填仪器编号).
4.如图为用过量的木炭还原氧化铜的实验装置.请回答下列有关问题:
(1)实验过程中首先观察到的又能证明炭与CuO发生化学变化的现象是
(2)a处排出的气体中,除含有未排尽的空气和未被完全吸收的CO2外,还一定含有
气体,写出有关的化学方程式
(3)酒精灯上加一网罩的作用是
(4)还原完毕后应进行的操作是(填序号)
A.先停止加热,再拨开管口的橡皮塞
B.先拨开管口的橡皮塞,再停止加热
C.先将洗气瓶中液面下的导管移到液面上,再停止加热
(5)该装置有什么缺陷,请你指出来:
(6)最能说明试管中反应已完成的实验现象是
5.某化学课外兴趣小组成员甲、乙、丙三位同学在学习了木炭还原氧化铜的实验后,提出如下问题:
“木炭与一氧化铅(化学式为PbO)反应生成铅的同时产生的气体一定全部为二氧化碳吗?
”请你和他们一起对产物中气体的成分进行研究,并回答有关问题.
(1)[猜想]:
甲同学认为:
反应产生的气体全部为二氧化碳.
乙同学认为:
反应产生的气体全部为一氧化碳.
丙同学认为:
反应产生的气体既有二氧化碳又有一氧化碳.
(2)[设计实验]:
根据各自的猜想,他们共同设计了实验(如图示),(他们在实验中进行了规范操作和细致的观察).
(3)[现象与结论]:
(提示:
CO会使新鲜鸡血变色)
如果甲同学猜想正确,装置B、C中的实验现象是
,
如果乙同学猜想正确,装置B、C中的实验现象是
如果丙同学猜想正确,装置B、C中的实验现象是
(4)此实验装置有不足之处,请你对该装置进行改进,具体措施是
(5)根据上述实验及学习的木炭与CuO、Fe2O3的反应,请你归纳出单质碳的一项重要用途是.
6.我们知道,物质的结构决定性质,性质决定用途,用途体现性质,请据此填空:
(1)因为木炭和活性炭具有疏松多孔的结构,所以具有
性;
(2)因为金刚石和石墨的
不同,所以它们的物理性质不同;
(3)因为石墨具有
性,所以能做电极、电刷;
(4)因为金属钨的
高,所以用作电灯泡的灯丝.
7.某学校的探究性学习小组发现,铜绿[Cu2(OH)2CO3]受热分解后,除生成CO2和水蒸气外,试管中还有一些黑色粉末状固体.他们通过实验探究,分析黑色固体的组成,并验证产生的气体.请填空:
(1)提出问题:
黑色固体是什么?
(2)猜想与假设:
黑色固体可能是:
a.炭粉
b.氧化铜
c.
(3)查阅资料:
炭粉和氧化铜均为黑色固体,其中炭粉不与稀酸反应,也不溶于稀酸,而氧化铜可与稀酸反应而溶解.
(4)设计实验方案:
向试管中的黑色固体滴加足量的
(填化学式)溶液,充分反应后,观察固体的溶解情况和所得溶液的颜色.
(5)现象与结论:
如果猜想a正确,则现象为
若现象是
,则猜想b正确;
假如现象为
,则猜想c成立.
(6)已知:
无水硫酸铜固体为白色,遇水蒸气则变为蓝色.若用右图装置验证两种气体生成物,应将生成的混合气体先通过
装置.当将气体通入装置A进行验证时,气流应从
口通入.
8.现有下列物质:
①活性炭
②一氧化碳③二氧化碳
④氢气,
请按以下要求填空.(只填序号)
(1)能用于灭火的是
(2)煤气的主要成分是
(3)可用于除去冰箱异味的是
(4)植物进行光合作用的原料是
(5)产生“温室效应”的主要原因之一是大量含碳物质的燃烧,导致大气中
的含量增大.为了减缓此现象,最理想的燃料是
9.某化学兴趣小组根据如图所示进行模拟炼铁的实验,并对产物成分进行探究.
经初步分析:
无色气体A不含有单质气体,黑色粉末B含有两种单质中的一种或者两种.
高炉炼铁的原理为:
Fe2O3+3CO
2Fe+3CO2,请写出反应器中一氧化碳是如何产生的化学方程式:
兴趣小组又分成甲乙两组分别对无色气体A和黑色粉末B的成分进行探究.
【猜想与假设】
甲组在分析了炼铁的原理后,认为无色气体A中可能有CO2,也可能有未反应的
.乙组认为黑色粉末的成分中存在以下三种情况:
假设一:
只含有铁.
假设二:
只含有
.
假设三:
以上两种物质都含有.
【实验与探究】
(1)为验证甲组的猜想,大家按如图示进行实验(箭头表示气体流向):
当看到Ⅰ中澄清石灰水变浑浊,Ⅲ中灼热的氧化铜变红,可以确定无色气体A的成分为:
,Ⅱ中浓硫酸的作用是:
(2)为验证乙组中假设三成立,大家用物理和化学两种方法来进行探究
实验方法
实验操作
实验结果
物理方法
假设三成立
化学方法
取少量黑色粉末B于试管中,加入过量的稀盐酸
写出黑色粉末B中加入过量的稀盐酸反应的化学方程式:
【交流与反思】在做甲组的实验中发现其存在一个很不环保的缺陷,请指出来
10.下图是有关氧气的知识网络图(部分反应条件已略去).
根据上图回答下列问题:
(1)生成氧气的两个反应都属于
反应(填基本反应类型),从节能、环保的角度考虑,实验室制取氧气最好选用
作反应物.
(2)X的化学式为
;
若反应①在氧气充足的条件下进行,生成X的化学式为
(3)若反应②的化学方程式为Y+5O2
3CO2+4H2O,Y的化学式为
(4)写出反应③的化学方程式
(5)在做反应④实验时,要预先在盛放氧气的集气瓶中放
11.从下列物质中,选择正确答案填在相应的空格里
①石墨
②干冰
③活性炭
④金刚石
⑤炭黑
(1)可用于人工降雨的是
(填序号,下同)
(2)用来切割玻璃的是
(3)能吸附有毒气体,常用于防毒面具中作吸附剂的是
(4)可用来作电极的是
12.九
(1)班化学兴趣小组成员张强、刘明和汪梅三同学在学习了木炭还原氧化铜的实验后,提出如下问题:
“木炭与氧化铅(化学式为PbO)反应生成铅的同时产生的气体一定全部是二氧化碳吗?
(1)猜想:
张强认为:
反应产生的气体全部是一氧化碳;
刘明认为:
反应产生的气体全部是二氧化碳;
汪梅认为:
(2)设计实验:
根据各自的猜想,他们共同设计了实验,实验装置如图(他们在实验中进行了规范操作和细致的观察)
(3)现象与结论:
(“实验中所用的新鲜鸡血是指先加入抗凝剂,再用水稀释后的鸡血.它遇O2呈鲜红色,遇CO2呈暗红色,遇CO呈胭脂红.”)如果张强猜想正确,装置B、C中的实验现象分别是_
如果汪梅猜想正确,装置B、C中的实验现象分别是
(4)从环保角度考虑该实验装置有不足之处是
请你对该装置进行改进,具体措施是
(5)根据上述实验及木炭与CuO的反应,请你归纳出单质碳的一项用途_
_
,
13.分如图A、B、C、D四个实验是九年级上册我们的实验探究,请回答:
(1)A实验的目的是
(2)B实验中B烧杯的作用是
(3)C实验是木炭还原氧化铜的实验,我们发现澄清石灰水会变浑浊,请写出澄清石灰水变浑浊的化学方程式
(4)D实验中小花变红的是
(填序号),该实验④发生反应的化学方程式是:
14.有A、B、C、D、E、F六种物质,其中A、B、C、D、E五种物质的组成中均含有同一种元素,A、F为单质,其余为化合物,D是鸡蛋壳及石灰石的主要成分.它们之间有如下转化关系(一些必要的反应物和反应条件已略去):
(1)写出A和D的名称:
A
,D
(2)向E的溶液中滴加紫色石蕊溶液的现象是
(3)写出反应④的化学方程式:
等;
(4)指出反应⑤在物质鉴别中的应用:
(5)从反应①②可得到的启示是:
15.水是人类生活中不可缺少的物质
(1)去年冬天至今年春天,我国西南地区遭遇大范围持续干旱.有些村庄打深井取用地下水.检验地下水是硬水还是软水,可用的物质是
,测定地下水的酸碱度可用
(2)有些村民取浑浊的坑水作生活用水.有同学利用所学的知识浑浊的坑水用图所示的简易净水器进行净化,其中小卵石、石英沙的作用是
活性炭的作用是
(3)如果地下水硬度大,或者坑水中病原微生物过多,都可以采取
方法,来降低硬度和杀灭病原微生物.
(4)下列物质都可用于水质的净化或杀菌消毒.
①臭氧(化学式O3):
有强氧化性,可用于游泳池、生活用水、污水的杀菌和消毒.臭氧和氧气组成元素相同而化学性质不同的原因是
②漂白粉:
可用于水的杀菌消毒,其有效成分是次氯酸钙[化学式为Ca(ClO)2].次氯酸钙可发