初中科学浙教版八年级下册第三章第四节二氧化碳练习题普通用卷Word文档下载推荐.docx
《初中科学浙教版八年级下册第三章第四节二氧化碳练习题普通用卷Word文档下载推荐.docx》由会员分享,可在线阅读,更多相关《初中科学浙教版八年级下册第三章第四节二氧化碳练习题普通用卷Word文档下载推荐.docx(22页珍藏版)》请在冰点文库上搜索。
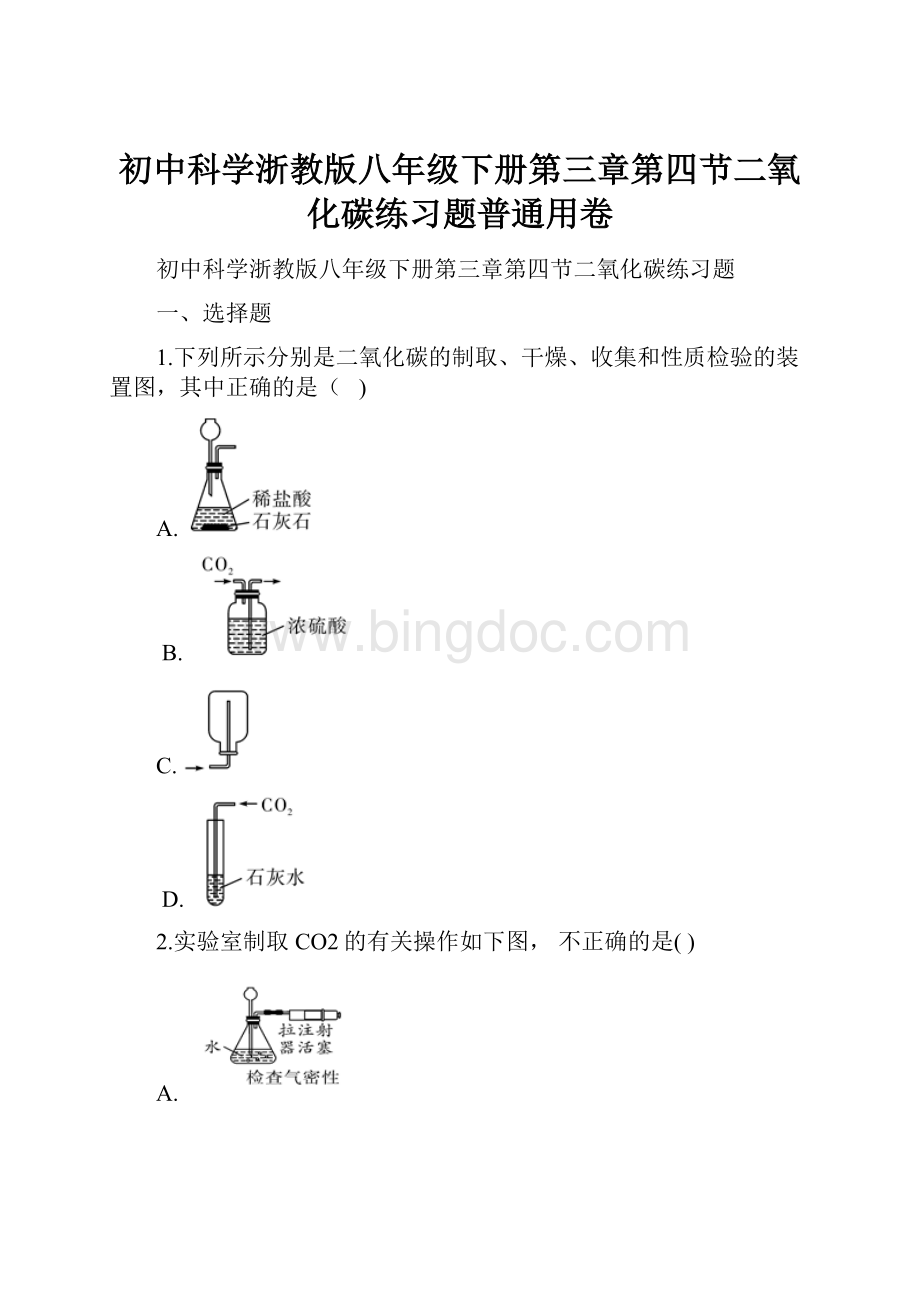
C.分别闻两种气体的气味
D.加入少量澄清的石灰水,振荡后观察
8.以下对二氧化碳的叙述不正确的是()
A.干冰是固体二氧化碳B.二氧化碳不支持燃烧
C.二氧化碳有毒D.二氧化碳密度比空气大
9.下列关于CO2的实验室制法及性质实验的说法不正确的是
(
)
A.制CO2的药品
B.发生装置
C.收集装置
D.比较CO2与空气的密度
A.AB.BC.CD.D
10.用下图装置进行CO2性质实验。
下列说法正确的是(
A.①证明是CO2使石蕊变红B.②可用于检验CO2气体
C.③观察到蜡烛自上而下依次熄灭D.①②③只能验证CO2化学性质
11.下列有关验证二氧化碳性质的实验中,只和它的物理性质有关的是()
12.下列说法正确的是()
A.CO2通入紫色石蕊试液中,液体变红,说明CO2能使紫色石蕊变红
B.检验家用液化石油罐的罐阀或减压阀是否漏气可用肥皂水
C.干冰和可燃冰都是纯净物,化学式相同,都为H2O
D.可燃物燃烧时温度需要达到着火点,所以可燃物的温度达到着火点一定能燃烧
13.下图是模拟二氧化碳的实验室制法、性质的检验等的综合实验,描述正确的是
A.本实验过程涉及到2个化学反应
B.1处变红
C.制备二氧化碳需要加热才能进行
D.3处会产生白色浑浊
14.如图,将充满CO2的试管倒扣在滴有紫色石蕊的蒸溜水中,一段时间后,下列实验现象描述正确的是()
①试管内液面上升
②试管内溶液变红
③试管内液面不上升
④试管内溶液变蓝
⑤试管内溶液不变色
A.①②B.①④C.②③D.③⑤
二、填空题
15.某同学设计如图所示实验,探究二氧化碳的有关性质,请填空。
(1)实验1中干紫色石蕊纸花喷水后放入二氧化碳中,观察到的现象是___________,该反应的化学方程式是_______________________。
(2)实验2是在实验1的基础上设计的创新改进实验,将二氧化碳缓慢通入竖直放置的玻璃管中,能观察到第_______(填序号)号棉球先变色,通过此现象可获得关于二氧化碳的另外一条性质是____________________。
16.
二氧化碳是我们身边重要的化学物质,将蘸有酒精的棉芯点燃放入烧杯中,向烧杯中缓缓倾倒二氧化碳,观察到烧杯中的棉芯自下而上熄灭,如图。
该实验中发生反应的化学方程式为______,
该实验说明二氧化碳具有的性质有______。
植物光合作用的化学方程式为:
6CO2+6H2O
6O2+X,则X的化学式为______。
17.“温控保鲜”和“气调保鲜”是两类食品保鲜技术。
它们通过降低温度和改变气体成分,达到抑制被储藏物细胞呼吸的目的。
(1)干冰可用于“温控保鲜”,利用干冰的性质是_____。
(2)“气调保鲜”中可使用CO2来抑制细菌。
CO2进入细菌细胞液后能产生酸性物质,抑制细菌生长。
请用化学方程式解释酸性物质的产生:
_____。
(3)冰箱中常用如图所示的膜分离技术实现“气调保鲜”。
分离后,通入冰箱保鲜室内的气体是_____(填“富氮空气”或“富氧空气”)。
18.碳和碳的化合物是非常重要的物质。
(1)将CO2通过灼热的碳层,该反应的化学方程式是_______________________;
此反应体现了CO2具有的化学性质是_________(填序号)。
A.导热性
B.还原性
C.氧化性
D.可燃性
(2)用如图所示装置研究CO2的性质,其中①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球。
说明CO2密度大于空气的实验现象是___________。
该实验还能研究的二氧化碳的性质是___________。
(3)将二氧化碳通入紫色石蕊试液中,溶液由紫色变为红色,化学方程式为_________________________。
将溶液加热至沸腾,溶液由红色又变为紫色,化学方程式为_________________________________。
三、分析计算题
19.请列实验常用装置,回答有关问题。
(1)图中标有字母的仪器名称:
a_____。
(2)若要制取二氧化碳,应选用的发生装置是__________
(填“A”或“B”),那么a中应加入___
(填写试剂名称),反应的化学方程式是____________;
如果用E装置收集该气体,则气体从___端进入(填“b”或“c”)。
(3)仪器a的下端要插入液面以下,原因是_______________________。
(4)实验室如用块状固体和液体无需加热制取难溶性气体,可将B装置改进为C装置(多孔隔板用来放块状固体),其优点是___________。
(5)200g稀硫酸与足量锌反应,生成0.4g氢气.求原硫酸溶液中溶质的质量分数。
四、解答题
20.实验室按图所示装置制取CO2,并验证实验CO2的性质.回答以下问题.
(1)上图中有一处明显的错误,请指出:
__________________________。
(2)装置B用来证明CO2能与水反应生成碳酸,B中应加入的试剂是____________,实验现象是_________ 。
(3)
装置C中盛有澄清的石灰水,通入CO2的实验现象是_____________________。
(4)装置D中,___________蜡烛先熄灭,___________蜡烛后熄灭,说明二氧化碳有_______________的化学性质,_______________的物理性质,因此可以用二氧化碳来_________________。
21.实验室用下图装置进行二氧化碳的制取和性质实验。
(1)A中发生反应的化学方程式是________。
(2)B中发生的反应的化学方程式是________。
(3)用化学方程式解释澄清石灰水变浑浊的原因是_______。
(4)将C中的导气管取出,伸入D中(如图所示),蜡烛由低到高依次熄灭。
说明二氧化碳具有的性质是________。
22.化学是一门研究物质的科学,我们一般从物质的组成(或构成)、性质、用途等方面研究一种物质。
以二氧化碳为例,请回答相关问题:
(1)如图甲所示实验中,a、d为用紫色石蕊试液润湿的棉球,b、c为用石蕊试液染成紫色的干燥棉球。
缓慢通入CO2一段时间后观察到:
d比a先变红,b、c不变红,此现象说明CO2具有的物理性质是______,化学性质是______。
(2)如图乙所示实验,将注射器中的Ca(OH)2溶液注入锥形瓶中,振荡,观察到瓶中小气球的变化是______;
发生这种变化的原因是______(用化学方程式表示)。
(3)利用CO2不燃烧,也不支持燃烧,且密度比空气大的性质,CO2在生活中可用于______。
答案和解析
1.【答案】D
【解析】
【分析】
本题主要考查气体的制取装置和收集装置的选择,同时也考查了二氧化碳的检验和干燥等,综合性比较强。
气体的制取装置的选择与反应物的状态和反应的条件有关;
气体的收集装置的选择与气体的密度和溶解性有关。
本考点是中考的重要考点之一,主要出现在实验题中。
【解答】
A.图示为制取二氧化碳的发生装置,装置中长颈漏斗未伸入液面以下,气体从长颈漏斗逸出,故A不正确;
B.图示为使用浓硫酸干燥二氧化碳气体的装置,应该长进短出,进气口和出气口反了,故B不正确;
C.图示为气体的收集装置,集气瓶瓶口向下,为向下排空气法收集气体,二氧化碳密度大于空气,应采取向上排空气法收集,故C不正确;
D.二氧化碳一般用澄清石灰水检验:
把气体通入澄清石灰水中,石灰水变浑浊,故D正确。
故选D。
2.【答案】B
本题难度不大,掌握实验室制取二氧化碳的反应原理、注意事项等是正确解答本题的关键。
A.根据检查气密性的方法解答;
B.根据制取二氧化碳的药品进行解答;
C.根据二氧化碳的密度进行解答;
D.根据二氧化碳气体检验方法解答。
A.检查装置气密性时,拉动注射器时,如果长颈漏斗末端产生气泡,说明装置不漏气,反之则漏气,故A选项正确;
B.稀硫酸与块状石灰石反应生成微溶于水的硫酸钙,会覆盖在石灰石表面,阻止反应的进行,不能用于制取CO2,故B选项错误;
C.二氧化碳的密度比空气的大,用图中装置收集二氧化碳时,长导管是进气管,将空气从短导管排出,故C选项正确;
D.因为二氧化碳不能燃烧,不支持燃烧,验满时应将燃着的木条放在短导管口,木条熄灭,说明集满了二氧化碳,故D选项正确。
故选B。
3.【答案】D
本题主要考查实验方案的设计与评价,掌握每个实验的实验原理、注意事项等知识是正确解答本题的关键。
A.白磷燃烧产生大量有毒的白烟,在试管的上方套上气球可以防止产生的白烟逸散到空气中,防止空气污染,能达到实验目的,故A不符合题意;
B.下层的蜡烛先熄灭,上层的蜡烛后熄灭,说明了CO2密度比空气大,能达到实验目的,故B不符合题意;
C.关闭弹簧夹,向长颈漏斗中加水,若长颈漏斗内能形成一段稳定的水柱,说明气密性良好,能达到实验目的,故C不符合题意;
D.左侧试管内的导气管在液面以下,气体无法排出,无法收集二氧化碳气体,即无法制取CO2,不能达到实验目的,故D符合题意。
4.【答案】A
本题考查了二氧化碳的实验室制法以及性质的探究,熟练掌握二氧化碳的化学性质、物理性质、二氧化碳的实验室制法等是正确解答本题的关键。
A.二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊变红色,但是不能说二氧化碳使紫色石蕊变红色,故A选项说法错误;
B.二氧化碳和氢氧化钙反应会生成碳酸钙沉淀和水,所以C处溶液变浑浊,故B选项说法正确;
C.二氧化碳的密度比空气大,不能燃烧,没有助燃性,所以D处的实验现象是下层蜡烛先熄灭,上层蜡烛后熄灭,故C选项说法正确;
D.通过C中分析可知,D处现象说明二氧化碳不可燃,不助燃,密度比空气大,故D选项说法正确。
故选A。
5.【答案】D
本题考查二氧化碳的制取、验满、性质探究,难度不大。
A.因实验室制取二氧化碳是利用碳酸钙与盐酸反应来制取,若选用硫酸,因硫酸钙微溶,包裹在碳酸钙的表面将阻止反应的进行,故A错误;
B.验满二氧化碳应该将燃着的木条放在集气瓶口,而不是伸到瓶内,故B错误;
C.紫色石蕊试液变为红色,说明CO2气体和水反应产生的碳酸使石蕊试液变成红色,而不是二氧化碳显酸性,故C错误;
D.低处的蜡烛先熄灭,既能说明CO2的密度比空气大,又能说明CO2不能燃烧也不支持燃烧,故D正确。
6.【答案】D
本题考查了学生分析问题的能力,通过对碳酸饮料的成分的分析进行合理的说明,要注意说明要有理有据。
打开碳酸饮料汽水瓶盖可观察到有气泡冒出,这个事实说明二氧化碳能与水反应生成碳酸。
故选D。
7.【答案】D
根据氮气和二氧化碳的性质分析,气体都是很轻的,不易用托盘天平称量来区分;
二者都不支持燃烧;
二者都无气味;
二氧化碳遇石灰水变浑浊,而氮气不会.二氧化碳遇石灰水变浑浊,是二氧化碳的特性,可用于与其他气体区分.
A、气体相对来说都是很轻的,不易用托盘天平称量来区分,故A错误;
B、氮气和二氧化碳都不支持燃烧,所以用带火星的木条伸人瓶底,木条会熄灭,故无法区分,故B错误;
C、氮气和二氧化碳都是没有气味的气体,无法用闻气味的方法区分,故C错误;
D、二氧化碳遇石灰水变浑浊,而氮气不会,所以加入少量澄清的石灰水,振荡后可以区分氮气和二氧化碳,故D正确。
故选:
D。
8.【答案】C
本题考查二氧化碳的性质、俗称和用途,熟练掌握二氧化碳的性质和用途是解题的关键。
A.干冰是固体二氧化碳,故正确;
B.二氧化碳不支持燃烧,故正确;
C.二氧化碳没有毒,故错误;
D.二氧化碳密度比空气大,故正确。
9.【答案】A
本题考查CO2的实验室制法及性质实验,难度不大,理解实验室制取CO2原理、装置及CO2性质是解题关键。
A.实验室制取CO2的药品为大理石或石灰石和稀盐酸,不能用稀硫酸,因为生成的硫酸钙微溶,覆盖在块状固体表面,阻止反应进行,A项错误;
B.实验室制取CO2用大理石或石灰石和稀盐酸在常温下反应,图中是固液常温下制取气体的发生装置,B项正确;
C.二氧化碳密度比空气大,可用向上排空气法收集,C项正确;
D.根据蜡烛自下而上依次熄灭,可比较CO2与空气的密度,D项正确。
10.【答案】B
根据二氧化碳反应生成碳酸分析;
根据二氧化碳能使澄清石灰水变浑浊分析;
根据二氧化碳的密度大于空气密度,不燃烧也不支持燃烧分析。
本题是对二氧化碳性质的考查,验证二氧化碳能否使紫色石蕊变红,需要排除水的干扰。
A.①不能证明CO2使石蕊变红,A错误;
B.常用澄清石灰水检验二氧化碳,B正确;
C.③观察到蜡烛自下而上依次熄灭,C错误;
D.③中还能得出二氧化碳的密度大于空气密度,D错误。
11.【答案】D
【解析】解:
A、稀盐酸和石灰石反应生气二氧化碳,二氧化碳使两支蜡烛从下到上依次熄灭,下面的先熄灭说明二氧化碳的密度比空气大,属二氧化碳的物理性质,蜡烛熄灭说明二氧化碳不燃烧也不支持燃烧,属于二氧化碳的化学性质,所以A不正确;
B、该实验二氧化碳和石灰水反应生成白色沉淀,属于二氧化碳的化学性质,所以B不正确;
C、二氧化碳溶于水能与水反应生成碳酸,碳酸使紫色的石蕊试液变红,这属于二氧化碳的化学性质,所以C不正确;
D、由于二氧化碳的密度比空气大,该操作只体现了二氧化碳的物理性质,所以D正确.
故选D
本题可以根据二氧化碳的物理性质和化学性质进行分析解答.以实验的形式验证了二氧化碳的性质,易于学生的掌握.
12.【答案】B
本题主要考查了燃烧的条件、二氧化碳的性质等,难度不大,根据已有的知识分析解答即可。
A.二氧化碳通入紫色石蕊试液,溶液变红,是因为二氧化碳与水化合生成了碳酸,碳酸使紫色石蕊变红,故A说法错误;
B.检验家用液化石油罐的罐阀或减压阀是否漏气可用肥皂水看是否有气泡,无气泡则不漏气,故B说法正确;
C.干冰是固态二氧化碳,其化学式为CO2,可燃冰是甲烷水合物,两者化学式不同,故C说法错误;
D.可燃物燃烧时温度需要达到着火点,但是可燃物的温度达到着火点不一定能燃烧,因为燃烧还需要可燃物与氧气接触,故D说法错误。
13.【答案】D
本题考查模拟二氧化碳的实验室制法,涉及二氧化碳的制备和性质,难度不大。
A.稀盐酸与石灰石反应生成氯化钙、二氧化碳和水;
二氧化碳和水反应生成碳酸,碳酸能使紫色的石蕊溶液变成红色;
二氧化碳能使澄清的石灰水变浑浊;
因此本实验过程涉及不止2个化学反应,故错误;
B.2处是紫色石蕊溶液,应变红,1处是蒸馏水,不会变红,故错误;
C.常温下石灰石和稀盐酸就可以反应产生二氧化碳,无需加热,故错误;
D.3处为澄清石灰水,二氧化碳与澄清石灰水反应会产生白色浑浊,故正确。
故选D。
14.【答案】A
本题难度不大,主要考查二氧化碳的性质,根据二氧化碳与水的反应及指示剂的性质分析。
将充满二氧化碳的试管倒扣在滴有紫色石蕊的蒸馏水中,一段时间后,二氧化碳溶于水并与水反应生成碳酸,试管内气压变小,故可以看到试管内液面上升。
碳酸有酸性,能使紫色石蕊变红,故可以看到试管内溶液变红,故A正确。
故选A。
15.【答案】
(1)石蕊纸花变红色
;
CO2+H2O═H2CO3
(2)④;
二氧化碳密度比空气大
本题考查探究二氧化碳的性质,依据实验现象和物质的性质作答。
(1)实验1中干紫色石蕊纸花喷水后放入二氧化碳中,观察到的现象是石蕊纸花变红色,是因为二氧化碳和水反应生成了碳酸,碳酸能使石蕊纸花变红,该反应的化学方程式是CO2+H2O═H2CO3;
(2)实验2是在实验1的基础上设计的创新改进实验,将二氧化碳缓慢通入竖直放置的玻璃管中,能观察到第④号棉球先变色,通过此现象可获得关于二氧化碳的另外一条性质是二氧化碳密度比空气大。
16.【答案】C2H5OH+3O2
2CO2+3H2O;
不能燃烧,也不能支持燃烧,密度比空气密度大;
C6H12O6
将蘸有酒精的棉芯点燃放入烧杯中,酒精燃烧生成二氧化碳和水,反应的化学方程式为:
C2H5OH+3O2
烧杯中的棉芯自下而上熄灭,说明了CO2密度比空气密度大;
棉芯熄灭,说明了二氧化碳不能燃烧,也不能支持燃烧;
由质量守恒定律可知:
反应前后,原子种类、数目均不变,由反应的化学方程式,反应前碳、氢、氧原子个数分别为6、12、18,反应后的生成物中碳、氢、氧原子个数分别为0、0、12,根据反应前后原子种类、数目不变,则每个X分子由6个碳原子、12个氢原子和6个氧原子构成,则物质X的化学式为C6H12O6。
由质量守恒定律:
反应前后,原子种类、数目均不变,进行分析解答。
本题难度不大,掌握二氧化碳的化学性质与物理性质、化学反应前后原子守恒是正确解答本题的关键。
17.【答案】
(1)升华吸热;
(2)CO2+H2O=H2CO3;
(3)富氮空气
本题考查了物质的性质与用途,解题时根据干冰的性质与用途、氮气的性质与用途分析解答即可。
(1)干冰升华要吸收大量的热,常用来作制冷剂,干冰用于“温控保鲜”是利用干冰升华吸热的性质,故填:
升华吸热;
(2)CO2进入细菌细胞液后能产生酸性物质,是CO2和细胞液中的水反应生成了碳酸,故填:
CO2+H2O=H2CO3;
(3)氮气不供给细胞呼吸且氮气的化学性质稳定,常用于食品保鲜,故填:
富氮空气。
18.【答案】
(1)C+CO2
2CO;
C;
(2)棉球①、④均变红,④比①变红的快;
CO2与H2O反应;
(3)H2O+CO2=H2CO3;
H2CO3=H2O+CO2↑。
(1)根据高温条件下碳与二氧化碳反应生成了一氧化碳分析;
(2)根据二氧化碳能和水反应生成碳酸,碳酸显酸性,能使石蕊试液变红色解答;
(3)根据二氧化碳和水反应生成碳酸,碳酸不稳定生成二氧化碳和水书写化学方程式。
(1)将CO2通过灼热的碳层,在高温条件下碳与二氧化碳反应生成了一氧化碳该,反应的化学方程式为C+CO2
2CO,此反应CO2提供了氧,表现的化学性质是氧化性;
(2)通二氧化碳,用石蕊溶液染成紫色的干燥棉球②③都不变色,说明二氧化碳不能使石蕊变色,通二氧化碳,用紫色石蕊溶液润湿的棉球都变红,说明二氧化碳和水发生了化学反应,并且④比①先变红,说明二氧化碳的密度比空气的大,该实验还能研究的二氧化碳的性质是与水反应;
(3)将二氧化碳通入紫色石蕊试液中,溶液由紫色变为红色,是因为二氧化碳和水反应生成碳酸,化学方程式为H2O+CO2=H2CO3;
将溶液加热至沸腾,溶液由红色又变为紫色,是因为碳酸分解生成二氧化碳和水,化学方程式为H2CO3=H2O+CO2↑。
故答案为:
(1)C+CO2
19.【答案】
(1)长颈漏斗
(2)B;
稀盐酸;
CaCO3+2HCl=CaCl2+H2O+CO2↑;
b
(3)防止生成的二氧化碳从长颈漏斗逸出
(4)控制反应的发生与停止
(5)设200g稀硫酸中硫酸的质量为x,
Zn+H2SO4=ZnSO4+H2↑
98
2
x
0.4g
x=19.6g
所以原硫酸溶液中溶质的质量分数为
。
答:
原硫酸溶液中溶质的质量分数为9.8%。
本题主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写及计算和判断气体的性质等,综合性比较强。
(1)仪器a的名称是长颈漏斗;
故填:
长颈漏斗;
(2)实验室用大理石(或石灰石)与稀盐酸在常温下制取二氧化碳,同时生成氯化钙和水,所以发生装置选用B,从长颈漏斗中加入稀盐酸,反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;
由于二氧化碳的密度比空气大,所以用E装置收集二氧化碳,应长进短出,即气体从b端进入;
B;
b;
(3)长颈漏斗的下端要插入液面以下,是为了防止生成的二氧化碳从长颈漏斗逸出;
防止生成的二氧化碳从长颈漏斗逸出;
(4)C装置中有多孔隔板用来放块状固体,其优点是控制反应的发生与停止;
控制反应的发生与停止;
(5)设200g稀硫酸中硫酸的质量为x,根据化学方程式Zn+H2SO4=ZnSO4+H2↑计算出溶质的质量,然后由溶质质量分数公式进行计算即可。
20.【