考点16 盐文档格式.docx
《考点16 盐文档格式.docx》由会员分享,可在线阅读,更多相关《考点16 盐文档格式.docx(38页珍藏版)》请在冰点文库上搜索。
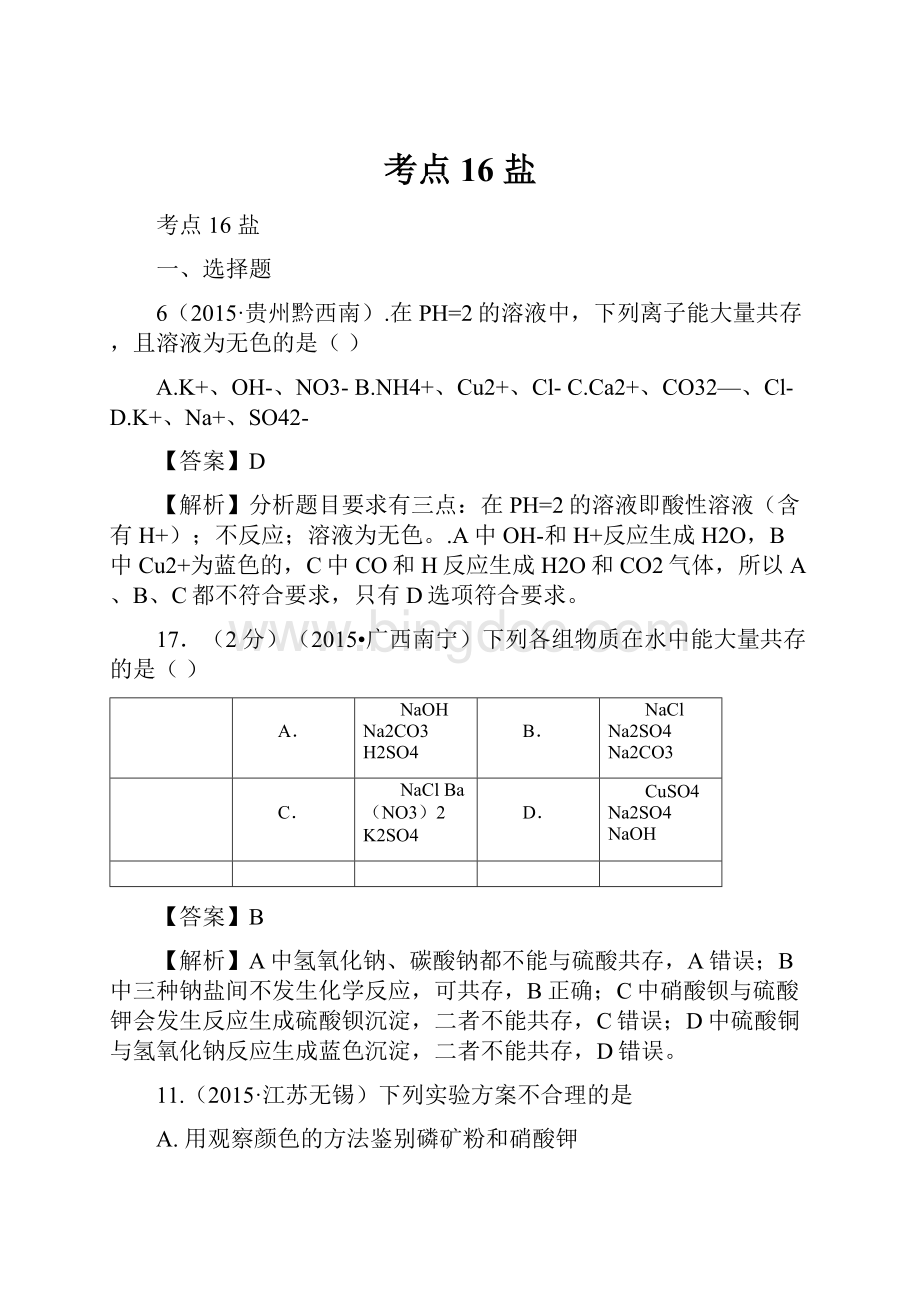
NH4N03、NaOH、NaCl溶于水温度分别是降温、升温和不变;
用FeSO4溶液、Cu和Ag,只能证明用Fe>
Cu,Fe>
Ag,无法比较Cu和Ag的活动性。
14.(2015•山东潍坊)今年世界卫生日的主题是从农场到餐桌,食品安全人人有责。
下列做法不会危害人体健康的是
A.用甲醛浸泡保存海产品B.用霉变的花生榨油
C.用工业用盐亚硝酸钠做调味品D.用含小苏打的发酵粉焙制糕点
【解析】不能用甲醛浸泡保存海产品,因为甲醛会与海产品中的蛋白质发生反应,破坏蛋白质的结构,使其变质,危害人体健康,可用甲醛水溶液制作动物标本,使标本能长久保存;
亚硝酸钠有毒,不能做调味品;
霉变的花生中含有黄曲霉毒素,不能用霉变的花生榨油。
7.(2015·
贵州毕节)生活中有许多盐,小苏打是其中一种,下列小苏打的化学式正确的是
A.Na2CO3B.NaHCO3C.NaClD.NaOH
【解析】小苏打是碳酸氢钠的俗称,所以小苏打的化学式为NaHCO3,碳酸钠的俗称是苏打,纯碱,氯化钠是食盐的主要成分,氢氧化钠是碱,其俗称是烧碱、火碱、苛性钠。
19.(2015·
山东枣庄)能在同一溶液中大量共存,且溶液为无色透明的一组物质是
A.FeCl3、CuSO4、NaCl
B.BaCl2、Na2SO4、NaOH
C.CaCl2、NaNO3、AgNO3
D.K2SO4、NaNO3、NH4Cl
【解析】题干提出两条限制条件:
一是能共存,即各物质间彼此不发生反应;
二是无色透明,即溶液中不能存在显色的物质。
A中各物质彼此不反应,但FeCl3显黄色,CuSO4显蓝色,不符合题意;
B中BaCl2与Na2SO4会发生反应生成BaSO4沉淀,不符合题意;
C中CaCl2与AgNO3会发生反应生成AgCl沉淀,不符合题意;
D中各物质间彼此不发生反应,且不存在显色物质,符合题意。
10、(2015·
湖北荆州)小明设计了下列四组物质,要求在一定条件下都能一步转化,其中错误的是()
A.Na2CO3→NaCl→NaNO3→NaOHB.C→CO→CO2→Na2CO3
C.Cu→CuO→CuSO4→Cu(OH)2D.CaCO3→CaO→Ca(OH)2→NaOH
【答案】A
【解析】碳酸钠与盐酸反应可生成氯化钠,氯化钠与硝酸银反应可生成硝酸钠,但硝酸钠无法与碱反应生成氢氧化钠,A错误;
碳在不完全燃烧时可生成一氧化碳,一氧化碳燃料时生成二氧化碳,二氧化碳与氢氧化钠反应时可生成碳酸钠,B正确;
铜在空气中加热可生成氧化铜,氧化铜与硫酸反应能生成硫酸铜,硫酸铜与碱溶液反应可生成氢氧化铜,C正确;
碳酸钙高温分解后可生成氧化钙,氧化钙与水反应生成氢氧化钙,氢氧化钙与碳酸钠反应时可生成氢氧化钠,D正确。
19.(2015•湖南郴州)下列各组离子在pH=1的溶液中能大量共存的是()
A.NH4+NO3-Na+Cl-B.CO32-K+Na+SO42-
C.Cu2+OH-Cl-Ba2+D.Ag+NO3-Cl-Na+
【解析】pH=1的溶液说明是酸性溶液
A.该组中的四种粒子之间不发生反应,也不与酸性物质发生反应,故可以大量共存;
B.该组中的四种粒子之间不发生反应,但是CO32-在酸性溶液中不能存在;
C.该组的四种粒子中的Cu2+与OH-会生成氢氧化铜沉淀,所以不能大量共存;
D.该组的四种粒子中的Ag+与Cl-会生成氯化银沉淀,所以不能大量共存;
所以,本题的选项为:
A。
10.(2015·
山东烟台)酸、碱、盐在工农业生产和日常生活中应用广泛。
下列做法错误的是()
A.用石灰乳与硫酸铜溶液配制农药波尔多液
B.用稀盐酸除去铁制品表面的铁锈
C.用食盐水除去水壶中的水垢
D.施用复合肥硝酸钾能使作物枝叶繁茂,并增加抗倒伏能力
【答案】C
【解析】氯化钠不与水垢的成分碳酸钙和氢氧化镁反应,因此不能出去该物质。
13.(2015•广东佛山)分别将下列各组物质同时加入到足量水中,最终能得到无色、透明溶液的是()
A.NaOHH2SO4BaCl2B.NaOHCuSO4NaCl
C.HNO3KNO3K2SO4D.Na2SO4FeCl3KCl
【解析】本题的关键在于最终得到无色透明的溶液,根据题意,结合选项可知,选项A中硫酸和氯化钡反应会生成硫酸钡沉淀;
选项B中氢氧化钠和硫酸铜反应生成蓝色的氢氧化铜沉淀;
选项C中三种物质彼此不反应,均易溶于水,也没有有颜色的离子,选项D三氯化铁溶于水会得到黄色溶液。
16、(2015·
湖北十堰)在某无色溶液中能大量共存的是()
A.Na+、Fe2+、NO3-、Cl-B.Na+、K+、NO3-、CO32-
C.Ba2+、K+、SO42-、Cl-DNH4+、K+、OH-、SO42-
【解析】由题干可知需要满足两个条件:
能在水中大量共存;
形成无色溶液。
B选项中各离子之间都不反应,B正确;
A选项中Fe2+在溶液中显浅绿色,不符合题意,A错误;
C.D选项分析如下:
Ba2+SO42-NH4+OH-
C.BaSO4
D.NH3·
H2OH2O+NH3↑
12.(2015•江苏连云港)三种物质间只通过一步反应就能实现如箭头所指方向的转化,下列符合要求的组合是()
A.①②B.①③C.②③D.①②③
【解析】碳酸钠与硫酸反应可一步直接到硫酸钠,硫酸钠可以与氢氧化钡反应生成氢氧化钠,氢氧化钠与二氧化碳可以反应生成碳酸钠,碳酸钠与氢氧化钡或氢氧化钙反应生成氢氧化钠;
氧化铜与酸反应可一步生成水,水通电分解生成氧气,氧气与氢气点燃生成水,氧气与铜在加热条件下生成氧化铜;
锌等金属与氯化亚铁、硫酸亚铁溶液反应,可以一步置换出金属铁,铁与硫酸或可溶性的硫酸铜溶液反应,可以一步生成硫酸亚铁,硫酸亚铁与氯化钡反应可一步生成氯化亚铁。
11.(2015·
浙江义乌)常温下,下列各组物质中,乙既能与甲反应又能与丙反应的是
选项
物质甲
物质乙
物质丙
A
HCl
Zn
AgCl
B
H2SO4
Fe2O3
NaCl
C
Ba(OH)2
Na2CO3
CaCl2
D
【解析】锌只能与氯化氢反应不能与氯化银(不溶于水)反应,A错;
氧化铁能够与硫酸反应不能与氯化钠反应,B错;
碳酸钠既能与氢氧化钡反应,又能够与氯化钙反应,C对;
氢氧化钡只能与硫酸反应不能与氯化钠反应,D错。
5.(2015•湖南益阳)2015年5月28日,广东省发布“输入性中东呼吸综合征”疑似病例后,许多中小学校为预防传染病的扩散,要求学生在饭前便后用84消毒液洗手。
84消毒液的主要成分是次氯酸钠(NaClO),则NaClO属于
A.氧化物B.酸C.碱D.盐
【解析】由两种元素组成的化合物中,如果其中有一种是氧元素,则该化合物又叫做氧化物;
解离生成的阳离子全部是氢离子的化合物叫做酸;
解离产生的阴离子全部是氢氧根离子的化合物叫做碱;
能解离出金属离子和酸根离子的化合物叫做盐。
由上分析可知次氯酸钠(NaClO)属于盐。
26.(2015•江苏苏州)下列离子能在pH=2的水溶液中大量共存的是
A.SO42-、NO3-、K+、OH-B.HCO3-、Cl-、SO42-、Na+
C.Cl-、NO3-、K+、Na+D.NH4+、Cl-、OH-、K+
【解析】pH=2的水溶液是酸性溶液,因此不可能含有、OH-、HCO3-故A、B、D不正确,因此选C。
6.(2015•江苏苏州)下列实验现象的叙述中,错误的是
A.氨气使湿润的蓝色石蕊试纸变红
B.细铁丝在氧气中剧烈燃烧,火星四射,放出热量,生成黑色固体
C.加热“铜绿”时,绿色固体变成黑色固体,管壁出现小水珠
D.向氯化钠溶液中滴加硝酸银溶液,生成白色沉淀
【解析】氨气是碱性气体,能使湿润的红色石蕊纸变蓝。
9.(2015•江西)某溶液中大量存在的离子仅有NH4+、Ca2+和X离子,则X可能是
A.OH-B.Cl-C.CO32-D.Na+
【解析】溶液是电中性的,即如果溶液中存在阳离子,同时也存在阴离子,根据题意,该溶液中已存在大量的钙离子和铵离子,这两种离子均为阳离子,所以X应该是阴离子,即D不正确;
铵离子与氢氧根离子不能大量共存,所以A不正确;
钙离子和铵离子都不与氯离子结合生成沉淀或气体,所以氯离子可与铵离子和钙离子大量共存,即B正确;
钙离子与碳酸根离子不能大量共存,所以C不正确。
13.(2015·
江苏南京)下列各组离子在水中能大量共存的是
A.Na+、H+、Cl-、HCO3-
B.Na+、K+、N03-、Cl-
C.H+、Na+、OH-、SO42-
D.Ag+、Ca2十、Cl-、NO3-
【答案】B
【解析】能大量共存,说明各离子彼此不发生反应。
A中H+与HCO3-会结合生成H2O和CO2,不能共存;
C中H+与OH-结合会生成H2O,不能共存;
D中Ag+与Cl-结合会生成AgCl沉淀,不能共存。
8.(2015•山东菏泽)下列各组离子可在同一溶液中大量共存的是()
A.H+SO42—K+CO32—B.Mg2+Cl—OH—Na+
C.Fe3+SO42—H+Cl—D.Na+Ba2+NO3—SO42—.
【解析】A中的氢离子和碳酸根离子可以结合成碳酸,二者不能共存;
B中的钠离子与氢氧根离子可以结合成氢氧化镁沉淀,故二者不能共存;
D中的钡离子与硫酸根离子可以结合成硫酸钡沉淀也不能共存。
29.(2015·
四川巴中)下列物质的转化中,只有加酸才能一步实现的是
A.CaCO3→CO2B.Zn→ZnSO4
C.CuO→CuCl2D.KOH→KCl
【解析】A.可以在高温条件下,CaCO3会分解生成CO2;
B.可以通过金属与酸或盐溶液的反应一步实现;
C.根据所学知识,CuO属于金属氧化物,只有通过与酸反应才能一步反应生成CuCl2;
D.可以通过与酸或盐的反应一步实现。
25.(2015·
四川巴中)下列各组离子在水中能大量共存的是
A.K+、Ca2+、NO3-、CO32-B.Na+、NO3-、K+、OH-
C.Na+、NH4+、OH-、Cl-D.Ba2+、H+、SO42-、NO3-
【解析】凡是在水溶液中能反应生成沉淀、气体或水的离子都不能共存,A中Ca2+和CO32-不能共存,C中NH4+和OH-不能共存,D中Ba2+和SO42-不能共存。
14、(2015·
四川成都)按下表进行实验,有关说法及分析错误的是
A、①有蓝色沉淀
B、②反应的化学方程式为:
CuSO4+BaCl2=BaSO4↓+CuCl2
C、两个反应都属于复分解反应
D、只要有沉淀生成的反应就属于复分解反应
【解析】氢氧化钠和硫酸铜能发生复分解反应,生成氢氧化铜蓝色沉淀,选项A正确;
氯化钡和硫酸铜反应生成硫酸钡沉淀和氯化铜,反应B的方程式符合反应事实,且遵循质量守恒定律,选项B正确;
这两个反应都是由两种化合物相互交换成分,生成另外两种化合物,都属于复分解反应;
选项C正确;
复分解反应的条件有三条,即生成气体、沉淀和水,三者居其一即可,但不是说只要有沉淀生成的反应就一定是复分解反应。
15.(2015·
浙江宁波)把盛有5g16%的NaOH溶液的短试管放入盛有l0g16%的CuS04溶液的锥形瓶里,如图所示。
倾斜锥形瓶直到使两溶液充分混合,混合后不可能的是
A.产生蓝色沉淀0.98g
B.锥形瓶内物质总质量不变
C.所得溶液的Na2S04质量分数大于9.5%
D.所得的Na2S04溶液质量与原CuS04溶液质量相等
【解析】根究反应方程式2NaOH+CuSO4==Na2SO4+Cu(OH)2↓中NaOH和CuSO4的质量比为1:
2,判断题目中NaOH和CuSO4恰好完全反应,生成的蓝色沉淀Cu(OH)2是0.98g,因此A正确;
化学反应前后质量守恒,而且没有气体产生,因此B正确;
反应后生成的Na2SO4是1.4g,1.4g/(5g+10g-0.98g)×
100%=9.9%>
9.5%,因此正确;
所得Na2S04溶液为5g+10g-0.98g=14.02g,而CuS04溶液的质量为10g,因此D不正确,综上D符合题意。
9.(2015·
浙江宁波)下列物质的用途只应用其物理性质的是
A.干冰在舞台制雾时作致冷剂
B.小苏打在做馒头时作发酵剂
C.还原铁粉在月饼盒内作除氧剂
D.生石灰在某些食品袋内作干燥剂
【解析】干冰升华吸热,是物理变化,表现的是物理性质,所以A正确;
小苏打在做馒头时是和发酵剂中的酸性物质反应,产生气体,因此是利用的化学性质,所以B不正确;
还原铁粉与氧气反应也发生化学变化,是铁的化学性质,所以C不正确;
生石灰做干燥剂是吸收水分,生成氢氧化钙,表现的是化学性质,所以D不正确,综上选A。
4(2015·
浙江杭州)Na2CO3的水溶液呈碱性,下列说法错误的是()
A.碳酸钠在水中会电离出OH-
B.往碳酸钠溶液中加稀硫酸后溶液的pH降低
C.碳酸钠溶液中存在OH-
D.往碳酸钠溶液中滴加紫色石蕊试液后溶液显蓝色
【解析】Na2CO3溶液呈碱性是因为碳酸根离子水解生成碳酸氢钠和氢氧化钠离子,其离子反应式CO32-+H2O
HCO3-+OH-而不是电离出OH-,故选A
重庆B卷)含有硫酸根离子的盐称为硫酸盐,下列物质属于硫酸盐的是()
A.H2SO4B.Na2SC.K2SO4D.SO2
【解析】上述四种物质,属于盐的是Na2S和K2SO4,H2SO4是酸,SO2是氧化物;
Na2S和K2SO4中含硫酸根的是K2SO4。
故选C
(2015·
山东泰安)16.氨碱法生产纯碱的主要反应原理如下:
(1)NaCl+NH3+CO2+H20=NaHCO3+NH4Cl
(2)2NaHCO3
Na2CO3+H2O+CO2↑。
对上述信息的有关理解不正确的是()
A.用食盐制纯碱需要含碳、氧元素的物质
B.
(1)中析出晶休后剩余溶液只有一种溶质
C.氨盐水比食盐水更易吸收二氧化碳D.碳酸氢钠比碳酸钠受热更易分解
【解析】
(1)中析出晶体后的溶液中会含有碳酸氢钠和氯化铵,B错误。
12.(2015•北京)能用于治疗胃酸过多症的物质是
A.蔗糖B.食盐
C.小苏打D.食醋
【解析】治疗胃酸过多要用碱性物质,以上物质中显碱性的只有小苏打。
小苏打质量胃酸过多发生反应的化学方程式为NaHCO3+HCl==NaCl+H2O+CO2↑。
12(2015·
宁夏)下列实验用品:
①pH试纸②无色酚酞溶液③紫色石蕊溶液④碳酸钠溶液,其中能将稀硫酸、氯化钠溶液和澄清石灰水鉴别出来的是( )
A.①②③ B.①③④ C.②③④ D.①②④
【解析】稀硫酸的pH小于7,氯化钠溶液的pH等于7,澄清石灰水的pH大于7,故pH试纸可以鉴别三种物质;
紫色石蕊溶液遇到稀硫酸会变红,遇到氯化钠溶液不变色,遇到澄清石灰水变成蓝色,故可以鉴别三种物质;
碳酸钠溶液与稀硫酸反应会产生气体,碳酸钠溶液与氯化钠溶液不反应,碳酸钠溶液和澄清石灰水反应会产生白色沉淀,故可以鉴别三种物质;
而无色酚酞遇到稀硫酸、氯化钠溶液均为无色,故无法鉴别。
故本题的正确答案为:
B。
5.(2015·
宁夏)食盐是重要的调味品,精盐是由粗盐提纯而来,在提纯过程中通常不需要的操作是( )
A.吸附 B.蒸发 C.过滤 D.溶解
【解析】将粗盐提纯为精盐,首先要将粗盐样品溶解在水中,然后用过滤的操作除去粗盐中的难溶性杂质,滤液为较纯净的氯化钠溶液,要得到固体氯化钠还要进行蒸发结晶的操作,因此提纯过程中不需要进行吸附操作。
故本题的选项为A。
8.(2015•贵州铜仁)下列反应不能一步实现的是( )
Zn→ZnSO4
Fe2O3→FeCl3
BaCl2→Ba(OH)2
CH4→H2O
【解析】A中可加入稀硫酸实现,其反应为Zn+H2SO4=ZnSO4+H2↑,B中可加入稀盐酸,其反应为Fe2O3+6HCl=2FeCl3+3H2O;
D中甲烷燃烧可生成水;
C中加入一种物质不能实现它们的转化,故答案选C。
10.(2015•吉林)用同一种基本反应类型,经过两步反应不能实现的转化是( )
A.C→H2CO3B.Cu→Cu(OH)2C.H2O2→H2D.NaOH→BaSO4
【答案】B【解析】A中C和氧气发生化合反应生成CO2,CO2与水发生化合反应生成H2CO3,正确;
B中Cu和AgNO3发生置换反应生成Cu(NO3)2,Cu(NO3)2和NaOH发生复分解反应生成Cu(OH)2,错误;
C中H2O2发生分解反应生成H2O,H2O分解生成氢气,正确;
D中NaOH和H2SO4发生复分解反应生成Na2SO4,Na2SO4与BaCl2发生复分解反应生成BaSO4,正确。
12、(2013•河南)现有10.6g碳酸钠和8.4g碳酸氢钠,分别与过量盐酸反应,其中【】
A:
碳酸钠消耗的氯化氢多B:
碳酸钠生成的二氧化碳多
C:
碳酸氢钠消耗的氯化氢多D:
碳酸氢钠生成的二氧化碳多
【解析】碳酸钠和盐酸完全反应时,消耗碳酸钠和盐酸以及生成二氧化碳的质量比为106:
73:
44;
而碳酸氢钠和盐酸完全反应时,消耗碳酸氢钠和盐酸以及生成二氧化碳的质量比为84:
36.5:
44,从数据上看并结合题意可知,碳酸钠消耗的盐酸质量大于碳酸氢钠,而二者所生成的二氧化碳的质量是相等的。
(2015年贵州遵义)7.下列离子在水溶液中无色且能大量共存的一组是
A.Ca2+、K+、Cl-、NO3-B.Na+、Cu2+、NO3-、SO42-
C.Fe3+、Na+、OH-、NO3-D.K+、H+、SO42-、CO32-
【解析】四种离子在水溶液中都无色,四种离子间不会结合成沉淀或水或气体,A正确;
铜离子在水溶液中显蓝色,B不正确;
铁离子能与氢氧根离子结合生成沉淀,所以C不正确;
氢离子能与碳酸根离子结合生成水和二氧化碳,所以D不正确。
二、填空、简答题
23.(2015•北京)(1分)她来到博物馆门口。
同学们在地质学家李四光的大理石雕像前,了解他的生平事迹。
大理石的主要成分是_____________。
【答案】碳酸钙
【解析】大理石、大理石、贝壳、蛋壳和水垢等的主要成分都是碳酸钙。
20.(2015·
陕西)工业上用纯碱和石灰石为原料制备烧碱的简要工艺流程如下图所示,请回答。
(1)石灰石、生石灰、熟石灰均能与下列(填字母)发生化学反应。
A.水B.盐酸C.二氧化碳
(2)步骤④发生反应的化学方程式是。
(3)某研究性学习小组的同学想检验上述工艺中的烧碱溶液里是否含有纯碱,甲同学选择了一种酸溶液,乙同学选择了一种碱溶液,丙同学也选择了一种溶液,该溶液中溶质与甲、乙同学所用溶液中溶质的物质类别不同,他们都能达到检验目的。
你认为丙同学所选溶液中的溶质可能是(填一种物质的化学式)。
【答案】
(1)B
(2)Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
(3)CaCl2或Ca(NO3)2或BaCl2或Ba(NO3)2
(1)能与盐、金属氧化物、碱能发生化学反应的物质是酸,所以选B;
(2)石灰水中的溶质是氢氧化钙,纯碱溶液的溶质是碳酸钠,所以反应的化学方程式是:
Ca(OH)2+Na2CO3===CaCO3↓+2NaOH;
(3)检验烧碱溶液中是否含有纯碱,就是检验溶液中是否含有碳酸根离子,因此从复分解反应发生的条件进行考虑,可以加酸或加入含有钙离子或钡离子的化合物的溶液,因此丙同学所选溶液中的溶质可能是CaCl2或Ca(NO3)2或BaCl2或Ba(NO3)2。
15.(2015•山东威海)用科学方法认识和改造物质
只有正确认识了物质,才能合理改造和应用物质.请你运用归纳/演绎、实验、比较/对比等科学方法认识氯化钠.
(1)用归纳演绎法认识氯化钠的性质
已知下列反应:
HCl+AgNO3=AgCl↓+HNO3MgCl2+2AgNO3=2AgCl↓+Mg(NO3)2
①上述反应属于四种基本反应类型中的,运用(填“归纳”或“演绎”)法得到这组反应发生的原因是.
②由①中得到的规律可以推测“氯化钠溶液也能跟硝酸银溶液反应”,运用的是(填“归纳”或“演绎”)法.
(2)用实验法认识氯化钠的性质
①要验证
(1)②中“氯化钠溶液也能跟硝酸银溶液反应”的推断,需要进行实验,实验方法是,反应的化学方程式是.
②有实验法认识氯化钠溶液的酸碱性,其实验方法是.
比较是为了找出事物的相同点,对比是为了找出事物的不同点.
图为氯化钠和硝酸钾溶解度曲线,通过比较/对比可以发现二者的相同点有(选字母编号,下同),不同点有.
A.易溶物质
B.溶解度随温度变化的方向
C.溶解度受温度影响的程度
D.20℃时的饱和溶液溶质质量分数
E.23℃时的溶解度
F.40℃100g饱和溶液降温到20℃析出晶体的质量
(4)用两种重要的实验法﹣﹣“蒸馏法和结晶法”改造物质
从古希腊炼金士到今天的化学工作者,都用了两种重要的实验法﹣﹣蒸馏法和结晶法.证明氯化钠溶于水没有新物质生