中考科学专题复习三种还原剂还原氧化铜Word下载.docx
《中考科学专题复习三种还原剂还原氧化铜Word下载.docx》由会员分享,可在线阅读,更多相关《中考科学专题复习三种还原剂还原氧化铜Word下载.docx(16页珍藏版)》请在冰点文库上搜索。
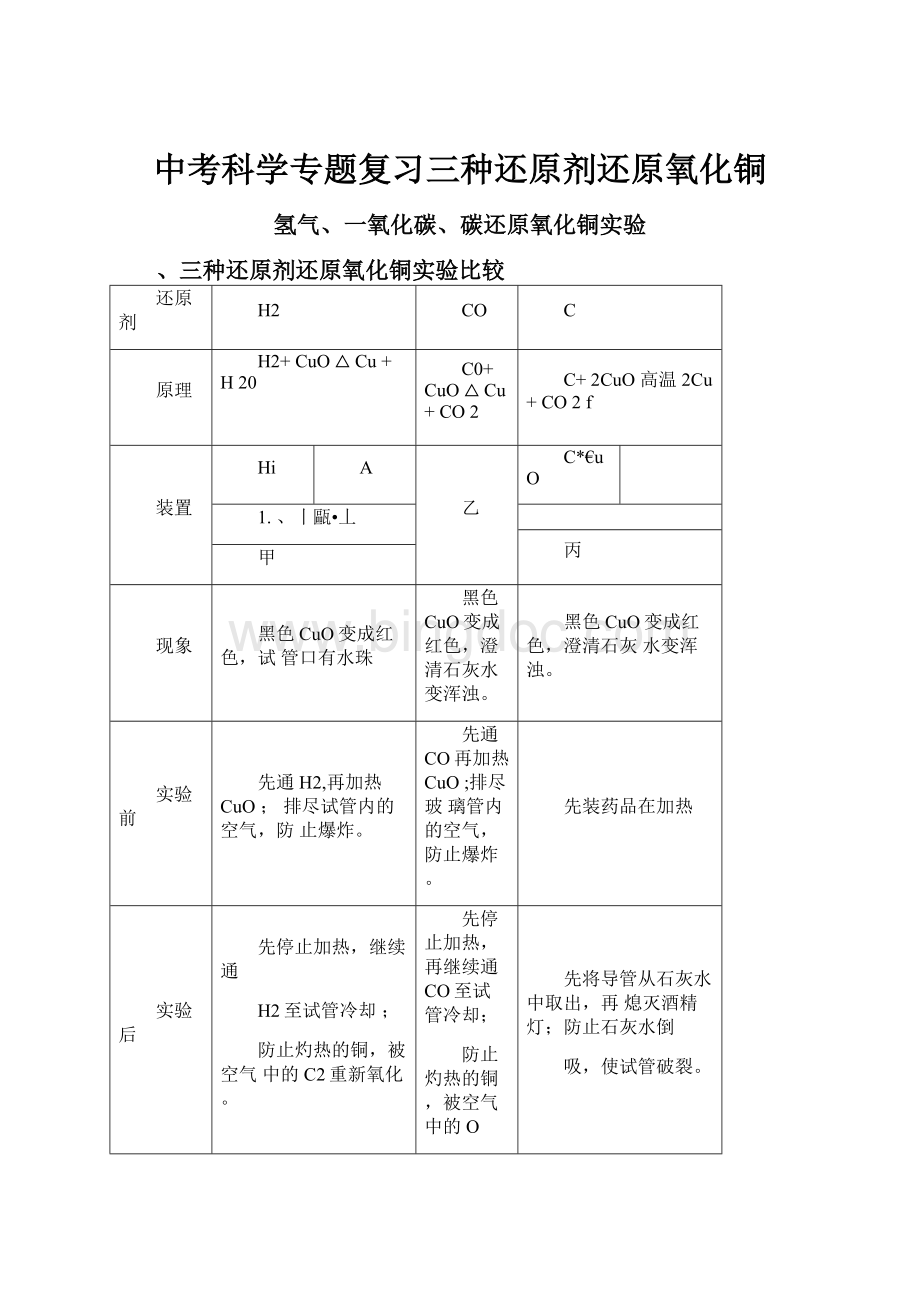
H2至试管冷却;
防止灼热的铜,被空气中的C2重新氧化。
先停止加热,再继续通CO至试管冷却;
防止灼热的铜,被空气中的O
重新氧化,还可以防止液体倒吸
先将导管从石灰水中取出,再熄灭酒精灯;
防止石灰水倒
吸,使试管破裂。
注意
事项
1•试管口略向下倾斜,防止小水珠倒流,使试管破裂。
2.导管通到试管底部,有利于排尽试管内空气,有利于H2与氧化
尾气处理,后面的酒精灯先点燃,后熄灭。
固固加热型,试管口应略向下倾斜。
铜充分接触
相同点
三个装置都要加热
不同点
1.乙、丙装置中,澄清石灰水的作用都是检验反应产物CQ。
2.甲、丙装置中,试管口都略向下倾斜;
试管口的区别是甲不能用橡皮塞,丙有橡皮塞
3.乙装置有尾气处理装置。
(原因:
CC有毒;
处理方法:
燃烧法、气囊收集法)
二、经典题型训练
1•一氧化碳还原氧化铜实验的过程中有如下几步操作:
①点燃酒精灯,加热氧化铜;
②撤去酒精灯,停
止加热;
③通入一氧化碳气体;
④停止通入一氧化碳气体;
⑤让还原出的金属铜完全冷却。
其中
正确操作的顺序为(
)
A.①③②④⑤B.
③①②⑤④C.③①②④⑤D.①③②⑤④
2.用一氧化碳还原氧化铜后
A.温度太低
,发现已制得的铜又很快变黑了,请推测产生这种现象的原因可能是()
B.试管口倾斜了
C.反应开始时,没有把试管内的空气排干净
D.铜没有在一氧化碳气流中冷却而又被空气中的氧气所氧化
3•氢气和一氧化碳还原氧化铜的实验装置如下,有关说法错误的是()
A.实验时都应该先通入气体后加热,防止发生爆炸
B.两者都可以通过观察黑色固体颜色的变化判断反应是否发生
C.甲试管略向下倾斜,乙玻璃管保持水平,是因为两种气体的密度不同
D.甲无尾气处理装置而乙有,是因为一氧化碳有毒而氢气无毒
4•木炭还原氧化铜和一氧化碳还原氧化铜的实验装置如下,下列说法正确的是()
6•氢气、木炭、一氧化碳是金属冶炼中常用的还原剂•如图甲是氢气还原氧化铜的实验,如图乙是木炭还原氧化铁的实验,如图丙是一氧化碳还原氧化铜的实验.
(1)实验装置的设计应考虑反应物、生成物的性质和反应条件等因素。
比较图甲和图丙所示的实验装置,从反应物的角度分析它们的不同点,写出一点并说明原因
(2)实验步骤的先后次序很重要,如甲实验中反应前须先通氢气后点灯,否则易发生爆炸;
请再列
出二项不能颠倒的先后次序:
甲实验中反应后必须,否则生成的红色
的铜会变成黑色;
丙实验中反应前必须,否则易发生煤气中毒.
(3)某同学正确操作做完乙实验后,发现澄清石灰水变浑浊,试管中粉末全部变为黑色,用另一试管取5克黑色残留粉末,加入足量稀硫酸充分振荡,她惊讶地发现试管中并未产生预期的气泡,她向老师求教,才知道铁的氧化物除了氧化铁和四氧化三铁外还有氧化亚铁(也为黑色),其中只有四氧化三铁常温下不溶于稀硫酸”,于是她又对试管中的悬浊液进行过滤和烘干操作,滤液无色澄清,滤渣经称量后仍为5克.请你据此写出乙实验试管中发生的化学方程式.
(4)到底是什么原因导致乙实验的冶炼效果不理想呢?
该同学先经过科学猜想,后用酒精喷灯代替
普通酒精灯重做这个实验来加以验证,结果证明她的猜想是正确的•由此推断,该同学的科学猜想是•
7•某化学兴趣小组同学对木炭还原氧化铜的实验进行了一系列的探究及分析
润化纸
C+CW
S灰澄石水
高温
澄清的
甲乙
C'
CuO
(1)点燃酒精灯,数分钟后发现图1甲装置的试管中出现的现象是
乙试管中发生反应的化学方程式为:
.
实验完毕,应先将导管移离液面,再熄灭酒精灯,其原因
并用弹簧夹夹紧橡皮管,其原因又是_
(2)C+2Cu8:
=2CU+CQT,C将CuO还原成Cu,故C作还原剂.
1先分析,再归纳:
反应前后,还原剂化合价的变化规律是
2根据你所得的规律,判断Zn+H2SQ—ZnSO4+H2仁还原剂是
B
郵
猜想n:
除铜外,还含有木炭
猜想川:
猜想w:
皿6
请在如图4所示框中简要写出计算过程
【问题讨论】
1D装置的作用是.
2在实验步骤b、c中洗连接A、B装置加入H2O2溶液后连接CD加热B装置的目的是
3在实验步骤d中,停止加热,继续加入H2O2溶液目的是.
4实验完成后,教师评议说:
按上述实验设计,即使B装置中反应完全,C装置吸收完全,也不会得出正确
结果•经讨论,有同学提出在之间(填两个装置的代号)加入一装置,就能得到较准确结
果,该装置的作用是,请你判断原测得结果
将(填偏大”不变”偏小”).
8•甲、乙两研究性小组在实验室分别用如图I和图II所示的实验装置做木炭还原氧化铜的实验•
(1)甲组的实验装置中酒精灯加网罩的目的是,与装置I相比,装置II的优点
是.
(2)甲组的同学想探究木炭还原氧化铜所生成的气体产物是什么?
他们提出了两个猜想,气体产物可
能是二氧化碳也可能是一氧化碳,乙组的同学认为甲组同学的猜想不够严谨,气体产物还可能
是
甲组同学用图I所示装置进行他们的实验探究,若产生的气体中有一氧化碳,则会造成空气污染,你认为他们设计的实验装置还存在的缺陷是.
(3)若W形管中的C和CuO在高温条件下充分反应,乙小组的同学对充分反应后W形管中的固体
成分有探究热情,他们提出了三个猜想:
①该固体全部是铜;
②该固体是铜和氧化铜两种物质的混合物③该固体是铜与木炭的两种物质的混合物;
④该固体是铜、木炭和氧化铜三种物质的混合物,你认
为上述猜想中明显不成立的是哪个,原因是•
9•小金利用图示装置进行甲、乙对比实验,探究温度对CO和Fe2O3反应的影响(固定装置略)。
(1)从实验安全角度考虑,图示装置还应采取的改进措施是
(2)完全反应后,两组的生成物均为黑色粉末(纯净物),分别用两组生成物进行以下实验:
歩?
S
操作
甲绢现象
乙绡现象
1
称量黑色粉末质量电
mi
2
取黑色粉末,用磁铁吸引
能披吸弓1
能被吸引
3
収黒色粉末,加入稀盐釀
全部溶解:
有大量气泡
无明显现象
4
取黑色耕末』扣入足量6E5溶港
有红色物厉供产
1甲组的黑色粉末与稀盐酸反应的化学方程式是。
2小金查阅资料后发现Fe3O4在常温下不与稀盐酸、CuSQ溶液反应,故猜想乙组的生成物为Fe3O4。
他又发现m2恰好为g,这可成为支持上述猜想的新证据。
10.为探究碳还原氧化铜的最佳实验条件,用木炭粉和氧化铜的干燥混合物1~2.5g进行系列实验。
〖查阅资料〗①氧化铜(CuO)为黑色固体。
②碳还原氧化铜得到的铜中可能含有少量的氧化亚铜;
氧化亚铜为红色固体,
〖进行实验〗实验1:
取质量比1:
11的木炭粉和氧化铜混合物1.3g,进行实验。
序号1—11—2
实验2:
取一定量的混合物,用1—2装置进行实验。
序号
木炭粉与氧化铜的质量比
反应后物质的颜色、状态
2—1
1:
9
红色固体有金
属光泽
混有少量黑色物质
2—2
10
混有很少量黑色物质
2—3
11
混有极少量黑色物质
2—4
12
无黑色物质
2—5
13
混有较多黑色物质
1解释与结论〗
(1)写出反应的化学方程式:
,这个反应中CuO是剂。
(2)实验1—2中,证明此产生了CO2的现象是,
(3)实验1的目的是。
(4)实验2的结论是:
。
1反思与评价〗
(5)有同学建议用超细炭粉与氧化铜粉末进行实验,你认为这样建议的理由是
(6)实验2未进行质量比为1:
14的实验,理由是
11.利用化学变化可以制备新物质,CO是一种无色、无臭的气体,密度比空气略小,难溶于水,易
于血红蛋白结合,具有可燃性•请结合所学知识和CO的相关信息回答下列问题:
(1)下列两个反应都能生成CO,从实验室制备气体的思路分析,实验室制备CO选择反应②而不
用①的理由是(任选一个角度回答)
咼温
①炽热的焦炭和水蒸气反应:
C+HO====CO+H
浓H2SO4
②草酸晶体和浓硫酸供热:
H2C2O4======CQ1+C0F+H20
△
(2)
某同学设计下列装置制备、提纯CO,并用CO来还原氧化铜•请根据如图回答:
(3)①写出一氧化碳还原氧化铁的化学反应方程式
2该同学的设计存在的一处明显缺陷是•
用改进后装置进行实验,在点燃E处酒精灯之前,必须进行的一项操作是
(从实验安全角度考虑).
3装置B的作用是,B中发生反应的化学方程式为
4证明一氧化碳能还原氧化铁的实验现象是:
装置E中固体颜色的变化为
C中,F中④在此实验中,我们还认识到CO和CO2的化学性质有许多的不同•试从微观的角度分析CO和CQ化
学性质不同的原因是
12.化学小组根据氨气还原氧化铜的反应,设计实验测定Cu元素的相对原子质量•
2XH,O1Ca(QH)2CaCL+2NH;
+2Hj()
已知:
①一f②氨气是碱性气体请结合下图回答问题
(1)将纯净干燥的氨气通入B中,观察到玻璃管内黑色固体变为亮红色,管口有液滴侗时生成空气中
含量最多的气体,写出B中发生反应的化学方程式为
(2)测定Cu元素相对原子质量的实验过程为:
先称量CuO的质量,完全反应后测定生成水的质量,由
此计算出Cu元素的相对原子质量•
I.小组同学利用上图进行实验,装置连接的合理顺序是(填序号,装置可重复使用)
n•在本实验中,使测定结果偏大的原因可能是(填序号);
③CuO中混有不反应的杂质川•在本实验中,还通过测定
①CuO未完全起反应②CuO不干燥
④NH4CI与Ca(OH)2混合物不干燥
的质量达到实验目的
13•某化学兴趣小组为了验证甲烷与水蒸气经高温催化反应得到的混合气体(以下简称“合成气”)中含有生成的氢气和一氧化碳,同时检验“合成气”中是否含有未反应完的甲烷和水蒸气,进行了如图所示的实验。
查阅资料知,氧化铁与氢气在高温条件下反应生成铁和水;
氧化铁与甲烷在高温条件下反应生成铁、
二氧化碳和水。
(1)请写出甲烷与水蒸气在高温催化条件下反应的化学方程式。
(2)实验开始前要先通一会“合成气”,然后再点燃B处的酒精喷灯,目的是。
(3)装置C和D的连接顺序颠倒,会影响实验操作,原因是。
(4)实验结束后,测得装置A、C、D的质量均增加,其中装置C增加了3.6g,装置D增加了3.3g。
假设加热时“合成气”在装置B中反应完全,则可推断出该“合成气”的组成物质为
(写化学式)。
(5)装置A与E在实验过程中的作用分别是
6.
(1)甲装置敞口,乙装置密闭(甲装置不用尾气处理,乙装置要点燃尾气),
原因是H2无毒,CO有毒
(2)先熄酒精灯,继续通氢气至试管冷却
,3)——
(3)
先点尾灯,后通CO
(4)加热的温度不够高
7.
(1)黑色固体变成红色固体
防止液体倒流炸裂试管
止氧气进入试管把铜氧化
(2)①升高②Zn
【实验反思】①没有处理尾气
CuD+CCu+COT咸CO^+C2C0.
②
猜想川:
除铜外,还含有氧化铜猜想W:
除铜外,还含有木炭和氧化铜
【数据计算】94%
【问题讨论】①防止空气中的水蒸气和二氧化碳进入C中.
②利用产生的氧气把反应生成的二氧化碳全部排入C中.
④A、B吸收水蒸气;
偏小.
8•聚拢火焰,提高温度操作简单,节约药品一氧化碳和二氧化碳没有处理尾气装置
④,高温条件下,氧化铜和木炭不能共存
9.
(1)在装置末端尖嘴导管处,放置一盏燃着的酒精灯(合理即可)
(2)①/c+2HCI=FcCh+Hj/upftrrvu(没配平扣1分);
②4.64
(3)还原性和可燃性(写出还原性即可)
10.
(1)C+2Cud=2Cu+CO2f氧化剂
(2)澄清石灰水变浑浊。
(3)探究氧化铜与木炭的受热面积对其反应的影响。
(4)木炭与氧化铜反应的最佳质量比为1:
12时恰好完全反应
(5)超细炭粉与氧化铜接触面积大,反应更充分
(6)木炭与氧化铜的质量比为1:
13时,氧化铜就已经过量了,所以没有必要进行1:
14的实验11.
【答案】
(1)对比反应①、②的条件,反应①的温度更高
没有变浑浊;
澄清的石灰水变浑浊
CO2
CO和的化学性质不同的原因是二者的分子构成不同,故填:
分子构成不同
(1)3EO+axilt:
心+N.43HJ)
12.
⑵I•③;
U.①③;
ni.cuo和Cu.
13.
(1}+H>
O璽空"
3H2+CO
(2)排净玻璃管中的空气,防止高温时引起嫁炸
(3)不能准确地测出生成水的质量
(4)co,%「%H2()
(5)除去水蒸气;
收集尾气r防止污染空邑