精品化学苏教必修2讲义专题1 微观结构与物质的多样性 第2单元 第2课时Word文档下载推荐.docx
《精品化学苏教必修2讲义专题1 微观结构与物质的多样性 第2单元 第2课时Word文档下载推荐.docx》由会员分享,可在线阅读,更多相关《精品化学苏教必修2讲义专题1 微观结构与物质的多样性 第2单元 第2课时Word文档下载推荐.docx(18页珍藏版)》请在冰点文库上搜索。
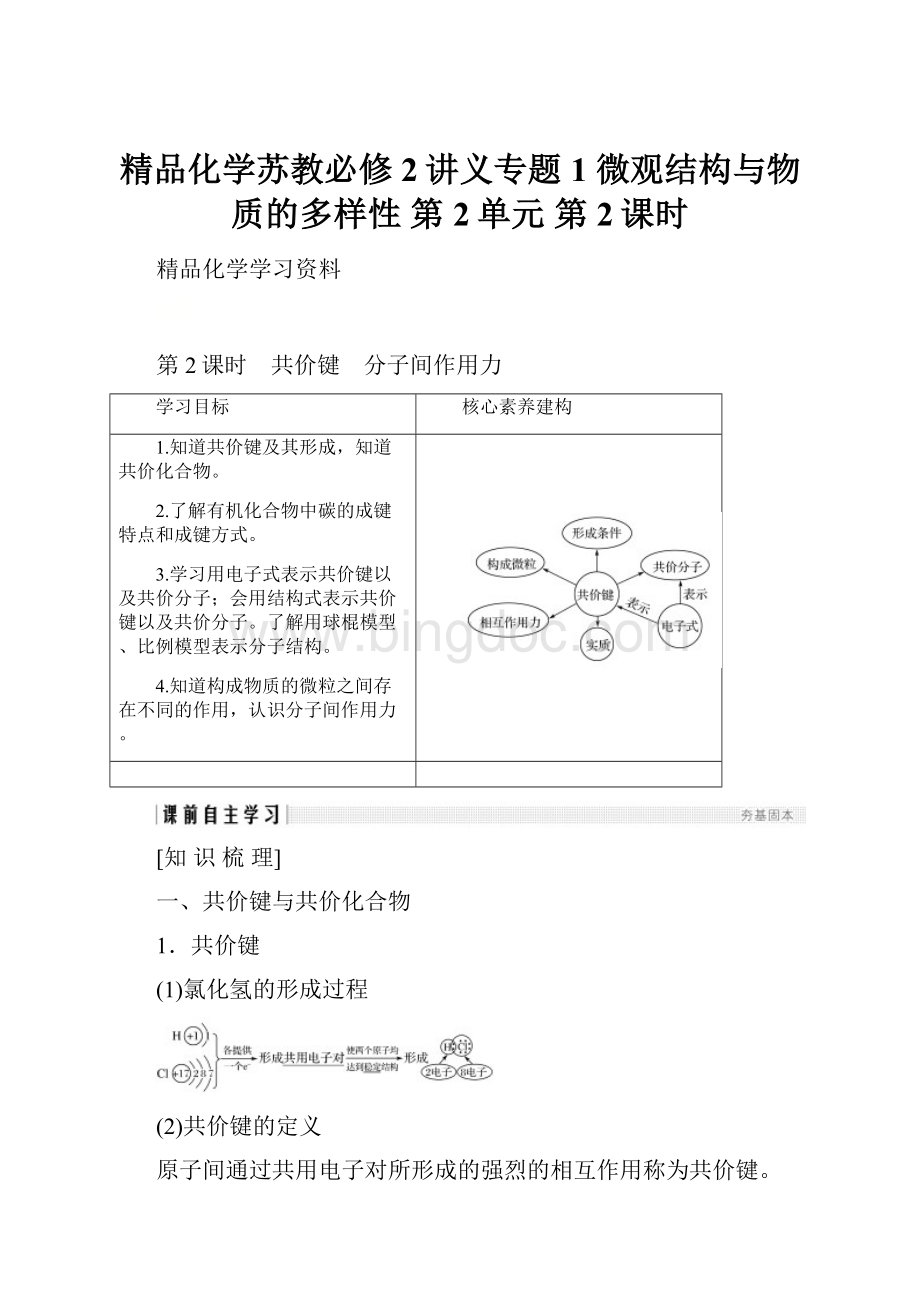
H2O
NH3
CH4
电子式
结构式
H—Cl
Cl—Cl
H—O—H
球棍模型
比例模型
【自主思考】
1.常见什么样的元素原子之间能形成共价键?
所有的非金属单质中都含有共价键吗?
提示
(1)同种或不同种非金属元素的原子之间能形成共价键。
(2)不正确,绝大多数非金属单质中存在共价键,但是稀有气体等单质分子内无化学键。
2.原子间通过共用电子对达到了稳定的电子层结构,怎样理解稳定结构?
提示 在共价分子中,各原子最外层都达到了最多能容纳的电子数,一般最外层达到8电子(当第1层为最外层时达到2个电子)稳定结构。
3.含有共价键的化合物一定是共价化合物吗?
提示 不对,含有共价键的化合物不一定是共价化合物,如NaOH中存在离子键和共价键,但是NaOH为离子化合物,还有非金属单质中可能含有共价键,但不属于化合物。
二、分子间作用力
1.分子间作用力
分子间存在着将分子聚集在一起的作用力,这种作用力称为分子间作用力,亦可称为范德华力。
(2)特征
①分子间作用力比化学键弱(填“强”或“弱”)得多。
②存在于分子之间,且分子充分接近时才有相互间的作用力,如固体和液体物质中。
③分子间作用力主要影响由分子构成物质的熔沸点、溶解度等物理性质,而化学键主要影响物质的化学性质。
如水从液态转化为气态只需要克服分子间作用力,而水分解需要破坏化学键。
2.氢键
(1)像H2O、NH3、HF这样的分子之间存在着一种比分子间作用力稍强的相互作用,这种相互作用叫氢键。
(2)氢键不是化学键,通常把氢键看作是一种较强的分子间作用力。
氢键比化学键弱,比分子间作用力强。
(3)分子间形成的氢键会使物质的熔点和沸点升高,对物质的溶解度有影响,如NH3极易溶于水,主要是氨分子与水分子之间易形成氢键。
4.举例说明有哪些事实可以证明分子间作用力的存在?
提示 干冰升华、硫晶体熔化、液氯汽化要吸收能量,说明干冰晶体内CO2分子之间、硫晶体内硫分子间、液氯中Cl2分子间存在着相互作用。
5.“氢键是一种化学键”对吗?
提示 氢键是一种特殊的分子间作用力,不是化学键。
6.水哪些特殊的物理性质与氢键有关?
提示
(1)沸点较高:
水分子间的氢键使水分子间作用力增强,因此水有较高的沸点。
(2)水结成冰密度变小:
在冰晶体中,水分子间形成的氢键比液态水中形成的氢键多,水分子间所形成的氢键使冰的微观结构里存在较大的空隙,因此,相同温度下冰的密度比水小。
(3)水的比热容较大。
[效果自测]
1.判断
(1)HCl分子中有一对共用电子对。
( )
(2)原子间以共用电子对形成的物质是共价化合物。
( )
(3)共价化合物中一定只含有共价键。
(4)共价键只存在于共价化合物中。
(5)共价化合物中一定不含有离子键。
(6)含有共价键的化合物一定是共价化合物。
(7)N2的电子式为N⋮⋮N。
答案
(1)√
(2)×
(3)√ (4)×
(5)√ (6)√ (7)×
2.下列说法中不正确的是( )
A.氢键是一种较弱的化学键
B.氢键可看作是一种较强的分子间作用力
C.分子间作用力只影响物质的物理性质
D.化学键能影响物质的物理性质和化学性质
答案 A
探究一、离子化合物与共价化合物的比较
【合作交流】
1.离子化合物与共价化合物有哪些不同?
(1)它们的构成粒子不同
提示 离子化合物的构成粒子是阴、阳离子。
共价化合物的构成粒子是原子。
(2)所含化学键类型不同
提示 离子化合物一定含有离子键,可能含有共价键。
共价化合物一定含有极性共价键,可能含有非极性共价键,一定不含有离子键。
(3)所含物质类别不同
提示 离子化合物有强碱、大多数盐、活泼金属氧化物、金属氢化物等。
共价化合物有酸、非金属氧化物、非金属氢化物、有机物等。
(4)主要物理特性不同
提示 离子化合物常温下为固体,熔点、沸点较高,熔融或溶于水能导电。
绝大多数共价化合物的熔点、沸点较低,熔融状态不能导电。
(5)用电子式表示方法不同
①写出下列共价化合物的电子式
CO2____________,H2O____________
②写出下列离子化合物的电子式
NaOH____________,Na2O2____________
【点拨提升】
1.离子键与共价键的比较
离子键
共价键
概念
阴、阳离子间通过静电作用所形成的化学键
原子间通过共用电子对所形成的化学键
成键微粒
阴、阳离子
原子
成键元素
活泼金属元素和活泼非金属元素(铵盐除外)
大多数为非金属元素
成键实质
阴、阳离子间的静电作用
共用电子对对两原子核产生的电性作用
形成过程
NaCl的形成过程如下:
HCl的形成过程如下:
H×
+
―→
存在范围
活泼金属氧化物、强碱、大多数盐
多数非金属单质、共价化合物及部分离子化合物
实例
CaCl2、Na2O2、NaOH
Cl2、CCl4、NaHCO3
2.离子化合物与共价化合物的比较
离子化合物
共价化合物
构成微粒
分子或原子
微粒间的作用
原子之间存在共价键
熔沸点
较高
一般较低,少部分很高(如SiO2)
导电性
熔融态或水溶液导电
熔融态不导电,溶于水有的导电(如硫酸),有的不导电(如蔗糖)
熔化时破坏的作用力
一定破坏离子键,可能破坏共价键(如NaHCO3)
一般不破坏共价键,极少部分破坏共价键(如SiO2)
强碱、大多数盐、活泼金属的氧化物
酸、非金属氢化物、非金属氧化物
3.判断离子化合物和共价化合物的方法
(1)由化学键类型判断
只含有共价键的化合物是共价化合物,只含离子键或既含离子键又含共价键的化合物是离子化合物。
(2)由化合物类型判断
①活泼金属的氧化物(过氧化物和氢化物)、强碱和大多数盐(少数盐如AlCl3、BeCl2等除外)属于离子化合物;
②非金属氧化物、非金属氢化物、含氧酸、多数有机物、少数盐(如AlCl3、BeCl2)属于共价化合物。
(3)由组成元素判断
一般含金属元素或NH
的化合物是离子化合物(AlCl3、BeCl2等少数除外),如NH4H、NH4HCO3、Ca(OH)2、KClO3等;
只由非金属元素构成的化合物(铵盐等除外)属于共价化合物。
【典题例证1】 下列物质中属于含共价键的离子化合物的是( )
A.H2SB.NH4NO3
C.K2SD.MgCl2
解析 H2S中含有两个H—S共价键;
NH4NO3中NH
与NO
之间以离子键结合,其中NH
中N与H原子之间及NO
中N与O原子之间都是以共价键结合;
K2S中两个K+分别与S2-以离子键结合;
MgCl2中Mg2+与两个Cl-分别以离子键结合。
H2S是共价化合物,NH4NO3、K2S、MgCl2是离子化合物。
答案 B
知识归纳 既含离子键,又含共价键的物质有活泼金属过氧化物、铵盐、含氧酸盐、强碱。
【学以致用1】 下列有关化学键的叙述正确的是( )
A.离子化合物中一定有离子键
B.含有共价键的化合物一定是共价化合物
C.非金属元素组成的化合物中只含共价键
D.单质分子中都存在化学键
解析 A正确,离子化合物的定义就是含有离子键的化合物;
B不正确,只含有共价键的化合物,才是共价化合物;
C不正确,非金属元素组成的化合物中也可能既含共价键,又含离子键,如NH4Cl中NH
与Cl-之间以离子键结合,N与H之间以共价键结合;
D不正确,除稀有气体外的非金属单质中都含有共价键,如H2、O2等。
探究二、化学键与分子间作用力
2.水很容易变成水蒸气,而水分解则需在电解的条件下才能进行,为什么?
提示 水变成水蒸气克服的是分子间的作用力,所需能量较小,水的分解需要克服原子间的共价键,所需能量较大。
化学键与分子间的作用力比较
微粒间作用力
组成微粒
存在
作用力
影响范围
化学键
强
离子化合物的化学性质及熔沸点、硬度等物理性质
共价化合物、离子化合物、非金属单质
单质、化合物的化学性质
分子间的
分子间作用力
分子
分子间
弱
熔沸点、溶解度等物理性质
氢键
【典题例证2】 共价键、离子键和分子间作用力是构成物质的微粒间的不同作用方式,下列物质中,存在分子间作用力和共价键的是( )
A.干冰B.氯化钠
C.氢氧化钠D.金刚石
解析 干冰是由分子构成的物质,分子间存在着分子间作用力,分子内存在共价键。
氯化钠是离子化合物,只存在离子键。
氢氧化钠是离子化合物,它不仅存在离子键,其“OH-”中还存在共价键。
金刚石是由原子构成的物质,只存在共价键。
【学以致用2】 下列物质内存在分子间作用力的是( )
A.CaCl2B.KOH
C.SO2D.Na2O
解析 分子间作用力一般存在于大多数共价化合物和非金属单质的分子之间,SO2是共价化合物,其分子间存在分子间作用力。
而另外三个选项均为离子化合物,是以离子键结合的,没有分子间作用力。
答案 C
1.下列说法中不正确的是( )
A.共价化合物中没有离子键
B.离子化合物中不一定没有共价键
C.共价化合物中可以有离子键
D.离子键只能存在于离子化合物中
解析 离子键只能存在于离子化合物中,共价化合物中只能有共价键。
2.下列物质中只含有共价键的是( )
A.NaCl、HCl、H2O、NaOHB.Cl2、Na2S、HCl、SO2
C.HBr、CO2、H2O、CS2D.Na2O2、H2O2、H2O、O3
解析 A项中:
NaCl只含有离子键,HCl、H2O只含有共价键,NaOH既有离子键又有共价键;
B项中:
Cl2、HCl、SO2分子中只有共价键,而Na2S中只有离子键;
D项中:
Na2O2既有离子键又有共价键,H2O2、H2O、O3分子中只有共价键。
3.下列分子的电子式书写正确的是( )
4.CO2气体在一定条件下可与金属镁反应,干冰在一定条件下也可以形成CO2气体,这两个变化过程中需要克服的作用力分别是( )
A.化学键,化学键
B.化学键,分子间作用力
C.分子间作用力,化学键
D.分子间作用力,分子间作用力
5.下列是中学化学常见的物质
A.HCl B.NaCl C.Na2SO4 D.Na2S E.He F.N2
请用序号回答
(1)~(3)题:
(1)这些物质中只含共价键的是________。
(2)既含离子键又含共价键的是________。
(3)试写出D、F的电子式以及F的结构式________、________、________。
解析 HCl、N2只含共价键;
NaCl、Na2S只含离子键,Na2SO4含离子键和共价键;
He无化学键。
答案
(1)A、F
(2)C
课时作业
基础巩固
1.下列说法正确的是( )
A.由分子组成的物质中一定存在共价键
B.由非金属元素组成的化合物一定是共价化合物
C.共价键只存在于双原子单质分子里
D.两个非金属元素原子间不可能形成离子键
解析 由分子组成的物质也可能是稀有气体,稀有气体为单原子分子,不存在化学键,A错误;
而由非金属元素组成的化合物如NH4Cl是离子化合物,所以B错误;
共价键不仅存在于双原子单质分子里,也存在于离子化合物(如Na2O2)和多原子共价化合物(如H2O2)中,C错误;
两个非金属元素原子间不能通过得失电子形成离子键,只能通过共用电子对形成共价键,所以D正确。
答案 D
2.某元素的原子最外层只有一个电子,它与卤素原子结合时,所形成的化学键( )
A.一定是离子键
B.一定是共价键
C.可能是离子键也可能是共价键
D.以上说法都不正确
解析 该元素如果是碱金属元素则与卤素形成的是离子键,如果是氢元素,则形成的是共价键。
3.下列物质中,属于共价化合物的是( )
A.NH4ClB.HNO3
C.NaClD.I2
解析 只有HNO3是共价化合物,全部由非金属元素以共价键的形式形成。
4.下列物质或微粒用电子式表示的形成过程错误的是( )
解析 B项错误,离子化合物的电子式中相同的离子不能合并写。
5.下列化学用语正确的是( )
A.氮分子的电子式:
B.硫原子的结构示意图:
C.NH4Cl的电子式:
D.水分子的结构式:
解析 A项,漏掉了N原子最外层没有成键的电子,氮分子的电子式应为
B项,原子中核电荷数与核外电子数相等,硫原子的结构示意图应为
C项,Cl-的电子没有标出。
D项正确。
6.下列物质中只含有共价键的化合物是( )
①H2O ②CaCl2 ③NaOH ④Cl2 ⑤NH4Cl ⑥H2O2 ⑦H2SO4 ⑧Na2O2
A.①⑥⑦B.②④⑥
C.③②⑤⑧D.①④⑥⑦
解析 Cl2属于单质,故④不符合,排除B、D两项;
H2O、H2O2、H2SO4中只含共价键;
NaOH、NH4Cl、Na2O2中既含离子键又含共价键;
CaCl2中只含离子键。
7.关于氢键,下列说法不正确的是( )
A.HF的沸点比HCl的沸点高是由于HF分子间存在氢键所致
B.水在结冰时体积膨胀,是由于水分子之间存在氢键
C.NH3的稳定性很强,是因为其分子间能形成氢键
D.在氨水中水分子和氨分子之间也存在着氢键
解析 本题着重对氢键理解的考查。
氢键是某些氢化物(NH3、H2O、HF)分子间存在的比分子间作用力稍强的作用力。
它的存在使氢化物的熔点、沸点相对较高,因此,HF的沸点高是由氢键所致,水在结冰时体积膨胀是由于水分子大范围的以氢键相互连结,形成相对疏松的晶体,从而在结构上有许多空隙,造成体积膨胀。
氨分子和水分子之间主要是以氢键结合的,故A、B、D选项正确;
C选项NH3的稳定性取决于N—H键,而不是氢键,故C不正确。
8.以下关于分子间作用力的叙述不正确的是( )
A.是一种较弱的化学键
B.分子间作用力较弱,破坏它所需能量较少
C.分子间作用力对物质的熔、沸点有影响
D.稀有气体原子间存在分子间作用力
解析 分子间作用力不是化学键,化学键是物质内成键原子或离子间较强的相互作用,而分子间作用力是分子间微弱的相互作用,破坏它所需能量较少。
一般说来,对于组成和结构相似的物质,相对分子质量越大,分子间作用力越大,物质的熔沸点也越高。
稀有气体是单原子分子,其原子就是气体分子,在稀有气体中仅存在着微弱的分子间作用力。
9.下表物质与其所含化学键类型、所属化合物类型完全正确的一组是( )
选项
A
B
C
D
CO2
MgCl2
NH4Cl
所含化学键类型
离子键、共价键
所属化合物类型
解析 依据电子式可判断化学键类型,CO2:
,MgCl2:
,HCl:
,NH4Cl:
据离子化合物和共价化合物的定义判断化合物类型,含离子键的化合物为离子化合物,只含共价键的化合物为共价化合物。
10.下列分子中所有原子都满足最外层为8电子结构的是( )
A.BF3B.SiCl4
C.H2OD.PCl5
解析 若化合物中某元素化合价的绝对值与其原子的最外层电子数之和为8,则满足最外层8电子稳定结构;
选项A中B为+3价,与最外层电子数3之和为6,不符合题意;
选项B中Si为+4价,最外层有4个电子,Cl化合价为-1价,最外层有7个电子,符合要求;
选项C中H最外层为2电子稳定结构;
选项D中P的化合价为+5价,最外层5个电子,其和为10,不符合题意。
能力提升
11.
(1)写出下列物质的结构式。
N2________,CO2________,NH3________。
(2)写出下列物质的电子式。
NH4Cl________,KOH________,Na2O2________。
解析
(1)根据N2、CO2、NH3的电子式可写出其结构式分别为:
。
(2)NH4Cl、KOH、Na2O2均为含有共价键的离子化合物,其电子式分别为
12.在下列变化中:
①I2升华 ②烧碱熔化 ③NaCl溶于水 ④H2O2分解 ⑤Na2O2溶于水。
(1)未破坏化学键的是________(填序号,下同);
(2)仅离子键被破坏的是________;
(3)仅共价键被破坏的是________;
(4)离子键和共价键同时被破坏的是________。
解析 ①只破坏了分子间作用力,未破坏化学键;
②③破坏了离子键;
④2H2O2
2H2O+O2↑,只破坏共价键;
⑤Na2O2溶于水发生反应:
2Na2O2+2H2O===4NaOH+O2↑,离子键和共价键均被破坏。
答案
(1)①
(2)②③ (3)④ (4)⑤
13.如图是元素周期表中短周期元素的一部分,表中所列字母分别代表一种元素。
(1)上述________(填字母)元素原子半径最小。
(2)“神舟”九号飞船内需要有一种化合物来吸收宇航员呼出的CO2,你认为该物质应该是由上图中的________和________(均填字母)元素组成的。
飞船中需要制造一种适合宇航员生存的人工生态环境,应该在氧气中充入一种气体,用于稀释氧气,该气体分子的电子式是________。
(3)在一定条件下,a与h可形成一种化合物,当该物质呈固态时,其分子内化学键的类型为________;
该物质的电子式是________,结构式是________。
(4)现有另一种元素X,其原子获得一个电子的能力比上图中所列元素都要强。
则X是________(填名称)元素,其在周期表中位于________族,氢化物分子的电子式为________。
解析 据元素周期表结构可知各元素分别为:
氢的原子半径最小。
原子得到电子伴随着能量的释放,在其他条件相同时,得电子越容易,元素的非金属性越强,因此X所代表的是位于第2周期ⅦA族的氟元素。
14.A、B、C、D、E五种短周期元素,它们的原子序数逐渐增大。
B元素原子L层上的电子数为K层电子数的2倍;
元素D的2价阴离子的核外电子排布与氖原子相同;
E与A同主族;
A和E这两种元素与D都能形成X2Y、X2Y2型化合物。
请回答:
(1)写出下列元素的元素符号:
A________;
B________;
C________;
E________。
(2)画出D的原子结构示意图________。
B在周期表中的位置为________。
(3)A与D形成的X2Y型化合物的电子式是________。
(4)C的氢化物的电子式________,含有________键(填“离子”或“共价”)。
解析 由题意可知B为6C,D为8O,而A、B、C、D、E原子序数逐渐增大,则C为7N,再由“A、E同主族且A和E这两种元素与D都能形成X2Y、X2Y2型化合物”知A为1H,E为11Na。
答案
(1)H C N Na
(2)