高考复习氧化还原反应方程式书写Word文件下载.doc
《高考复习氧化还原反应方程式书写Word文件下载.doc》由会员分享,可在线阅读,更多相关《高考复习氧化还原反应方程式书写Word文件下载.doc(4页珍藏版)》请在冰点文库上搜索。
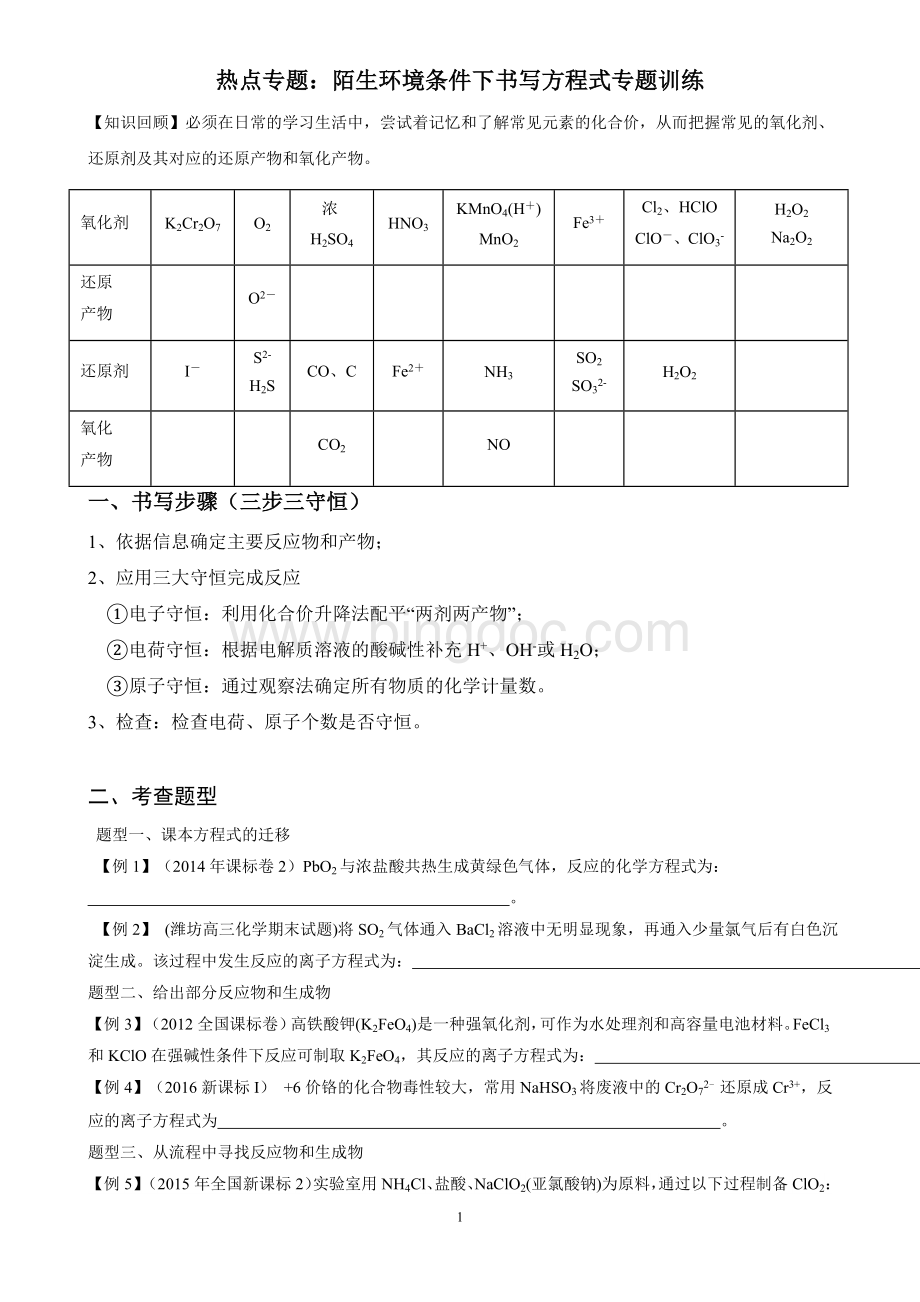
产物
O2-
还原剂
I-
S2-
H2S
CO、C
Fe2+
NH3
SO2
SO32-
氧化
CO2
NO
一、书写步骤(三步三守恒)
1、依据信息确定主要反应物和产物;
2、应用三大守恒完成反应
①电子守恒:
利用化合价升降法配平“两剂两产物”;
②电荷守恒:
根据电解质溶液的酸碱性补充H+、OH-或H2O;
③原子守恒:
通过观察法确定所有物质的化学计量数。
3、检查:
检查电荷、原子个数是否守恒。
二、考查题型
题型一、课本方程式的迁移
【例1】
(2014年课标卷2)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为:
。
【例2】(潍坊高三化学期末试题)将SO2气体通入BaCl2溶液中无明显现象,再通入少量氯气后有白色沉淀生成。
该过程中发生反应的离子方程式为:
。
题型二、给出部分反应物和生成物
【例3】
(2012全国课标卷)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。
FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为:
。
【例4】
(2016新课标I)+6价铬的化合物毒性较大,常用NaHSO3将废液中的Cr2O72﹣还原成Cr3+,反应的离子方程式为 。
题型三、从流程中寻找反应物和生成物
【例5】
(2015年全国新课标2)实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:
氯化铵溶液
电解
NCl3溶液
ClO2
溶液X
H2
盐酸
NaClO2溶液
电解时发生反应的化学方程式为。
题型四、陌生电化学方程式
【例6】
(2015新课标2)26.(14分)酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是有碳粉,二氧化锰,氯化锌和氯化铵等组成的填充物,该电池在放电过程产生MnOOH,……
(1)该电池的正极反应式为;
电池反应的离子方程式为。
练习:
1、某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况。
此消毒液中NaClO可吸收空气中的CO2生成NaHCO3和HClO而变质。
写出化学反应方程式。
2、氯化亚铁溶液经高温喷雾焙烧时转化为氯化氢气体和氧化铁粉末。
有关的化学方程式为:
。
3、完成氧化焙烧过程中生成的化学方程式
____Cr(OH)3+____Na2CO3+_____=____Na2CrO4+___CO2↑+_____
4、洗涤剂中的双氧水可以将废水中的氰化物转化为无毒物同时生成,写出反应的离子方程式;
5、高铁酸钾是一种高效多功能水处理剂。
工业上常采用NaClO氧化法生产,反应原理为:
①
在碱性条件下,利用NaClO氧化Fe(NO3)3制得Na2FeO4。
NaClO
+
Fe(NO3)3
NaOH=Na2FeO4↓+
NaCl
NaNO3
②
Na2FeO4与KOH反应生成K2FeO4:
Na2FeO4
2KOH=K2FeO4
2NaOH主要的生产流程如下:
(1)写出反应①的离子方程式。
(2)若NaClO加入过量,氧化过程中会生成Fe(OH)3,写出该反应的离子方程式:
。
若Fe(NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化还原反应生成K3FeO4,此反应的离子方程式:
(3)配平以下方程式
NaClO+Fe(NO3)3+NaOH=Na2FeO4↓+NaCl+NaNO3+;
6、为了处理含有Cr2O72-酸性溶液的工业废水,采用如下方法:
向废水中加人适量NaCl,以Fe为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成排出,从而使废水中铬含量低于排放标准。
①Cr2O72-转变为Cr3+的离子方程式为。
7、实验室可由软锰矿(主要成分为MnO2)制备KMnO4,方法如下:
软锰矿与过量固体KOH和KClO3在高温下反应,生成锰酸钾(K2MnO4)和KCl:
用水溶解,滤去残渣,滤液酸化后,K2MnO4转化为MnO2和KMnO4;
滤去MnO2沉淀,浓缩滤液,结晶得到深紫色的针状KMnO4。
(1)软锰矿制备K2MnO4的化学方程式是 。
(2)K2MnO4制备KMnO4的离子方程式是 。
8、将20mL0.5mol·
L-1Na2SO3溶液逐滴加入到20mL0.2mol·
L-1KMnO4溶液(硫酸酸化)中,溶液恰好褪为无色。
写出反应的离子方程式(已知反应后溶液存在Mn2+)。
9、硫酸亚铁在硫酸酸化条件下将MnO2还原为MnSO4,酸浸时发生的主要反应的离子方程式为。
10、我国卫生部已明确提出:
要逐步用二氧化氯替代氯气进行饮用水的消毒。
ClO2不稳定,可与NaOH溶液、H2O2反应,转化为比较稳定的亚氯酸钠(NaClO2)。
该反应的化学方程式为___________________________________。
NaClO3
溶液
ClO2发生器
ClO2吸收器
NaClO2
11、以Cl2为基本原料可以制取多种消毒剂,如亚氯酸钠(NaClO2)。
它常用于砂糖、油脂的漂白和杀菌。
以下是获得亚氯酸钠的简单流程图:
SO2
ClO2发生器中的反应的离子方程式是:
。
ClO2吸收器中反应的化学方程式为:
12、直接加热AlCl3·
6H2O不能得到无水AlCl3。
SOCl2为无色液体,极易与水反应生成HCl和一种具有漂白性的气体。
AlCl3·
6H2O与SOCl2混合加热制取无水AlCl3,反应的化学方程式是。
13、工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁[Fe(OH)SO4]的工艺流程如下:
(1)反应Ⅱ中发生反应的离子方程式为。
(2)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,Fe(OH)2+可部分水解生成Fe2(OH)42+聚合离子,该水解反应的离子方程式为。
14、活性氧化锌用作橡胶硫化的活性剂、补强剂。
以氧化锌粗品为原料制备活性氧化锌的生产工艺流程如下:
氧化锌粗品
H2SO4
溶解
滤渣
产品
滤液
Na2CO3
煅烧
除杂
沉淀
(1)“沉淀”得到ZnCO3·
2Zn(OH)2·
H2O,“煅烧”在450~500℃下进行,“煅烧”反应的化学方程式为。
15、反应Ⅰ的滤液中含有MnSO4、ZnSO4、CuSO4、Fe2(SO4)3、Al2(SO4)3等。
试完成反应Ⅰ中生成CuSO4和MnSO4的化学方程式:
MnO2+CuS+=↓++CuSO4+。
16、写出氮化镁与水反应的化学方程式:
,上世纪60年代有人将上述反应的气体作为燃料电池的燃料进行了实验,该气体与O2反应制成了N2和水,写出此碱性燃料电池的负极反应式:
。
4