中考命题研究遵义中考化学教材知识梳理第5章金属冶炼与利用分析.docx
《中考命题研究遵义中考化学教材知识梳理第5章金属冶炼与利用分析.docx》由会员分享,可在线阅读,更多相关《中考命题研究遵义中考化学教材知识梳理第5章金属冶炼与利用分析.docx(15页珍藏版)》请在冰点文库上搜索。
中考命题研究遵义中考化学教材知识梳理第5章金属冶炼与利用分析
第5章 金属的冶炼与利用
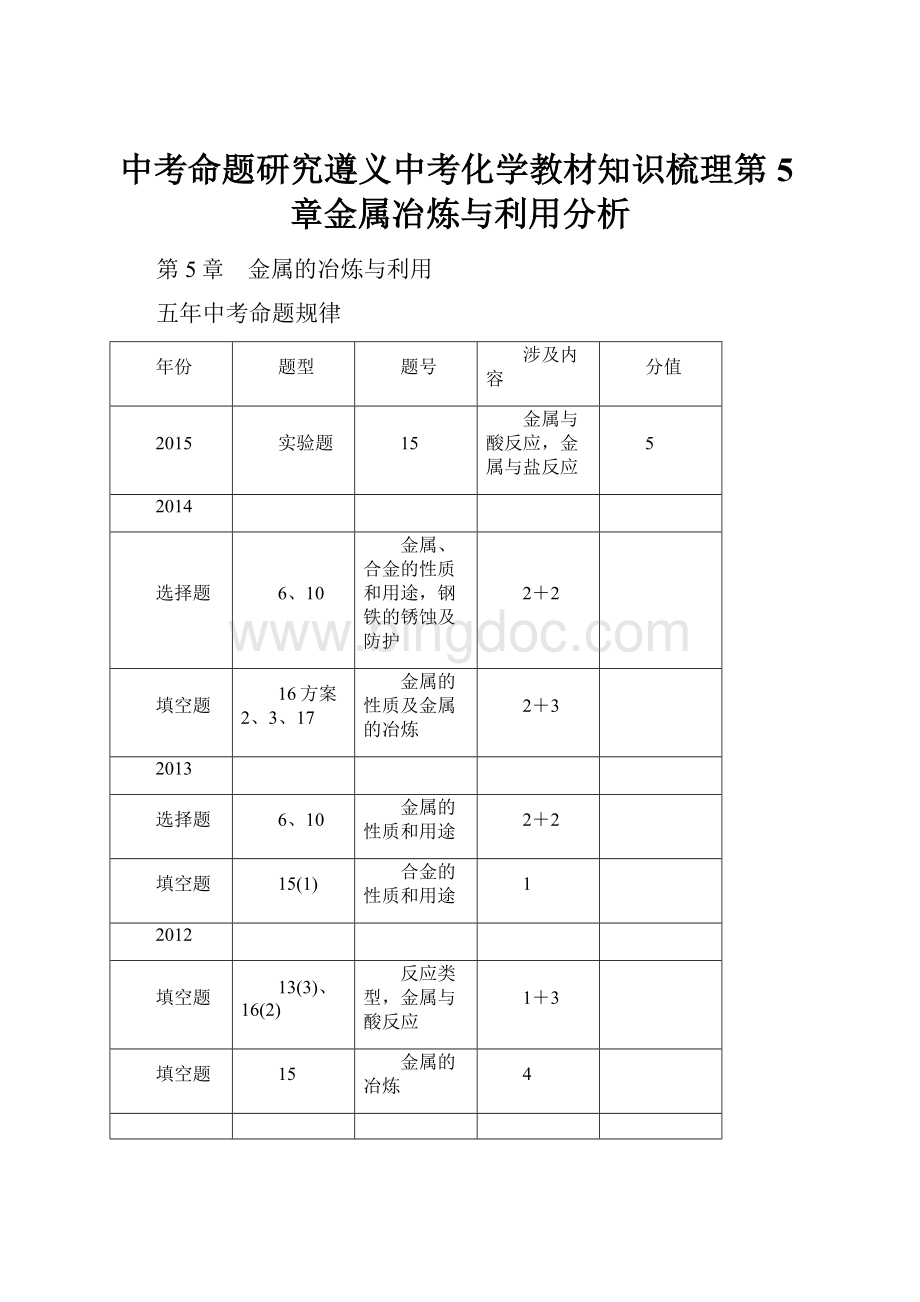
五年中考命题规律
年份
题型
题号
涉及内容
分值
2015
实验题
15
金属与酸反应,金属与盐反应
5
2014
选择题
6、10
金属、合金的性质和用途,钢铁的锈蚀及防护
2+2
填空题
16方案2、3、17
金属的性质及金属的冶炼
2+3
2013
选择题
6、10
金属的性质和用途
2+2
填空题
15
(1)
合金的性质和用途
1
2012
填空题
13(3)、16
(2)
反应类型,金属与酸反应
1+3
填空题
15
金属的冶炼
4
五年中考真题演练
金属的性质
1.(2015,遵义,15,5分)请按要求完成下列金属性质的实验。
研究一:
金属与酸反应过程中的能量变化。
(1)打磨后的镁条与稀盐酸反应,试管外壁发烫,说明该反应________(选填“放热”或“吸热”),反应的化学方程式为____________________;
(2)实验测得反应中产生气体的速度(v)与时间(t)的关系如右图,请根据t1~t2时间段反应速率变化,说明化学反应速率受________等因素影响。
研究二:
金属与盐溶液反应过程中的相关变化。
(1)某同学用硫酸铜溶液把“铁勺”变“铜勺”,其反应的化学方程式为__________________;
(2)在一定量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉,充分反应后,下图描述相关变化曲线,一定不正确的是________。
A
B
C
D
2.(2013,遵义,6,2分)下列有关金属的说法正确的是( )
A.铝有良好的抗氧化能力
B.合金一定不含非金属
C.生铁是化合物
D.赤铁矿是金属材料
3.[2012,遵义,13(3),1分]九年级化学学习的物质和化学反应在日常生活中有着实际的应用。
化学反应释放的热量常被人们所利用,如8Al+3Fe3O4高温9Fe+4Al2O3,铝热反应所放出的热量可用于焊接钢轨,该反应属于________(选填基本反应类型)反应。
金属的冶炼
4.(2011,遵义,15,4分)A~H均为初中化学中常见的物质,已知A、B为黑色固体,D为紫红色固体单质,F为红棕色粉末。
它们之间的转化关系如图所示(部分物质已略去),请回答:
(1)写出A+B→C+D的化学方程式:
____________________,该反应属于________反应(填化学反应基本类型)。
(2)写出E→G的化学方程式:
__________________________________。
(3)写出一个能实现G→D的化学方程式:
______________________。
5.(2014,遵义,8,2分)如图所示,为某化工企业生产流程示意图,有关说法正确的是( )
A.③中氩气(Ar)作反应物
B.钛酸亚铁(FeTiO3)中钛元素为+3价
C.②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为7∶1
D.①中反应为2FeTiO3+6C+7Cl2一定条件2X+2TiCl4+6CO,则X为FeCl2
金属防护和废金属回收
6.(2014,遵义,10,2分)控制变量法是实验探究的重要方法。
下列设计方案探究目的不能实现的是( )
A.甲可探究可燃物的燃烧是否需要与氧气接触
B.甲可探究可燃物的燃烧是否需要达到一定温度
C.乙中①③对比可探究铁的锈蚀条件与氧气是否有关
D.乙中①②③对比可探究铁的锈蚀条件与氧气和水等物质是否有关
中考考点清单
金属材料
1.金属的概念。
金属材料包括各种________和各种________。
2.金属的物理性质。
(1)颜色:
大多数金属呈银白色,特例:
金呈________色,铜呈________色。
(2)状态:
常温下为固体,特例:
________是液体。
(3)特性:
具有良好的导电性、导热性、延展性等。
3.合金。
(1)概念:
由一种金属跟其他______或________熔合形成的有金属特性的物质。
(2)常见的合金。
①青铜:
人类历史上使用最早的合金,由锡和铜组成。
②生铁和钢:
使用很广的钢和生铁由铁、碳组成,两者的区别是含碳量不同。
铁合金
生铁
钢
碳的含量
③其他常见的合金:
不锈钢、黄铜、铝合金。
(3)性质特点:
合金的硬度一般比组成它的各成分金属________;熔点一般比组各成它的成分金属________。
金属的化学性质
1.金属的化学性质。
(1)金属与氧气反应。
O2与镁________________________
与铁________________________
与铜________________________
与铝________________________
(2)金属与酸溶液反应。
镁与稀盐酸________________________
与稀硫酸________________________
锌与稀盐酸________________________
与稀硫酸________________________
铁与稀盐酸________________________
与稀硫酸________________________
【特别提醒】氢气的实验室制取。
(1)药品:
锌和稀硫酸。
(2)化学方程式:
Zn+H2SO4ZnSO4+H2↑。
【难点突破】金属与酸反应的曲线。
①等质氢图。
两种金属反应产生的氢气质量相同,此图反映了两种情况:
a.酸不足,金属过量,产生的氢气质量由酸的质量决定。
b.酸足量,投放的两种金属与酸反应产生氢气的质量恰好完全相同,如24g镁和56g铁分别投入足量的酸中反应产生的氢气质量相同。
②等质等价金属图。
如等质量的镁、铁、锌与足量的酸反应,生成物中金属的化合价均为+2价,产生氢气的速率和质量不同。
此图反映出:
a.金属越活泼,图示反应物的曲线越陡,如Mg线比Zn线陡,Zn线比Fe线陡。
b.金属的相对原子质量越小,与酸反应产生的氢气越多,曲线的拐点越高,消耗的酸越多。
(3)金属与某些盐溶液反应。
①铁与硫酸铜溶液。
现象:
银白色固体表面________________,溶液颜色由________逐渐变为__________;化学方程式:
____________________;结论:
铁的活动性________(选填“大于”或“小于”)铜。
②铜与硝酸银溶液。
现象:
铜丝表面__________________,溶液颜色由________变为________;化学方程式:
________________________;结论:
铜的活动性________(选填“大于”或“小于”)银。
2.置换反应。
①定义:
由一种单质跟一种化合物作用生成________和________,这样的反应叫做置换反应。
置换反应中一定存在化合价变化的元素。
②表达式:
A+BC→AC+B,例如:
Mg+2HClMgCl2+H2↑,Fe+2HClFeCl2+H2↑。
金属矿物和铁的冶炼
1.金属在自然界中的存在
极少数不活泼的金属(如铂、金、银等)在自然界中以________形式存在,其他大多数以________形式存在,金属化合物以矿物的形式存在。
2.金属矿石。
(1)铁矿石。
名称
化学式
赤铁矿
________
磁铁矿
Fe3O4
菱铁矿
FeCO3
黄铁矿
________
(2)铜矿石:
黄铜矿、孔雀石、斑铜矿和赤铜矿。
(3)铝矿石:
铝土矿和明矾石等。
3.实验突破:
金属的冶炼。
(1)实验原理:
铁的冶炼原理:
3CO+Fe2O3高温2Fe+3CO2(一氧化碳还原氧化铜的反应原理:
CO+CuO△Cu+CO2)
(2)装置。
(3)实验现象:
点燃酒精喷灯后,可观察到澄清石灰水________,玻璃管中固体__________________(一氧化碳还原氧化铜现象:
试管内固体________________、澄清石灰水________)。
(4)操作顺序。
操作顺序
解释或结论
先点燃酒精灯,通入一段时间CO再点燃酒精喷灯
先点燃酒精灯的目的是防止CO造成空气污染,通入CO的目的是除尽装置内的空气,防止加热时发生爆炸
点燃酒精喷灯,给氧化铁加热
使氧化铁和一氧化碳发生反应
实验结束,先熄灭酒精喷灯,继续通入CO直至试管冷却
防止试管内压强减小,引起倒吸,防止生成的铁被空气中的氧气氧化
(5)尾气处理:
CO有毒,应将排出的尾气________或收集起来。
金属防护和废金属回收
1.钢铁的锈蚀及防护。
(1)铁锈的主要成分________。
(2)锈蚀条件:
铁与________、________同时接触。
2.实验突破:
金属的锈蚀。
(1)实验原理:
________________________________________________________________________。
(2)实验操作。
编号
Ⅰ
Ⅱ
Ⅲ
实验
条件
铁钉与空气和水同时接触
铁钉全部没入蒸馏水中
铁钉在干燥的空气中
实验
图示
(3)实验现象:
经过一段时间后,第一支试管中铁钉表面出现________铁锈,且在空气和蒸馏水________处铁锈更多,第二支试管和第三支试管中铁钉表面________锈迹。
(4)实验结论:
对比第一支试管的现象和第二支试管的现象可知铁生锈需要________;对比第一支试管的现象和第三支试管的现象可知铁生锈需要________。
铁生锈的条件是________________________。
(5)注意事项:
①第二支试管所用蒸馏水是经煮沸并迅速冷却的蒸馏水,煮沸的目的是____________________,迅速冷却的目的是______________________。
②第二支试管中植物油的作用是________________,防止空气中的氧气溶解到水中。
③第三支试管加入干燥剂的目的是________________。
【温馨提示】同样暴露在空气中的金属铁比金属铝容易锈蚀的原因:
铁锈疏松多孔,不能阻止铁与氧气、水继续反应;而铝与氧气反应生成的致密的氧化铝薄膜能防止铝进一步被氧化。
3.
(1)除锈方法:
①物理方法:
砂纸打磨、冷拉。
②化学方法:
用________除铁锈,反应的化学方程式为________________________________.
(2)防护方法:
①保持钢铁表面________;
②在钢铁表面________________;
③在钢铁表面镀上一层________。
4.废金属的回收利用。
(1)废金属的危害:
不但造成资源浪费,还会产生镉、汞等有毒金属对环境的污染。
(2)废金属回收利用的意义:
既可以节约大量的金属资源,又能减少重金属对环境的污染。
中考重难点突破
金属材料的判断
【例1】(2014,钦州)3D打印技术将改变人类的生活方式。
下列3D打印常用材料中,属于合金的是( )
A.尼龙 B.陶瓷
C.不锈钢D.橡胶
【解析】尼龙是有机合成材料,陶瓷是无机非金属材料,不锈钢是金属材料,橡胶是有机高分子材料,其中天然橡胶属于天然高分子材料,合成橡胶属于合成高分子材料。
【答案】C
1.(2015,苏州)材料是人类赖以生存和发展的重要物质。
下列材料分类中正确的是( )
A.铝合金属于金属材料
B.有机玻璃属于无机非金属材料
C.塑料属于复合材料
D.陶瓷属于合成材料
金属的化学性质
【例2】(2014,临沂)若金属锰在金属活动性顺序中位于铝和锌之间,则下列反应不能发生的是(提示:
MnSO4溶于水)( )
A.Mn+2HClMnCl2+H2↑
B.Fe+MnSO4FeSO4+Mn
C.2Al+3MnSO4Al2(SO4)3+3Mn
D.Mg+MnSO4MgSO4+Mn
【解析】金属锰在金属活动性顺序中位于铝和锌之间,则金属活动性顺序为Mg>Al>Mn>Zn>Fe>H,根据置换反应发生的规则,金属Mn分别能和稀盐酸、ZnSO4、FeSO4溶液反应,MnSO4溶液能和Mg、Al反应,而Fe和MnSO4的反应不可能发生。
故选B。
【答案】B
【方法指导】金属与盐溶液反应的先后规律。
(1)当活动性较强的金属与另外多种活动性较弱的金属的盐溶液反应时,活动性最弱的金属盐溶液优先与金属反应;
(2)当活动性较弱的金属的盐溶液与另外多种活动性较强的金属单质反应时,活动性最强的金属单质优先与盐溶液反应。
如Fe加入CuSO4、AgNO3的混合溶液中时,Fe先与AgNO3反应,AgNO3反应完后,再与CuSO4反应。
2.(2015,佛山)为了探究a、b、c三种金属活动性顺序,某同学设计了如下实验。
实验结论正确的是( )
A.b>a>cB.a>b>c
C.c>b>aD.c>a>b
金属与酸反应的图象问题
【例3】(2014,衡阳)相同质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(M、N在生成物中均为+2价),生成H2质量和反应时间的关系如下图所示。
下列有关叙述正确的是( )
A.金属活动性N>M
B.生成H2的质量相等
C.相对原子质量N>M
D.消耗盐酸的质量相等
【解析】根据图象可以看出,纵坐标表示生成氢气质量,横坐标表示反应时间,故斜率表示反应速率。
由于M的斜率比N的大,所以M比N反应的速率快,所以M比N活泼,故A项错误;根据图象可以看出,M产生的氢气多,N产生的氢气少,故B项错误;价态相同的等质量金属与足量的酸反应时,相对原子质量越大,产生的氢气越少,M产生的氢气比N多,说明N的相对原子质量比M大,故C项正确;若两个反应消耗盐酸的质量相等,则置换出的氢的质量相等,产生的氢气的质量应该相同,而由图象可以看出二者产生的氢气质量不相等,故D项错误。
【答案】C
3.(2014,南宁)将等质量的镁和铁分别放入等质量、相同质量分数的稀盐酸中,产生氢气的质量与反应时间的关系如图所示,下列说法错误的是( )
A.反应结束后镁一定有剩余
B.反应消耗盐酸的总质量一定相等
C.O~t1时段,产生氢气的质量镁比铁大
D.O~t2时段,参加反应的镁的质量与铁相等
【方法指导】金属与酸反应的图象问题分析。
以四种常见金属Mg、Al、Fe、Zn为例,它们与酸反应的快慢顺序(即活动性顺序)为Mg>Al>Zn>Fe。
下图为这四种金属与酸反应的常见图象。
金属与酸反应的图象主要注意三个方面:
(1)观察图象的横坐标和纵坐标所表示的量的意义。
(2)观察图象的斜率,即金属与酸反应的速率。
斜率越大,速率越快。
简称为“陡不陡,比速率”。
(3)观察图象的水平线,即金属与酸反应产生的氢气的量的多少。
水平线越高,产生的氢气的量越多。
简称为“高不高,比多少”。
古今名言
敏而好学,不耻下问——孔子
业精于勤,荒于嬉;行成于思,毁于随——韩愈
兴于《诗》,立于礼,成于乐——孔子
己所不欲,勿施于人——孔子
读书破万卷,下笔如有神——杜甫
读书有三到,谓心到,眼到,口到——朱熹
立身以立学为先,立学以读书为本——欧阳修
读万卷书,行万里路——刘彝
黑发不知勤学早,白首方悔读书迟——颜真卿
书卷多情似故人,晨昏忧乐每相亲——于谦
书犹药也,善读之可以医愚——刘向
莫等闲,白了少年头,空悲切——岳飞
发奋识遍天下字,立志读尽人间书——苏轼
鸟欲高飞先振翅,人求上进先读书——李苦禅
立志宜思真品格,读书须尽苦功夫——阮元
非淡泊无以明志,非宁静无以致远——诸葛亮
熟读唐诗三百首,不会作诗也会吟——孙洙《唐诗三百首序》
书到用时方恨少,事非经过不知难——陆游
问渠那得清如许,为有源头活水来——朱熹
旧书不厌百回读,熟读精思子自知——苏轼
书痴者文必工,艺痴者技必良——蒲松龄
声明
访问者可将本资料提供的内容用于个人学习、研究或欣赏,以及其他非商业性或非盈利性用途,但同时应遵守著作权法及其他相关法律的规定,不得侵犯本文档及相关权利人的合法权利。
谢谢合作!