高考化学复习高考探究实验题的训练docxWord文件下载.docx
《高考化学复习高考探究实验题的训练docxWord文件下载.docx》由会员分享,可在线阅读,更多相关《高考化学复习高考探究实验题的训练docxWord文件下载.docx(13页珍藏版)》请在冰点文库上搜索。
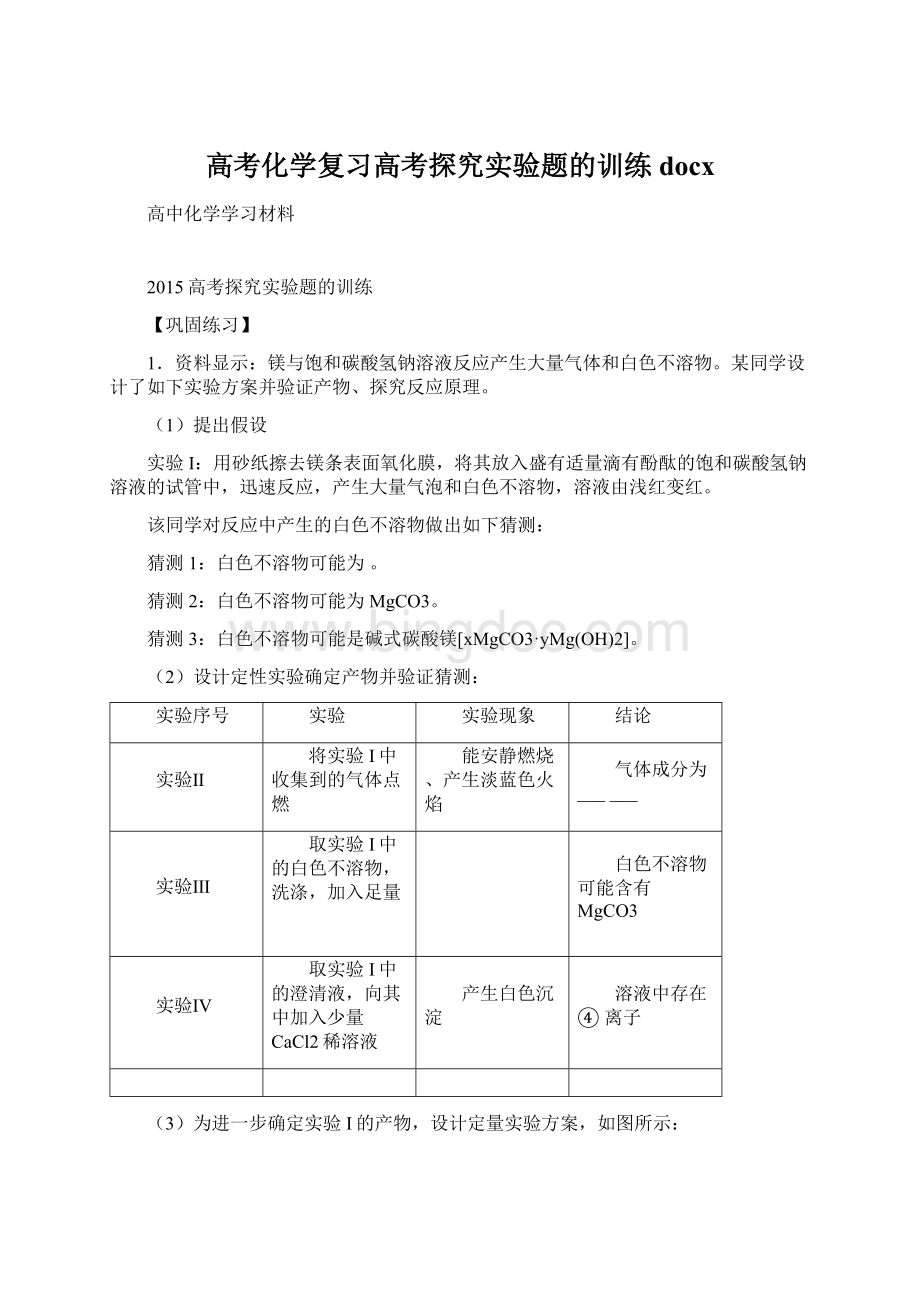
取实验I中的白色不溶物,洗涤,加入足量
白色不溶物可能含有MgCO3
实验Ⅳ
取实验I中的澄清液,向其中加入少量CaCl2稀溶液
产生白色沉淀
溶液中存在④离子
(3)为进一步确定实验I的产物,设计定量实验方案,如图所示:
称取实验Ⅰ中所得干燥、纯净的白色不溶物22.6g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中。
实验前后装置A增重1.8g,装置B增重8.8g,试确定白色不溶物的化学式。
(4)请结合化学用语和化学平衡移动原理解释Mg和NaHCO3溶液反应产生大量气泡的原因_________。
2.某研究性学习小组用如图所示的装置进行Na2O2和H2O反应的实验。
(1)可以验证有氧气生成的实验方法是:
(2)将导管q放入水中,反应过程中导管口有气泡冒出,说明:
。
(3)往试管中加水至固体完全溶解且不再有气泡生成后,取出试管,往试管中滴入实验室常用无色指示剂试液A,可观察到溶液变红,后红色褪去,则该指示剂为。
小组同学经查阅资料后得知红色褪去的原因有二:
一是NaOH溶液的浓度过大;
二是反应过程中可生成H2O2,H2O2氧化漂白了酚酞试液。
为了排除前者因素影响,可采取的方法是
(4)为进一步探究H2O2是否能够氧化指示剂试液,某同学向3mL30%H2O2的溶液中滴入2滴品红指示剂,充分振荡并放置约3min,溶液红色无明显改变。
后加入少量0.5mol/LNaOH的溶液后,可看到产生许多小气泡,且溶液红色可迅速褪去。
该现象表明:
,产生气泡的反应方程式为
3.在三支洁净试管中分别倒入约2mL工业硝酸,进行下述三个实验,以证明“工业硝酸呈黄色是由于NO2溶于浓硝酸引起的”,实验方法和现象如下表:
①置于酒精灯上小火加热(在通风厨中进行)
有红棕色气体逸出,继续加热,直到不再有红棕色气体逸出为止。
溶液的黄色变浅,但不能完全消失。
②通入氧气
通入足量氧气后,上述工业硝酸黄色变浅。
③加入5mL的蒸馏水,振荡使之充分混合
试管中的硝酸接近于无色。
说明:
在①②实验后的溶液中加入各1mL苯,充分振荡,静置,苯层为无色,下层仍为浅黄色。
⑴根据上述实验①②的现象你能得出什么结论?
___________________________________
_____________________________________________________________________。
⑵①②实验最终溶液是浅黄色,请猜想可能原因__________________________________,试设计实验方案证明你的猜想_________________________________________________
__________________________________________________________________________。
⑶实验③与实验①②最终实验颜色不同的原因可能是______________________________,
试设计实验方案证明________________________________________________________
4.某种催化剂为铁的氧化物。
化学兴趣小组在实验室对该催化剂中铁元素的价态进行探究:
将适量稀硝酸加入少许样品中,加热溶解;
取少许溶液,滴加KSCN溶液后出现红色。
一位同学由此得出该催化剂中铁元素价态为+3的结论。
(1)请指出该结论是否合理并说明理由
。
(2)请完成对铁元素价态的探究:
限选实验仪器与试剂:
烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹:
3mol·
L-1H2SO4、3%H2O2、6mol·
L-1HNO3、0.01mol·
L-1KmnO4、NaOH稀溶液、0.1mol·
L-1Kl、20%KSCN、蒸馏水。
①提出合理假设
假设1:
;
假设2:
假设3:
②设计实验方案证明你的假设(不要在答题卡上作答)
③实验过程
根据②的实验方案,进行实验。
请在答题卡上按下表格式写出实验操作步骤、预期现象与结论。
实验操作
预期现象与结论
步骤1:
步骤2:
步骤3:
……
5.某研究小组探究SO2和Fe(NO3)3溶液的反应。
已知:
1.0mol/L的Fe(NO3)3溶液的pH=1
请回答:
(1)装置A中反应的化学方程式是。
(2)为排除空气对实验的干扰,滴加浓硫酸之前应进行的操作是。
(3)装置B中产生了白色沉淀,其成分是,说明SO2具有性。
(4)分析B中产生白色沉淀的原因:
观点1:
观点2:
SO2与Fe3+反应;
观点3:
在酸性条件下SO2与NO3-反应;
①按观点2,装置B中反应的离子方程式是,证明该观点应进一步确认生成的新物质,其实验操作及现象是。
②按观点3,只需将装置B中的Fe(NO3)3溶液替换为等体积的下列溶液,在相同条
件下进行实验。
应选择的试剂是(填序号)。
a.0.1mol/L稀硝酸
b.1.5mol/LFe(NO3)2溶液
c.6.0mol/LNaNO3和0.2mol/L盐酸等体积混合的溶液
6.某化学课外活动小组通过实验研究NO2的性质。
2NO2+2NaOH==NaNO3+NaNO2+H2O
任务1:
利用下图所示装置探究NO2能否被NH3还原(K1、K2为止水夹,夹持固定装置略去)。
(1)E装置中制取NO2反应的化学方程式是。
(2)若NO2能够被NH3还原,预期观察到C装置中的现象是。
(3)实验过程中,未能观察到C装置中的预期现象。
该小组同学从反应原理的角度分
析了原因,认为可能是:
①NH3还原性较弱,不能将NO2还原;
②在此条件下,NO2的转化率极低;
③。
(4)此实验装置存在一个明显的缺陷是。
任务2:
探究NO2能否与Na2O2发生氧化还原反应。
(5)实验前,该小组同学提出三种假设。
二者不反应;
NO2能被Na2O2氧化;
(6)为了验证假设2,该小组同学选用任务1中的B、D、E装置,
将B中的药品更换为Na2O2,另选F装置(如右图所示),重
新组装,进行实验。
①装置的合理连接顺序是(某些装置可以重复使用)。
②实验过程中,B装置中淡黄色粉末逐渐变成白色。
经检验,该白色物质为纯净物,
且无其他物质生成。
推测B装置中反应的化学方程式为。
7.一学习小组利用下图所示装置,对某含少量Fe的废铜屑进行铜含量的测定,并探究利用其制备硫酸铜溶液。
(1)向A中加入10g废铜屑样品,关闭弹簧夹,打开B活塞向A注入足量稀硫酸后关闭。
此时装置C中发生的现象是。
(2)反应进行到A中不再产生气泡时,若C中收集到448mL(已换算成标准状况)气体,则该废铜屑中铜的质量百分含量为。
(3)拆除C、D装置后,打开弹簧夹,持续将空气通入A中,至A中固体全部消失,再继续通入一段时间空气后,关闭弹簧夹,停止通入空气。
①该过程中发生反应的离子方程式是、;
②为使A中固体加快溶解速率,以下方法运用合理的是。
a.对A装置加热b.向A内加入少量Fe2O3c.向A内加入少量CuO
d.增大空气通入量e.向A内加入少量FeSO4f.向A内加入少量H2O
(4)将A中溶液倒入烧杯内,加入Cu2(OH)2CO3将其调节至pH=4时,溶液中铁被完全沉淀,过滤后即得红褐色沉淀与硫酸铜溶液,此过程离子反应方程式是。
(5)有同学认为,可以不用测量气体法计算废铜屑中铜的质量百分含量,则其采用的方法是,其具体操作步骤可续写为:
8.Na2CO3溶液和CuSO4溶液混合后,产生蓝色沉淀,请你推测可能有哪些产物?
并设计实验来验证。
[提示]经查资料得知:
CuCO3和Cu(OH)2均不带结晶水。
假设一:
假设二:
假设三:
9.氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品。
某研究小组用粗铜(含杂质Fe)按下述流程制备氯化铜晶体(CuCl2·
2H2O)。
(1)实验室采用如下图所示的装置,可将粗铜与Cl2反应转化为固体1(部分仪器和夹持装置已略去)。
①仪器A的名称是。
②装置B中发生反应的离子方程式是。
③有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为是否必要
(填“是”或“否”)。
(2)试剂X用于调节pH以除去杂质,X可选用下列试剂中的(填序号)。
a.NaOHb.NH3·
H2Oc.CuOd.Cu2(OH)2CO3e.CuSO4
(3)在溶液2转化为CuCl2·
2H2O的操作过程中,发现溶液颜色由蓝色变为绿色。
小组同学欲探究其原因。
在氯化铜溶液中有如下转化关系:
Cu(H2O)42+(aq)+4Cl-(aq)CuCl42-(aq)+4H2O(l)
蓝色黄色
①上述反应的化学平衡常数表达式是K=。
若增大氯离子浓度,K值(填“增大”、“减小”或“不变”)。
②取氯化铜晶体配制成蓝绿色溶液Y,进行如下实验,其中能够证明CuCl2溶液中有上述转化关系的是(填序号)。
a.将Y稀释,发现溶液呈蓝色
b.在Y中加入CuCl2晶体,溶液变为绿色
c.在Y中加入NaCl固体,溶液变为绿色
d.取Y进行电解,溶液颜色最终消失
10.某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验。
【实验1】铜与浓硫酸反应,实验装置如图20所示。
实验步骤:
①先连接好装置,检验气密性,加入试剂;
②加热A试管直到B中品红褪色,熄灭酒精灯;
③将Cu丝上提离开液面。
(1)装置A中发生反应的化学方程式为。
(2)熄灭酒精灯后,因为有导管D的存在,B中的液体不会倒吸,其原因是。
(3)拆除装置前,不需打开胶塞,就可使装置中残留气体完全被吸收,应当采取的操作是。
【实验2】实验中发现试管内除了产生白色固体外,在铜丝表面还产生黑色固体甲,其中可能含有氧化铜、硫化铜、硫化亚铜,以及被掩蔽的氧化亚铜。
查阅资料:
①氧化亚铜在酸性环境下会发生自身氧化还原反应生成Cu2+和铜单质,在氧气流中煅烧,可以转化为氧化铜。
②硫化铜和硫化亚铜常温下都不溶于稀盐酸,在氧气流中煅烧,硫化铜和硫化亚铜都转化为氧化铜和二氧化硫。
为了研究甲的成分,该小组同学在收集到足够量的固体甲后,进行了如图21的实验:
(4)②中检验滤渣是否洗涤干净的实验方法是。
(5)③中在煅烧过程中一定发生的反应的化学方程式为。
(6)下列对于固体甲的成分的判断中,正确的是(填字母选项)。
A.固体甲中,CuS和Cu2S不能同时存在
B.固体甲中,CuO和Cu2O至少有一种
C.固体甲中若没有Cu2O,则一定有Cu2S
D.固体甲中若存在Cu2O,也可能有Cu2S
【答案与解析】
1.
(1)猜测1:
Mg(OH)2
(2)①氢气②稀盐酸(合理均可)③产生气泡,沉淀全部溶解④CO32-
(3)2MgCO3·
Mg(OH)2或Mg(OH)2·
2MgCO3或Mg3(OH)2(CO3)2
(4)NaHCO3溶液中存在如下平衡:
HCO3-
H++CO32-、H2O
H++OH-;
Mg和H+反应生成H2和Mg2+,Mg2+跟OH-、CO32-生成难溶物Mg(OH)2·
2MgCO3,则H+、OH-、CO32-的浓度均降低,促使上述两平衡均向右移动。
故Mg和饱和NaHCO3溶液反应产生大量气体H2。
2.1)将带火星的木条靠近导管p处,木条复燃。
(2)该反应放热
(3)酚酞试液(4)从试管中取出少许溶液加水稀释,再滴入A指示剂,红色不能褪去。
(5)说明H2O2本身并不能氧化漂白指示剂,但在碱性条件下可迅速将指示剂氧化:
。
3.⑴呈黄色的工业硝酸中存在NO2气体,但还有其他呈黄色的杂质
⑵可能含有Fe3+;
在加热除去NO2的工业硝酸中加入KSCN溶液,或在除去NO2的工业硝酸中,缓缓加入足量NaOH固体
⑶NO2与水反应使溶液恢复无色,也可能是由于水将工业硝酸的黄色冲淡了。
做对比实验:
取与除去NO2的工业硝酸颜色一样的FeCl3溶液2mL,加入5mL的蒸馏水,观察现象
4.
(1)该结论不正确。
稀HNO3有强氧化性,若该铁的价态为+2价,则被氧化为+3价同样可使KSCN溶液变血红色。
(2)①
催化剂中铁元素的价态为+3价。
催化剂中铁元素的价态为+2价。
催化剂中铁元素的价态既有+3价也有+2价。
③
用滴管量取一定量的3mol·
L-1H2SO4于试管中,加热煮沸数分钟以除去其中溶解的氧
用钥匙取少许样品于试管中,用滴管加入步骤1中的稀硫酸,并加热,充分反应后得到A溶液
固体溶解,溶液颜色有变化
取少量步骤2中的A溶液于试管中,滴加1~2滴KSCN溶液,振荡
(1)若溶液不变红色,则假设2成立
(2)若溶液变红色,则假设1或假设3成立
步骤4:
另取少量步骤2中的A溶液于试管中,滴加1~2滴0.01mol·
L-1KMnO4溶液,振荡试管
结合步骤3中的
(2):
(1)溶液呈紫红色,则假设1成立
(2)若溶液紫红色褪去,则假设3成立
5.
(1)Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O
(2)打开弹簧夹,向装置中通入一段时间的N2,关闭弹簧夹
(3)BaSO4还原性
(4)观点1:
SO2和Fe3+、酸性条件下NO3-都反应(1分)
①SO2+2Fe3++Ba2++2H2O=BaSO4↓+2Fe2++4H+(可分两步写)
取少量B中溶液于试管中,加入少量铁氰化钾[K3Fe(CN)6]溶液产生蓝色沉淀,则溶液中有Fe2+,观点2合理
②c
6.
(1)Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O
(2)C装置中混合气体颜色变浅(其他合理答案酌情给分)
(3)在此条件下,该反应的化学反应速率极慢。
(4)缺少尾气吸收装置
(5)NO2能被Na2O2还原(其他合理答案酌情给分)
(6)①EDBDF或EDBF
②2NO2+Na2O2===2NaNO3
7.
(1)水面下降,水顺长导管排入D中
(2)88.8%
(3)①4Fe2++O2+4H+=4Fe3++2H2O
2Fe3++Cu=2Fe2++Cu2+
②abde
(4)Cu2(OH)2CO3+H++Fe3+=2Cu2++Fe(OH)3↓+CO2↑(也可分两步写)
(5)测定沉淀法,将(4)中所得红褐色沉淀洗涤、干燥、称量、计算
8.假设一:
Na2CO3溶液和CuSO4溶液混合后直接发生沉淀反应,生成CuCO3沉淀。
Na2CO3溶液和CuSO4溶液混合后发生双水解反应,生成Cu(OH)2沉淀。
Na2CO3溶液和CuSO4溶液混合后既发生沉淀反应,又发生双水解反应,生成CuCO3和Cu(OH)2两种沉淀的混合物。
方案一:
向洗涤干净并低温烘干的沉淀中加入盐酸,证明生成物中含CuCO3,另取沉淀加热灼烧,检验生成的水,证明生成物中含Cu(OH)2。
方案二:
将洗涤干净并低温烘干的沉淀直接加热灼烧,将生成的气体依次通过无水硫酸铜、澄清石灰水,检验生成的水或二氧化碳,证明生成物中含Cu(OH)2或CuCO3或两者兼有。
9.
(1)①分液漏斗
②MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
③否
(2)cd
(3)①不变
②abc
10.
(1)2H2SO4(浓)+Cu
CuSO4+SO2↑+2H2O。
(2)试管A中气体压强减小,空气从D导管进入试管A中。
(3)从D管口向A中大量鼓气。
(4)取最后一次洗涤后所得液体于试管中,滴加硝酸银溶液,若无白色沉淀产生,则说明沉淀洗涤干净;
若有白色沉淀生成,则说明未洗干净。
(5)2CuS+3O2
2CuO+2SO2(条件也可为“煅烧”)
(6)BCD