初中化学人教版九年级下学期 第八单元课题3 金属资源的利用和保护B卷Word文档格式.docx
《初中化学人教版九年级下学期 第八单元课题3 金属资源的利用和保护B卷Word文档格式.docx》由会员分享,可在线阅读,更多相关《初中化学人教版九年级下学期 第八单元课题3 金属资源的利用和保护B卷Word文档格式.docx(13页珍藏版)》请在冰点文库上搜索。
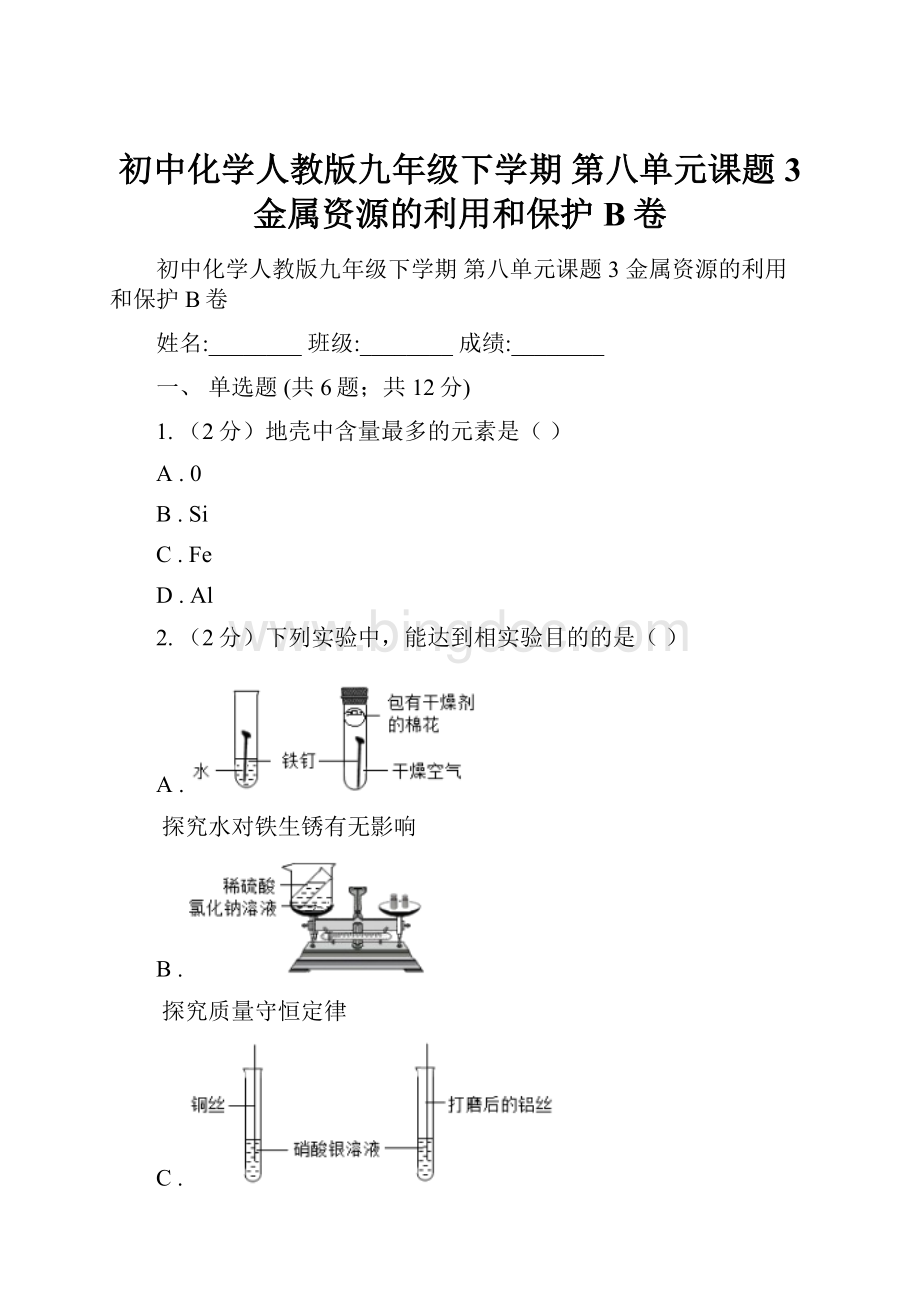
探究甲烷的组成
3.(2分)为防止家中菜刀生锈,小风设计了如下方案:
①每天用汽油擦拭一遍②用完后保存在盐水中③擦干后用植物油涂抹④用干布把它擦干,悬挂⑤用食醋涂抹⑥用酱油涂抹。
请选出你认为合理的方案()
A.①②③④⑥⑦
B.②③④
C.③④
D.⑤⑥⑦
4.(2分)金属用途广泛,其结构和性质是化学的重要研究内容。
下列说法正确的是()
A.金属铝耐腐蚀,是因为铝的化学性质稳定
B.“真金不怕火炼”仅仅是因为黄金的熔点高
C.合金与组成它的金属相比,硬度更大,熔点更低
D.铁生锈是铁与氧气和水共同作用的结果,铁锈的主要成分是Fe3O4
5.(2分)谚语诗词中蕴含着科学道理。
A.“真金不怕火炼”是说黄金熔点很高
B.“满架蔷薇一院香”的原因是分子在不停地运动
C.“百炼成钢”与“只要功夫深铁杵磨成针”蕴含的化学原理相同
D.“众人拾柴火焰高”是指可燃物越多,着火点越低,越容易着火
6.(2分)下列实验设计能够实现其对应实验目的是()
验证质量守恒定律
测定空气中氧气含量
探究铁钉锈蚀的条件
探究燃烧条件之一:
温度达到着火点
二、实验探究题(共3题;
共21分)
7.(7分)铜、铁是人类使用最早、应用广泛的金属.
(1)
(一)对古代制品的认识
青铜铸件、丝绸织品、陶瓷器皿是我国古代劳动人民创造的辉煌成就.
①上述制品不涉及到的材料是________(选填序号).
A、金属材料
B、无机非金属材料
C、复合材料
②如图1为出土文物古代青铜铸件“马踏飞燕”.该文物能保存至今的原因可能是________(选填序号).
A、铜的活泼性弱
B、铜不会生锈
C、深埋于地下,隔绝空气
(2)
(二)铁、铜的冶炼
①我国古代曾用孔雀石炼铜,涉及主要反应的化学方程式:
________,2CuO+C
2Cu+CO2↑.
②铁、铜矿石有赤铁矿(Fe2O3)、磁铁矿(Fe3O4)、黄铁矿(FeS2)、黄铜矿(CuFeS2)等.CuFeS2为二硫化亚铁铜,其中S元素的化合价为________.
③工业炼铁大多采用赤铁矿、磁铁矿.以磁铁矿为原料炼铁反应的化学方程式为________.炼铁不采用黄铁矿、黄铜矿,可能的原因是:
黄铁矿、黄铜矿含铁量相对低;
________.
④以黄铜矿为原料,采用生物炼铜是现代炼铜的新工艺,原理为:
4CuFeS2+17O2+2H2SO4
4CuSO4+2Fe2(SO4)3+2H2O.
向上述反应后的溶液中加入Fe粉,得到FeSO4溶液和Cu.
1)发生主要反应的化学方程式:
Fe+Fe2(SO4)3=3FeSO4,________.
2)FeSO4溶液经蒸发浓缩、________、过滤等操作得到FeSO4•7H2O晶体.
(3)(三)黄铜矿中铁、铜含量的测定
在科研人员指导下,兴趣小组称取25.00g黄铜矿(含少量Fe2O3和其它不含金属元素的杂质)模拟生物炼铜,使其全部转化为CuSO4、Fe2(SO4)3溶液.向溶液中加入过量NaOH溶液得到Cu(OH)2、Fe(OH)3固体.
①证明NaOH溶液过量的方法:
静置,向上层清液中滴加________溶液,无现象.
②用图2装置对固体进行热分解实验.
【资料】
①在68℃时,Cu(OH)2分解为CuO;
在500℃时,Fe(OH)3分解为Fe2O3.
②在1400℃时,CuO分解为Cu2O和O2,Fe2O3分解为复杂的铁的氧化物和O2.
1)装配好实验装置后,先要________.
2)停止加热后仍需继续通N2,可防止倒吸和________.
3)控制不同的温度对A中固体加热,测得装置B和C中铜网的质量变化如表.
温度/℃
室温
100
550
1400
B装置/g
200.00
201.80
205.04
C中铜网/g
100.00
101.28
①此黄铜矿中铜、铁元素的质量分数:
ω(Cu)%=________;
ω(Fe)%=________.
②复杂的铁的氧化物化学式为________.
8.(2分)U型玻璃管是常见的化学仪器,在实验中有广泛的应用。
(1)借助U型玻璃管探究微粒的性质,如图1所示,打开玻璃旋塞,观察到湿润的红色石蕊试纸从左到右先后变蓝,该实验说明分子________,湿棉花的作用是________。
(2)借助U型玻璃管探究钢铁锈蚀的条件,如图2所示:
①一段时间后潮湿的钢丝棉有明显锈迹,干燥的钢丝棉没有锈迹,此现象说明________。
②实验结束时,细心的同学发现浸没在凉开水中的钢丝棉也有少量锈迹,说明本实验有不完善之处,请利用原有装置提出具体改进方案________。
(3)借助U型玻璃管粗略测定空气中氧气的体积分数,如图3所示,得出空气中氧气体积分数约为五分之一的实验现象是________。
9.(12分)小明对铁的锈蚀进行如下探究.室温时,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,装置如图.观察到量筒内水沿导管慢慢进入广口瓶(净容积为146mL).当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零).记录起始和最终量筒的读数以及所需时间如下表.
序号
样品
量筒起始
读数
量筒最终
所需时间
铁粉、
碳和
滴水
约
碳、
滴水和少量
(1)实验①和②说明
可以________(填“加快”或“减慢”)铁锈蚀的速率.
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是________(填“放热”或“吸热”)过程.
(3)实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是:
________.
(4)实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成.
(5)该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是________
(6)现仅提供:
量筒、大烧杯、玻璃棒、水、滤纸包(内含
),请你帮助小明再设计一个测量空气中氧气体积含量的实验方案,画出实验装置示意图即可(注明滤纸包的位置).
三、综合题(共4题;
共17分)
10.(3分)2017年九江迎来了高铁时代,正在建设的九江南站即九江高铁站,将使九江人民的出行变得更加方便、快捷。
结合所学化学知识,回答下列问题:
(1)动车电路中的导线大多是用铜制的,这是利用了铜的延展性和________,动车使用的金属材料大多数是________(填“纯金属”或“合金”)。
(2)动车表面喷漆除美观外,主要是为了防止外壳与________和________接触而生锈。
(3)铝热剂是修建铁路时常用的焊接材料,其反应原理是在高温下,铝与氧化铁反应得到熔融的铁与一种氧化物,该反应的化学方程式为:
________。
11.(4分)厨房中,蓝藏着很多化学知识:
(1)厨房里用案刀切菜后,发现一段时间后生销了,生锈的原因是铁与________物质反应。
(2)炒菜时油锅中的油不慎着火,可用锅盖盖灭,其灭火原理为________。
(3)蛋白质是构成细胞的基本物质,下列食品中富含蛋白质的是
(填字母序号)。
A.米饭和馒头
B.花生油和大豆油
C.鸡蛋和牛肉
D.水果和蔬菜
(4)厨房中能用来除去水壶中水垢的物质是
A.食醋
B.食盐水
C.食用油
D.洗洁精
12.(6分)回答下列问题。
(1)天然存在的最硬物质是________;
(2)K2CO3、Na2CO3都含________(填离子符号);
(3)CO2与H2O反应,生成一种能使石蕊溶液变红的物质,这种物质是________;
(4)炼铁时高炉内发生如下反应:
,其中________发生氧化反应;
(5)写出甲烷燃烧的化学方程式________;
13.(4分)铁是生产、生活中应用广泛的金属材料。
(1)在酱油中加入铁强化剂,可预防________填(“佝偻病”“贫血”或“骨质疏松“);
(2)某种含铁粉的麦片,食用后在胃酸(盐酸)作用下将铁粉转化为人体可吸收的铁元素,反应的化学方程式为________;
(3)对铁质零件进行“发蓝”处理后,其表面会形成致密氧化膜,从而有效避免腐蚀;
①致密氧化膜能有效阻止铁锈蚀的原因是________;
②为检验“发蓝”处理的铁质零件表面是否形成致密氧化膜,将该零件浸泡于硫酸铜溶液中,发现零件表面出现红色物质,由此可知“发蓝”处理效果不好,因为________(用化学方程式表示)。
(4)某同学对x、银、铜、铁四种金属混合物的成分进行探究,流程如下:
①四种金属的活动性由强到弱的顺序是________;
②固体丙的组成可能是________。
四、计算题(共1题;
共3分)
14.(3分)现有黄铜
合金
与100g稀硫酸在烧杯中恰好完全反应,反应后测得烧杯中剩余物的总质量为
求:
(1)反应生成氢气的质量为多少g。
(2)黄铜中铜的质量为多少克?
参考答案
1-1、
2-1、
3-1、
4-1、
5-1、
6-1、
7-1、
7-2、
7-3、
8-1、
8-2、
8-3、
9-1、
9-2、
9-3、
9-4、
9-5、
9-6、
10-1、
10-2、
10-3、
11-1、
11-2、
11-3、
11-4、
12-1、
12-2、
12-3、
12-4、
12-5、
13-1、
13-2、
13-3、
13-4、
14-1、
14-2、