完整版初中化学综合性试题Word格式文档下载.docx
《完整版初中化学综合性试题Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《完整版初中化学综合性试题Word格式文档下载.docx(24页珍藏版)》请在冰点文库上搜索。
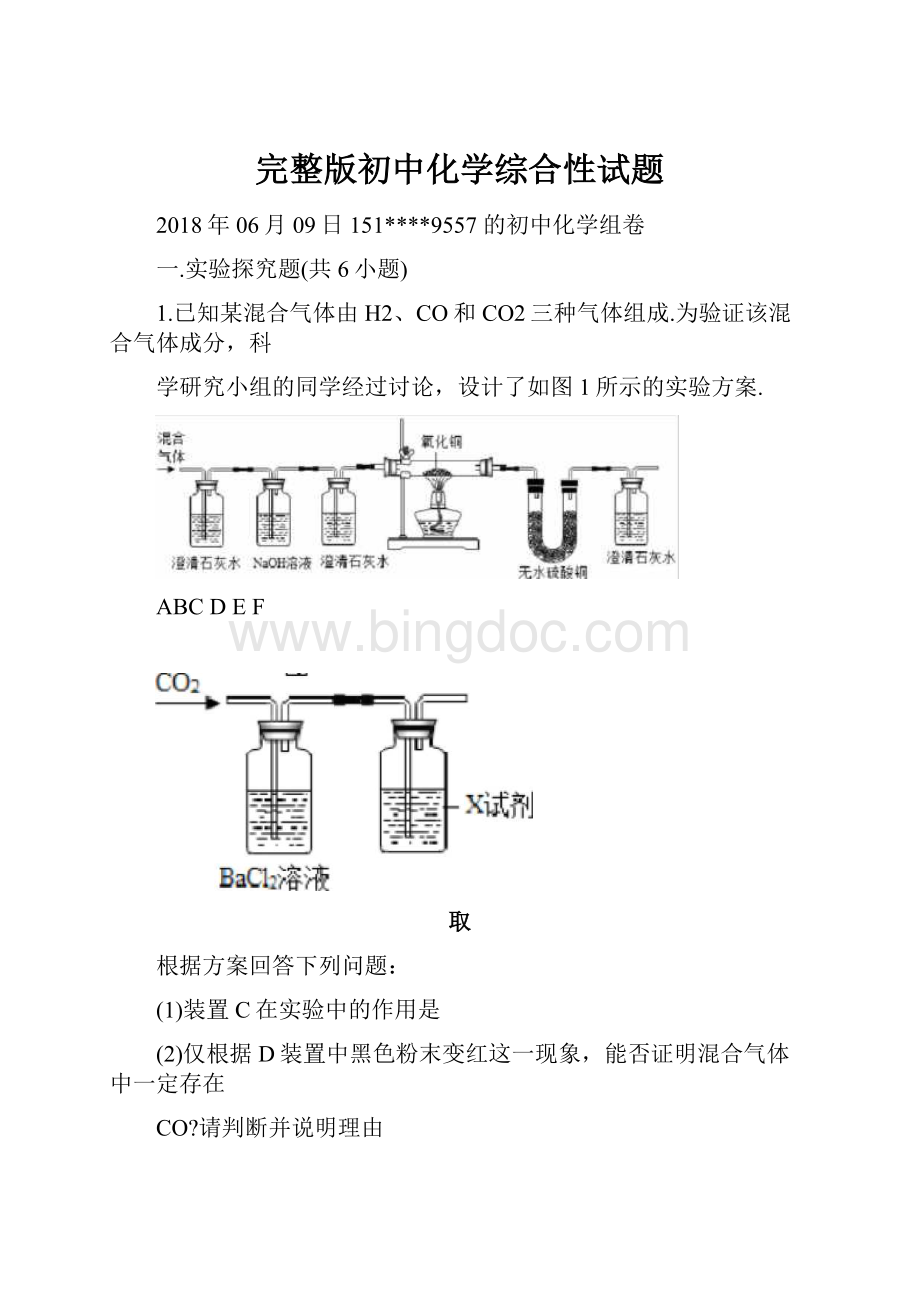
(1)如果NaOH溶液中混有少量的Na2CQ杂质,常加入适量(填物质的化学式),再过滤除去该杂质.
(2)小王、小张通过以上探究分析推出:
实验室里保存Ba(OH)2溶液的方法
应该是.
3.现有2瓶无色且失去标签的碳酸钠溶液和氢氧化钠溶液,如何鉴别,其方案很多.
【提出问题】仅提供氢氧化钙溶液和稀盐酸,能否将碳酸钠溶液和氢氧化钠溶液区别开来?
【猜想假设】将失去标签的两种溶液分别编号为A、B,假设A为碳酸钠溶液,B为氢氧化钠溶液.
【设计思路】现有甲、乙两位同学分别思考得出如下初步鉴别思路:
甲:
将两种溶液取样,分别滴入稀盐酸,根据是否有气泡产生来判断各是哪种溶
液.
乙:
将两种溶液取样,分别滴入氢氧化钙溶液,振荡,根据是否有白色沉淀生成来判断各是哪种溶液.
(1)以上两种思路是否都正确
(填都正确”或幺个正确一个不正确”)
【实验探究】请参与下列实验过程:
(2)请在上述实验思路中选择一个你认为正确的思路(填甲”或乙”)进行实验
(3)填写出实验报告:
实验步骤实验现象结论、化学反应方程式
①将A、B两溶液各取少A溶液样品中有:
则A为溶液
量,分别放入两支试管中;
B为溶液
②反应的化学方程式为:
【发散思维】鉴别碳酸钠溶液和氢氧化钠溶液,还可从下列试剂中选取.请你选择一种能鉴别这两种溶液的试剂(请填写序号)
A.KOHB.Na2SQC.BaC2D.NaCl
4.馒头、面包等发面食品的一个特点是面团中有许多小孔,他们使发面食品松软可口。
小明学习相关化学知识后,将家里制作馒头用的白色粉末带到实验室与兴趣小组的同学一起进行探究。
【初步探究】取少量白色粉末于试管中,加适量水,测得溶液的pH>
7,说明
溶液呈性。
【提出问题】白色粉末成分是什么?
【查阅资料】
(1)碳酸钠、碳酸氢钠都可用于制作发面食品。
(2)碳酸氢钠不稳定,受热易分解生成二氧化碳和水等;
碳酸钠很稳定。
猜想I:
碳酸钠
猜想H:
碳酸氢钠
【实验探究】甲乙兴趣小组设计不同实验方案进行探究。
甲组方案:
如图1,取适量白色粉末于试管中,将导管伸入澄清石灰水,加热,澄清石灰水变浑浊,猜想R正确。
写出装置B中反应的化学方程式
乙组方案:
用如图2所示装置作为反应容器,准确测量生成气体的体积以判断白
色粉末的成分。
分别向盛有碳酸钠、碳酸氢钠和白色粉末的锥形瓶中,注入等体积、等浓度的足
量的稀盐酸,记录如表:
头驳编P
锥形瓶内物质[来源
最终得到CO2
名称
质量/g
体积/mL
①
a
Vi
②
V2
③
白色粉末
m
V3
实验①的化学反应方程式为
;
表中m二
g;
根据上表中数据分
析,猜想R正确,判断的依据是。
【反思应用】
(1)甲组方案中,无法判断白色粉末是否为碳酸钠和碳酸氢钠的混合物;
乙组方案可以判断,如果是两者的混合物,应该满足的条件是。
(2)家中制作馒头、面包时,将面粉发酵(产生有机酸),再加入适量的碳酸氢钠,可以使馒头、面包松软。
原因是。
5.经过监测和治理,我省的土壤质量已经得到了很好的改善,但个别地区仍然存在盐碱地.某校化学兴趣小组的同学们为此开展了实践活动,他们采集了本地的土样,并对土样围绕两个问题进行探究
查阅资料
①枸杞和合欢均可在轻度盐碱地中生存.
②盐碱地显碱性.
③该土样中的可溶性物质只含NaCl,CaC2和NazCQ.
探究过程
(1)甲组探究土样的酸碱度
具体操作是,由此得出,该土样的pH>
7.
(2)乙组探究土样的成分(如图所示)
向土样中加入足量的蒸储水,发生反应的化学方程式.
同学们对溶液I中的溶质成分很感兴趣,作出如下猜想:
猜想①:
猜想②:
猜想③:
设计实验,继续探究:
验证猜想所用试实验现象实验结果
剂
方案一AgNOb溶液和稀硝由白色沉淀生成猜想①正确
酸
方案二无明显现象猜想②不正确
方案三猜想③正确
反思与评价:
①通过交流,甲组认为乙组的方案一不太严谨,理由是.
②同学们对沉淀CaCO的来源展开了热烈的讨论.一致认为CaCO也可能来自
士样本身.请解释土样中存在CaCO的原因
总结与提升:
改良我省的盐碱地,充分利用土地资源,造福山西人民,我们任重而道远.以下
建议你认为正确的是
a,轻度盐碱地可以种植枸杞
b.可以用熟石灰改良盐碱地
c.盐碱地应避免施用碱性化肥.
6.乙快(QH2)气体在空气中燃烧能产生高温火焰(氧快焰),工人师傅常用氧快焰切割或焊接金属。
乙快由碳化钙(化学式为CaC)与水反应生成,同时
生成一种白色固体。
【提出问题】白色固体是什么物质?
【做出猜想】小明经过思考认为有以下几种可能:
猜想一:
CaQ猜想二:
猜想三:
Ca(OH)2
他的依据是。
【交流反思】经过同学们交流讨论,认为猜想一不成立,请用化学方程式说明猜想一不成立的原因。
(一)取少量白色固体放入试管中,滴加稀盐酸至过量,始终没有观察到,证明猜想二不成立。
(二)取少量白色固体加入到水中,取上层清液,滴入溶液,有白色沉淀出现,证明猜想三成立。
【实验结论】白色固体是Ca(OH)2。
【拓展应用】将碳化钙固体放入氯化俊溶液中充分反应后有气体生成,该气体的成分是(写化学式)。
参考答案与试题解析
1.已知某混合气体由H2、CO和CQ三种气体组成.为验证该混合气体成分,科
副
(1)装置C在实验中的作用是检验二氧化碳气体是否除尽
请判断并说明理由不能.H2能与氧化铜反应
若不可靠,请对图1实验装置提出改进意见不可靠,图1实验装置中应在CD之间加一个气体干燥装置
(4)图1方案B装置可用来吸收CQ但没有现象.为证明CQ和NaOH能发生反应,小丁又设计了图2所示的方案.则图2方案中所加试剂X应该是氨
氧化钠和氯化钢.
【解答】解:
(1)根据可用澄清石灰水检验二氧化碳气体知,装置C在实验中的作用是检验二氧化碳气体是否除尽;
(2)在加热条件下,H2、CO均能与氧化铜反应,使D装置中产生黑色粉末变红这一现象,所以仅根据D装置中黑色粉末变红这一现象,不能证明混合气体中一定存在CO;
(3)装置E中出现白色硫酸铜粉末变成蓝色的实验现象,说明有水蒸气进入,
该水蒸气可能是氢气与氧化铜反应产生的,也可能是气体从C中带入的,所
以小丁根据装置E中出现白色硫酸铜粉末变成蓝色的实验现象,得出该混合气体中有氢气存在的结论是不可靠的,图1实验装置中应在CD之间加一个气体干燥装置;
(4)钢离子遇碳酸根离子会产生碳酸钢沉淀,则图2方案中所加试剂X应该是氢氧化钠和氯化钢.
答案:
(1)检验二氧化碳气体是否除尽;
(2)不能,H2能与氧化铜反应;
(3)不可靠,图1实验装置中应在CD之间加一个气体干燥装置;
(4)氢氧化钠和氯化钢.
小王、小张认为NaOH溶液一定变质的理由(用化学方程式表示)2NaOH+CO
一Na2CC3+H2O.
(1)小王设计好方案后,进行了如下实验来验证自己的猜想,请你协助小王完
成实验现象的填写:
①取一定量NaOH溶液样品于试管有白色沉淀产NaOH溶液样品部分变质
中,滴加足量BaC2溶液生
②取经过①反应后的滤液,向其中溶液变成蓝色
滴加紫色石蕊溶液
(2)小张取用小王第①步反应后的滤液,滴加CuC2溶液,有蓝色沉淀产生,证明自己的猜想错误.
(1)如果NaOH溶液中混有少量的N&
CQ杂质,常加入适量Ca(OH)2(填物质的化学式),再过滤除去该杂质.
应该是密封保存.
NaOH溶液一定变质的理由是氢氧化钠能和空气中的二氧化碳反应生成碳酸钠和
水,反应的化学方程式为:
2NaOH+CQ—Na2CC3+H2O.
故填:
2NaOH+CQ—Na2CQ+H2O.
(1)①取一定量NaOH溶液样品于试管中,滴加足量BaC2溶液,说明溶液中含有碳酸钠;
②取经过①反应后的滤液,向其中滴加紫色石蕊溶液,溶液变蓝色,说明溶液中含有氢氧化钠,实验过程如下表所示:
实验步骤现象结论
①取一定量NaOH溶液样品于试管有白色沉淀产生
NaOH溶液样品部分变质
②取经过①反应后的滤液,向其中溶液变成蓝色
(2)小张取用小王第①步反应后的滤液,滴加CuC2溶液,有蓝色沉淀产生,说明溶液中含有氢氧化钠,进一步证明自己的猜想错误.
第9页(共18页)
蓝.
(1)如果NaOH溶液中混有少量的N%CQ杂质,常加入适量的氢氧化钙溶液,再过滤除去该杂质.
Ca(OH)2.
(2)通过以上探究分析推出:
氢氧化钢能和空气中的二氧化碳反应生成碳酸钢沉淀和水,因此实验室里保存Ba(OH)2溶液的方法应该是密封保存.
密封保存.
甲:
将两种溶液取样,分别滴入稀盐酸,根据是否有气泡产生来判断各是哪种溶液.
(1)以上两种思路是否都正确都正确(填都正确”或"
个正确一个不正
确”)
【实验探究】请参与下列实验过程:
(2)请在上述实验思路中选择一个你认为正确的思路
进行实验
①将A、B两溶液各取少量,分别放入两支试管中;
实验现象
A溶液样品中有:
气泡产生
甲(填甲"
或乙”)
结论、化学反应方程式
则A为碳酸钠溶液
B为氮氧化钠溶液反应的化学方程式为:
②向两支试管中分别NaOh+HCLNaC+hhO,
滴加足量稀盐酸Na2CQ+2HCl=2NaC+H2O+C
观察现象02T
【发散思维】鉴别碳酸钠溶液和氢氧化钠溶液,还可从下列试剂中选取.请你选择一种能鉴别这两种溶液的试剂C(请填写序号)
A.KOHB.NazSQC.BaC2D.NaCl
(1)稀盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,和氢氧化钠反应生成氯化钠和水,因此可以将两种溶液取样,分别滴入稀盐酸,根据是否有气泡产生来判断各是哪种溶液;
氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,和氢氧化钠不能反应,因此
可以将两种溶液取样,分别滴入氢氧化钙溶液,振荡,根据是否有白色沉淀生成来判断各是哪种溶液;
由以上分析可知,以上两种思路都正确.
都正确.
(2)选择的正确思路是甲.
甲.
(3)实验报告如下表所示:
B为氢氧化钠溶液
反应的化学方程式为:
NaOH+HCHNaC+H2。
,
Na2C03+2HCl=2NaC+H20+CC2T
可以用氯化钢溶液,这是因为氯
实验步骤实验现象
①将A、B两溶液各取少A溶液中产生气泡
量,分别放入两支试管
中;
②向两支试管中分别滴
加足量稀盐酸,观察
【发散思维】鉴别碳酸钠溶液和氢氧化钠溶液,
化钢和碳酸钠反应生成白色沉淀碳酸钢和氯化钠,不能和氢氧化钠反应.
C.
4.馒头、面包等发面食品的一个特点是面团中有许多小孔,他们使发面食品松
软可口。
小明学习相关化学知识后,将家里制作馒头用的白色粉末带到实验
室与兴趣小组的同学一起进行探究。
溶液呈碱性。
图1即
ntL注射器
写出装置B中反应的化学方程式CO2+Ca
(OH)口:
——CaCQj+H2O。
用如图2所示装置作为反应容器,准确测量生成气体的体积以判断白色粉末的成分。
分别向盛有碳酸钠、碳酸氢钠和白色粉末的锥形瓶中,注入等体积、等浓度的足量的稀盐酸,记录如表:
实验编号
锥形瓶内物质[来源最终得到CO2
名称质量/g体积/mL
碳酸钠aVi
2碳酸氢钠aV2
3白色粉末mV3
实验①的化学反应方程式为NmCQ+2HCI——2NaC+CO2」+H2O;
表中m=
ag;
根据上表中数据分析,猜想R正确,判断的依据是V3=V2。
乙组方案可以判断,如果是两者的混合物,应该满足的条件是V1<
V3<
V20
(2)家中制作馒头、面包时,将面粉发酵(产生有机酸),再加入适量的碳酸氢
钠,可以使馒头、面包松软。
原因是碳酸氢钠与有机酸反应生成二氧化碳
气体,气体在面团中形成许多小气室,使馒头、面包疏松多孔。
【初步探究】
取少量白色粉末于试管中,加适量水,测得溶液的pH>
7,说明溶液呈碱性。
碱。
【实验探究】
装置B中,二氧化碳和氢氧化钙反应生成碳酸钙和水,反应的化学方程式为:
CO2+Ca(OH)2——CaCOj+H2O;
实验①中,碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,反应的化学反应方程式为:
Na2CC3+2HCl——2NaC+CQ"
40;
为了进行对比,表中m=ag;
根据上表中数据分析,如果猜想II正确,则V3=V2o
CQ+Ca(OH)2——CaCOj+H2O;
N&
CQ+2HCI——2NaC+CC2T+H2O;
a;
V3=V2。
(1)碳酸钠、碳酸氢钠和稀盐酸反应的化学方程式及其质量关系为:
Na2CO3+2HCl——2NaC+CO2T+H2O,NaHCQ+HCLNaC+H2O+CO2T,
1064484
44
由以上质量关系可知,相同质量的碳酸钠和碳酸氢钠与足量稀盐酸反应时,碳酸
氢钠生成的二氧化碳多,如果是两者的混合物,应该满足的条件是Vi<
V3V
V
Vl<
V2o
原因是:
碳酸氢钠与有机酸反应生成二氧化碳气体,气体在面团中形成许多小气室,使馒头、面包疏松多孔。
碳酸氢钠与有机酸反应生成二氧化碳气体,气体在面团中形成许多小气室,使馒头、面包疏松多孔。
③该土样中的可溶性物质只含NaCl,CaC2和NmCQ.
具体操作是取土壤样品于烧杯中,加入蒸储水搅拌、静置,用玻璃棒蘸取上层清液7在pH试纸上,将试纸显示颜色与标准比色卡对照,读出pH值,由此得出,该土样的pH>
向土样中加入足量的蒸储水,发生反应的化学方程式N&
CQ+CaC2=CaCOJ+2NaCl.
只有氯化钠
含有氯化钠、氯化钙
含有氯化钠、碳酸钠
AgNO3溶液和稀硝
由白色沉淀生成
猜想①正确
无明显现象
猜想②不正确
碳酸钠溶液
猜想③正确
稀盐酸
有气泡产生
反思与评价:
①通过交流,甲组认为乙组的方案一不太严谨,理由是若溶液中含有氯化钙,
滴加AgNC3溶液和稀硝酸,也会产生白色沉淀.
②同学们对沉淀CaCO的来源展开了热烈的讨论.一致认为CaCO也可能来自士样本身.请解释土样中存在CaCO的原因在灌溉或雨水的作用下、碳酸钠和氯化钙也会反应生成碳酸钙沉淀.
改良我省的盐碱地,充分利用土地资源,造福山西人民,我们任重而道远.以下建议你认为正确的是ac
c,盐碱地应避免施用碱性化肥.
于烧杯中,加入蒸储水搅拌、静置,用玻璃棒蘸取上层清液滴在pH试纸上,
将试纸显示颜色与标准比色卡对照,读出pH值;
(2)氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠,化学方程式为:
Na2CQ+CaC2=CaCOJ+2NaCl;
碳酸钠和氯化钙反应时,两种物质可能恰好完全反应,可能其中的一种物质过量,
所以
只有氯化钠;
含有氯化钠、氯化钙;
含有氯化钠、碳酸钠;
碳酸根离子和钙离子反应会生成碳酸钙沉淀,氢离子和碳酸根离子反应会生成二
验证猜想所用试
方案一AgNOs溶液和稀硝
实验结果
氧化碳气体,所以
反思与评价①氯离子和银离子反应会生成氯化银沉淀,所以通过交流,甲组认
为乙组的方案一不太严谨,理由是:
若溶液中含有氯化钙,滴加AgNO3溶液
和稀硝酸,也会产生白色沉淀;
②碳酸根离子和钙离子反应会生成碳酸钙沉淀,所以解释土样中存在CaCO的
原因:
在灌溉或雨水的作用下,碳酸钠和氯化钙也会反应生成碳酸钙沉淀;
总结与提升盐碱地不能用氢氧化钙进行处理,避免使用碱性化肥,故选ac.
故答案为:
(1)取土壤样品于烧杯中,加入蒸馏水搅拌、静置,用玻璃棒蘸取上
层清液滴在pH试纸上,将试纸显示颜色与标准比色卡对照,读出pH值;
(2)Na2CQ+CaQ=CaCOj+2NaCl;
方案一AgNOs溶液和稀硝由白色沉淀生成猜想①正确
方案二碳酸钠溶液无明显现象猜想②不正确
方案三稀盐酸有气泡产生猜想③正确
反思与评价①若溶液中含有氯化钙,滴加AgNO3溶液和稀硝酸,也会产生白色沉淀;
②在灌溉或雨水的作用下,碳酸钠和氯化钙也会反应生成碳酸钙沉淀;
总结与提升ac.
CaQ猜想二:
CaCO:
他的依据是质量守是定律。
【交流反思】经过同学们交流讨论,认为猜想一不成立,请用化学方程式说明猜想_不成立的原因CaOHH2rCa(OH)2。
(一)取少量白色固体放入试管中,滴加稀盐酸至过量,始终没有观察到气泡放出,证明猜想二不成立。
(二)取少量白色固体加入到水中,取上层清液,滴入碳酸钠溶液、有白色沉淀出现,证明猜想三成立。
【拓展应用】将碳化钙固体放入氯化俊溶液中充分反应后有气体生成,该气体的成分是NH3(写化学式)。
【做出猜想】
依据质量守恒定律;
化学反应前后元素的种类不变,故可以做出的猜想是:
猜想一:
CaO;
猜想二CaCO;
Ca(OH)2;
CaCO;
质量守恒定律;
【交流反思】
经过同学们交流讨论,认为猜想一不成立。
是因为CaO能与水反应生成氢氧化
钙,有水存在,不能有氧化