高考试题化学实验文档格式.docx
《高考试题化学实验文档格式.docx》由会员分享,可在线阅读,更多相关《高考试题化学实验文档格式.docx(19页珍藏版)》请在冰点文库上搜索。
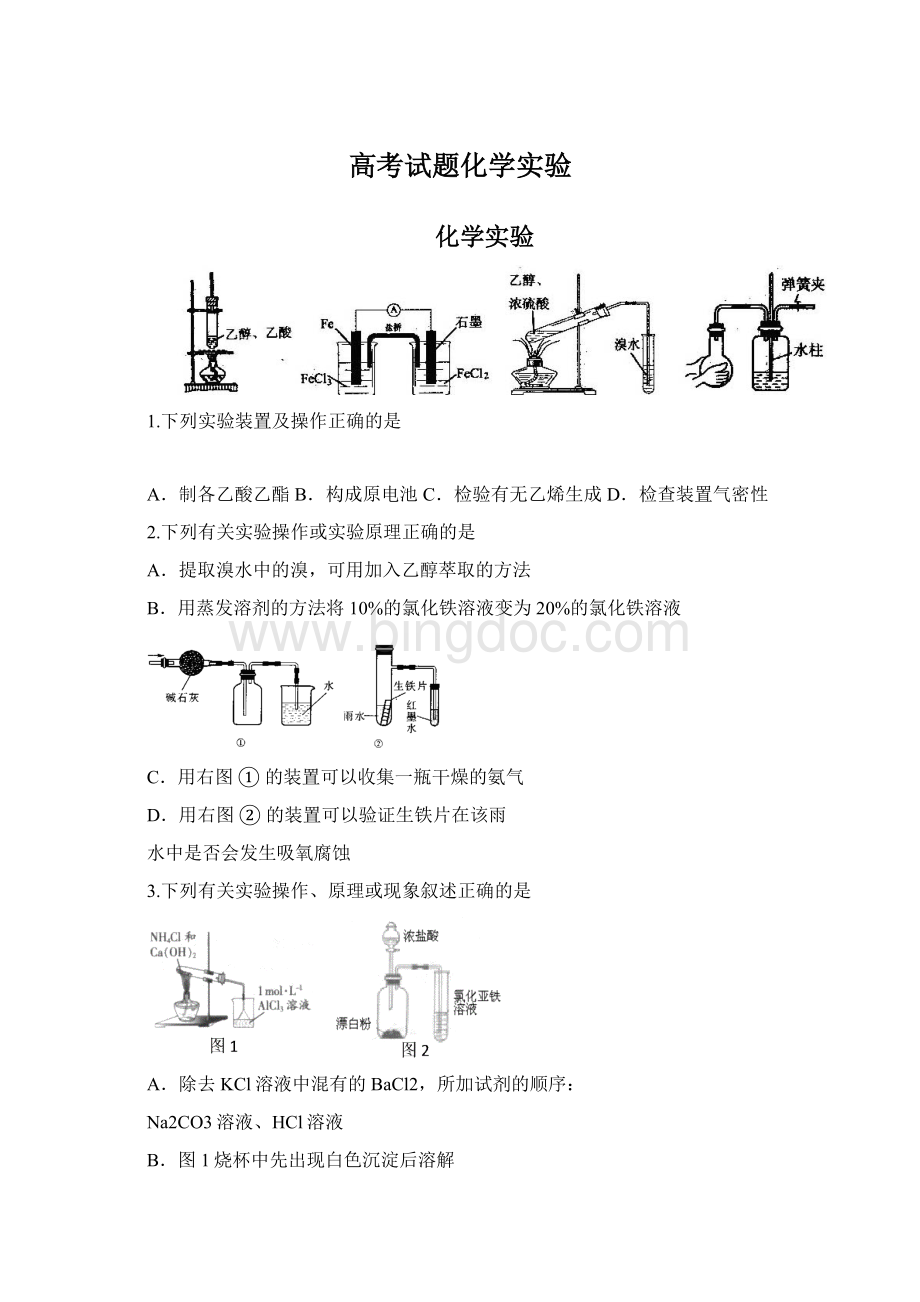
C.某盐焰色反应火焰为黄色,则该盐金属元素一定只有钠元素
D.如右图所示,放置一段时间后,饱和CuSO4溶液中出现蓝色
晶体,说明CaO有一定的脱水性
8.根据下图海水综合利用的工业流程图,判断下列说法正确的是
已知:
MgCl2·
6H2O受热生成Mg(OH)Cl和HCl气体等。
A.过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质
B.在过程③中将MgCl2·
6H2O灼烧即可制得无水MgCl2
C.在过程④、⑥反应中每氧化0.2molBr-需消耗2.24LCl2
D.过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题
9.下列有关实验原理、装置、操作或结论的描述中,不正确的是(有关装置中的夹持仪器略去未画)
10.下列实验方法合理的是
A.用pH试纸检验NH3的性质时,必须先将试纸润湿
B.用明矾可除去中性废水及酸性废水中的悬浮颗粒
C.仅用水即可鉴别苯、四氯化碳、甘油三种无色液体
11.下列物质制备的叙述正确的是()
A.钠在纯氧中燃烧生成Na2O2,在空气中燃烧生成Na2O
B.过量的CO2通入CaCl2溶液中生成可溶性的Ca(HCO3)2
C.在沸水中滴入饱和FeCl3溶液可制备Fe(OH)3胶体
D.在乙酸钠溶液中通入CO2可制备乙酸
12.下列实验不能达到预期目的的是
A.利用Ⅰ制取Fe(OH)2
B.利用Ⅱ装置制取C2H4
C.利用Ⅲ装置进行铜与浓硝酸反应的实验
D.利用Ⅳ装置收集NH3
13
14.为达到对某溶液检验的目的,以下说法正确的是
A.样品得到使湿润蓝色石蕊试纸变红色的气体,说明样品中含NH4+
B.样品无明显现象出现白色沉淀,说明样品中含SO42-
盐酸酸化酸化
C.样品出现白色沉淀,说明样品中含Ag+
D.样品得到使澄清石灰水变浑浊的气体,说明样品中含CO32-或HCO3-
15.实验室一瓶固体M的标签右半部分已被腐蚀,剩余部分只看到“Na2S”字样(如图所示)。
已知,固体M只可能是Na2SO3、Na2SiO3、Na2SO4中的一种。
若取少量固体M配成稀溶液进行有关实验,下列说法错误的是………………………………………………………()
(A)只用盐酸一种试剂就可以确定
该固体M的具体成分
(B)往溶液中通入二氧化碳,若有白色沉淀,则固体M为Na2SiO3
(C)测定溶液的酸碱性,若溶液显中性,则固体M一定是Na2SO4
(D)往溶液中加硝酸酸化的BaCl2,若有沉淀,则固体M为Na2SO4
16、某实验报告记录了如下数据,其中数据合理的是……………………………………()
(A)用pH试纸测得氯水的pH为2.1(B)用50mL量筒量取23.00mL浓盐酸
(C)用温度计测量出酒精的沸点为78.5℃(D)用托盘天平称量氧化铜粉末为11.70g
17.关于下列图示的说法中正确的是()
A.由图①所示实验可得出三种元素的非金属性强弱顺序为:
氯>
碳>
硅
B.图②可用于干燥、收集氯化氢,并吸收多余的氯化氢
C.图③表示可逆反应CO(g)+H
2O(g)
CO2(g)+H2(g)的△H>
D.对反应:
A(s)+2B(g)
xC
(g),根据图④可以求出x=2
18.关于下列各实验装置图的叙述中,正确的是……………………………………()
(A)装置①可用于分离苯和溴苯的混合物
(B)装置②可用于吸收HCl或NH3气体
(C)装置③可用于分解NH4Cl制备NH3
(D)装置④b口进气可收集CO2或NO气体
19.关于图中各装置的叙述不正确的是
A.装置①是中和滴定法测定硫酸的物质的量浓度
B.装置②中手捂烧瓶(橡胶管已被弹簧夹夹紧),发现导管中有液柱上升并保持稳定,则说明装置不漏气
C.装置③中X若为四氯化碳,可用于吸收氨气,并防止倒吸
D.装置④可检验溴乙烷发生消去反应得到的气体中含有乙烯(假定每个装置中吸收完全)
20.关于下列各实验装置的叙述中,不正确的是()
A.装置①中X若为CCl4,可用于吸收NH3或HC1,并防止倒吸
B.装置②可用于收集H2、NH3、CO2、Cl2、HC1、NO2等气体
C.装置③可用于分离C2H5OH和H2O的混合物
D.装置④可用于干燥、收集NH3,并吸收多余的NH3
21.下列说法正确的是()
A.不用其他试剂无法鉴别下列四种溶液:
Na2CO3、Al2(SO4)3、NaCl、NaHSO4
B.可以用分液漏斗分离下列三组液态混合物:
硝基苯和水、油酸和水、乙酸乙酯和乙醇
C.在由水电离出的c(H+)=1×
10-14mol/L的溶液中可以大量存在Na+、K+、NO3-、HCO3-
D.实验室保存少量液溴和白磷常用水封
22.下列实验装置设计正确且能达到目的的是
测定乙醇结构式滴定法测定硫酸合成氨并检验氨的生成 碘的CCl4溶液中分离I2
的物质的量的浓度并回收CCl4
ABCD
23.根据下列实验事实,得出的结论正确的是()
A.某试液
无明显现象
有红棕色气体放出,说明原试液中不含有NO
,加入浓硫酸后生成NO
B.某试液
有红褐色沉淀生成
沉淀溶解,溶液呈紫色,
则说明原试液中可能含有
C.某试液
产生黄色沉淀,证明原试液中一定含I-
D.某试液
溶液显红色,证明原试液一定是碱溶液
24.下列对实验现象或结论的预测正确的是
A.向苯酚钠溶液中通入CO2,溶液变浑浊,继续通入CO2至过量,又变澄清
B.向NaOH溶液中通入足量CO2,再加入少量Ba(OH)2溶液,CO32-浓度增大
C.向NaAlO2溶液中通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失
D.向银氨溶液中滴加盐酸至过量,开始有沉淀出现,后来沉淀又溶解
25.下列有关实验的叙述中,正确的是
A.用氨水不能鉴别Al(NO3)3、AgNO3、KNO3三种溶液
B.右图所示的装置可用于干燥、收集并吸收多余的氨气
C.少量的CO2通入苯酚钠溶液中生成NaHCO3,说明酸性:
H2CO3>C6H5OH>HCO3—
D.淀粉和稀H2SO4混合加热后,再加新制的Cu(OH)2悬浊液加热至沸腾,无砖红色固体生成,说明淀粉没有水解
26.下列实验原理、装置、试剂选用、结论正确的是
A.用湿润的pH试纸测定稀盐酸的pH
B.用下图1构成锌—铜原电池
C.用下图2根据有关实验现象推知酸性:
CH3COOH>
H2CO3>
C6H5OH
D.用下图3验证溴乙烷发生消去反应生成烯烃
图1图2图3
27.下列实验方案正确且能达到相应实验预期目的的是()
①② ③ ④
A.①制取少量蒸馏水B.②用铜和浓硝酸制取少量NO2
C.③比较MnO2、Cl2、I2的氧化性D.④探究NaHCO3的热稳定性
28.下列实验能达到预期目的的是
①用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸;
②用NaOH溶液除去苯中的少量苯酚;
③用饱和NaHCO3溶液除去CO2中的少量SO2;
④用加热的方法提取NH4Cl固体中混有的少量碘;
⑤用酒精萃取碘水中的碘;
⑥用米汤检验食用加碘盐中含碘;
⑦用溴水鉴别直馏汽油与裂化汽油。
A.①⑤⑦B.②③⑦C.①②④⑤D.②③⑤⑥
29.下列原理或操作的说法正确的是
A.取某试样溶液少量,加入苯酚,同时再加入氯水,若溶液显紫色,说明原试样中含Fe2+
B.排除碱式滴定管尖嘴部分气泡的方法是弯曲乳胶管,让尖嘴略朝上,挤捏乳胶管
C.硫酸亚铁铵晶体制备实验的最后一步是将溶液蒸发到有大量晶体析出,用余热蒸干即可得产物
D.实验室制酚醛树脂的方法是:
将适量反应物放入一支试管中,振荡、摇匀后,塞紧橡胶塞,水浴加热数分钟
30.下列与实验相关的叙述正确的是
A.从碘水中提取单质碘时,可用无水乙醇代替CCl4
B.用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸
C.酸碱滴定时,若加入待测液前用待测液润洗锥形瓶,将导致测定结果偏高
D.检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸
31.下列装置或操作能达到实验目的的是
水
A
Na2CO3
NaHCO3
CCl4
澄清石灰水
盐桥
Zn
Cu
100mL
容量瓶
ZnSO4
CuSO4
A.分离水和CCl4B.定容C.比较两种盐的热稳定性D.构成铜锌原电池
32.关于下列各装置图的叙述中,正确的是()
①②③④
A.实验室用装置①制取氨气
B.装置②中X若为四氯化碳,可用于吸收氨气,并防止倒吸
C.装置③可用于制备氢氧化亚铁并观察其颜色
D.装置④是原电池,锌电极为阴极,发生氧化反应
33.关于下列图示的说法中正确的是()
A.图①表示可逆反应“CO(g)+H2O(g)
CO2(g)+H2(g)”中的△H大于0
B.图②为电解硫酸铜溶液的装置,一定时间内两电极产生单质的物质的量之比一定为1:
1
C.图③实验装置可完成比较乙酸、碳酸、苯酚酸性强弱的实验
D.图④量取0.10mol·
L—1KOH20.00mL
34.下列操作或判断正确的是
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中溶液变浑浊,一定是
B.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有
C.向AlCl3溶液中加入氨水产生白色沉淀,继续滴加至过量沉淀溶解
D.加入氢氧化钠溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,一定有
35.下图所示的实验方法、装置或操作中正确的是()
A.干燥SO2B.实验室制取并收集O2C.装置气密性的检查D.吸收氨气
D.用KMnO4酸性溶液鉴别CH3CH2CH2OH和CH3CH2CHO
36.下列实验现象所对应的离子方程式不正确的是
实验
现象
离子方程式
KI淀粉溶液
H2SO4
在空气中放置一段时间后,溶液呈蓝色
4H++4I-+O2==2I2+2H2O
滴加KSCN的
FeSO4溶液
B
Cl2水
溶液由浅绿色变为
红色
2Fe2++Cl2==2Fe3++2Cl-
Fe3++3SCN-==Fe(SCN)3
C
NaOH溶液
溶液由黄绿色变为
无色
Cl2+2OH-==Cl-+ClO-+H2O
D
加有酚酞的
Ba(OH)2溶液
有白色沉淀生成
溶液由红色变为无色
Ba2++OH-+H++SO42-==BaSO4↓+H2O
37.下列实验的解释或结论不正确的是
选项
实验
解释或结论
用激光笔照射水玻璃溶液,有丁达尔现象
SiO32-水解生成硅酸胶体
在新制的氯水中加入碳酸钙粉末,充分搅拌
氯水中HCLO的物质的量增加
向包有Na2O2的脱脂棉滴少量水,脱脂棉燃烧
Na2O2与H2O反应放热并有O2生成
向某溶液中加入稀盐酸,再加入硝酸钡溶液生
成白色沉淀
原溶液中一定存在SO42-
38下表中实验操作能达到实验目的的是()
实验操作
实验目的
A
向过量的苯酚溶液中加入少量的溴水
观察坐成的白色沉淀三溴苯酚
向甲酸钠溶液中加新制的Cu(OH)2并加热
确定甲酸钠中含有醛基
向酒精和醋酸的混合溶液中加入金属钠
确定酒精中混有醋酸
将溴乙烷与氢氧化钠溶液共热一段时间,再向冷却后的混合液中滴加硝酸银溶液
检验水解产物中的溴离子
39.下列推断正确的是
事实
结论
常温下铁、铜均不溶于浓硫酸
常温下铁、铜与浓硫酸均不反应
HCl与Na2CO3溶液反应生成CO2
可用饱和Na2CO3溶液除去CO2中的少量HCl
氧化铜高温下生成红色物质,该物质可与稀硫酸反应
氧化铜高温下可分解生成Cu2O
稀、浓NHO3分别与铜反应,还原产物为NO和NO2
稀HNO3氧化性比浓HNO3强
40.下述实验不能达到预期目的的是()
编号
实验内容
实验目的
将SO2通入酸性KMnO4溶液中
证明SO2具有漂白性
将Cl2通入NaBr溶液中,然后加入CCl4,振荡、静置
比较氯与溴的氧化性强弱
将铜片分别与浓、稀硝酸反应
探究浓、稀硝酸氧化性的相对强弱
向盛有20g蔗糖的烧杯中加入几滴水,搅拌均匀。
再加入少许浓硫酸,迅速搅拌。
探究浓硫酸的脱水性
41.下列实验不能达到预期目的的是
序号
实验操作
Cl2、Br2分别与H2反应
比较氯、溴的非金属性强弱
MgCl2、AlCl3溶液中分别通入NH3
比较镁、铝的金属性强弱
测定Na2CO3、Na2SO4两溶液的pH
比较碳、硫的非金属性强弱
用同一电路测定等浓度的盐酸、醋酸两溶液的导电性
比较盐酸、醋酸的酸性强弱
42.下列各组解释合理的是
物质的检验、制备和用途及实验现象
解释
在一定浓度的乙酸溶液中加入少量乙酸钠固体,溶液pH增大
完全是由于乙酸根水解所致
向少量未知溶液中滴加氯化钡溶液,有白色沉淀生成
该溶液中一定含有SO2-4
常温下可用铁或铝制容器来盛装浓硫酸或浓硝酸
铁、铝表面发生了钝化现象
向饱和NaCl溶液中通入足量的NH3和CO2,有NaHCO3固体析出
NaHCO3是难溶于水的盐
43.下列实验操作、现象与实验结论一致的是
实验操作、现象
实验结论
向某溶液中加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸沉淀不消失
该溶液中有SO42-
甲苯中滴入少量浓溴水,振荡,静置,溴水层褪色
甲苯与溴发生了取代反应
将FeCl3溶液分别滴入NaBr、NaI溶液中,再分别滴加CCl4,振荡,静置
氧化性:
Fe3+>Br2>I2
除锈的铁钉在浓硝酸中浸泡后,用蒸馏水洗净,再放入CuSO4溶液中无现象
铁钉表面形成了一层致密稳定的氧化膜
44.下列实验操作、强验现象及解释与结论都正确的是
实验现象
解释与结论
将乙醇与浓硫酸共热至l700C,所得气体通入酸性KMn04溶液中
KMn04溶液褪色
乙醇发生消去反应,气体中只有乙烯
淀粉溶液和稀H2S04混合加热,加新制Cu(oH)2悬浊液加热至沸腾
有砖红色沉淀产生
淀粉发生水解,产物有还原性
向甲苯中滴入适量浓溴水,振荡,静置
溶液上层呈橙红
色,下层几乎无色
甲苯和溴发生取代反应,使溴水褪色
向蔗糖中加入浓硫酸
放热,变黑膨胀,有
刺激性气味
浓硫酸有脱水陛和强氧化性,生成c、S02和C02等
45.下列实验操作与预期实验目的或所得实验结论正确的是
实验目的或结论
向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成
该溶液中不一定含有SO42-
用洁净的Pt蘸取某溶液进行焰色反应,火焰呈黄色
该溶液中一定含有Na+,无k+
将CH3CH2Br与NaOH溶液混合加热,再滴加AgNO3溶液,未产生浅黄色沉淀
CH3CH2Br未发生水解
将打磨过的Al片投到一定浓度的CuCl2溶液,出现气泡并有固体生成,过滤,向固体中加入过量的氨水,固体部分溶解
Al与CuCl2溶液反应,生成了H2和Cu(OH)2
根据下列实验现象,所得结论正确的是
序
号
实
验
现
象
悬浊液由白色变为浅黄色
生成白色胶状沉淀
左边棉球变为橙色,右边棉球变为蓝色
锥形瓶中有气体产生,烧杯中液体变浑浊
结
论
溶解性:
AgBr>AgCl
同浓度溶液的pH:
NaAlO2>NaHCO3
Cl2>Br2>I2
非金属性:
Cl>C>Si