四川省成都七中届高三化学零诊模拟Word格式.docx
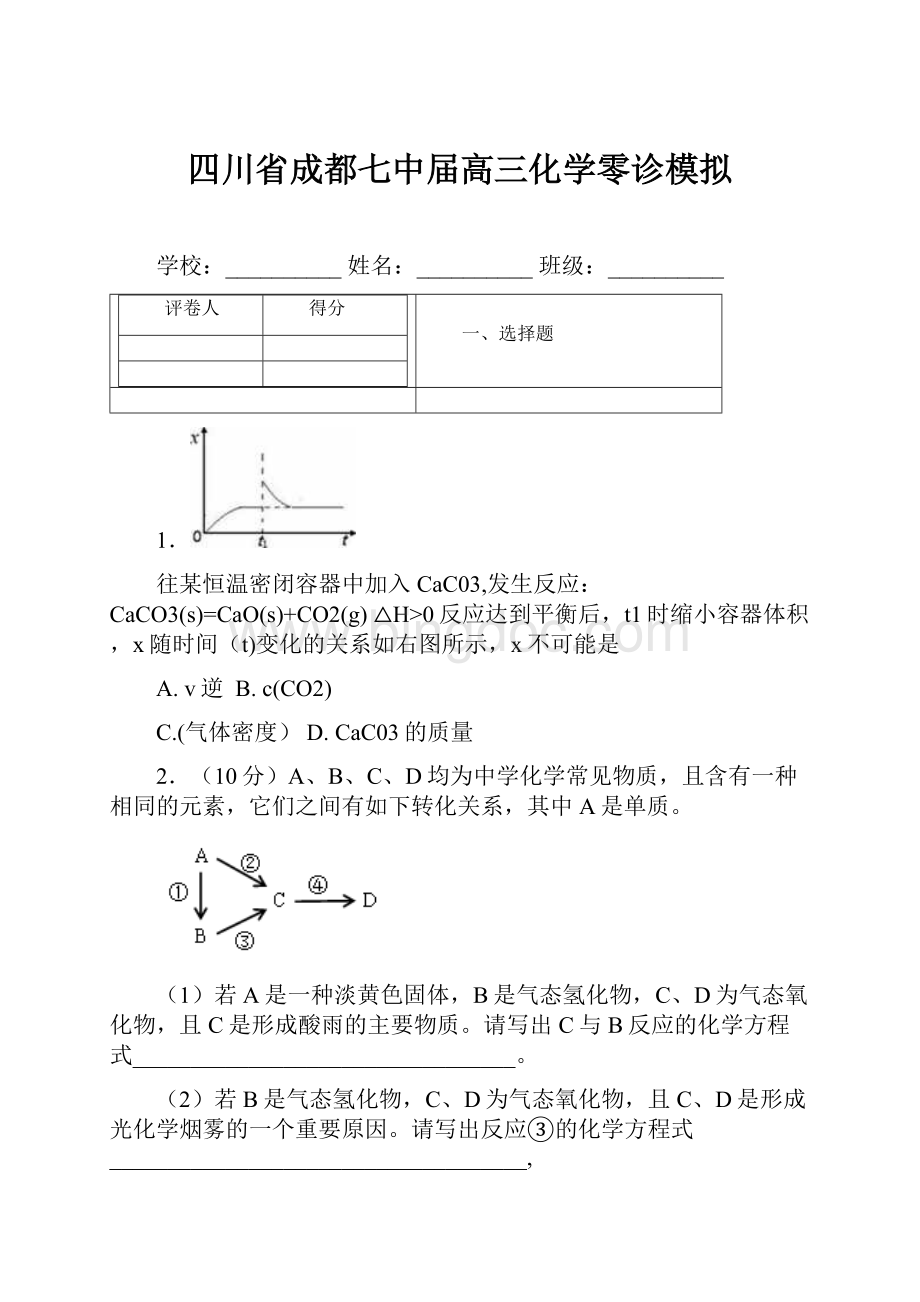
《四川省成都七中届高三化学零诊模拟Word格式.docx》由会员分享,可在线阅读,更多相关《四川省成都七中届高三化学零诊模拟Word格式.docx(11页珍藏版)》请在冰点文库上搜索。
(2)若B是气态氢化物,C、D为气态氧化物,且C、D是形成光化学烟雾的一个重要原因。
请写出反应③的化学方程式____________________________________,
实验室中检验气体B存在用的试剂或用品为________________。
(3)若B、D既能溶于强酸溶液,又能溶于强碱溶液,反应②③均需要强碱性溶液,反应④可以通过滴加少量稀盐酸实现。
据此判断A元素在周期表中的位置是_________________,请写出②的离子方程式_____________________________________。
(4)若C是一种淡黄色固体,常用于吸吸面具中的供氧剂,D是一种强碱。
写出反应④的离子方程式_____________________________。
3.根据下列实验中的操作,对应的现象以及结论都正确的是(
)
选项
操作
现象
结论
A
向NaAlO2溶液中滴加NaHCO3溶液
产生白色沉淀
结合H+的能力比
强
B
蘸有浓氨水的玻璃捧靠近X
有白烟产生
X—定是浓盐酸
C
将气体分别通入溴水和酸性高锰酸钾溶液中
两溶液均褪色
该气体一定是乙烯
D
炭粉中加入浓硫酸并加热,导出的气体通入
BaCl2溶液中
有白色沉淀产生
有SO2和CO2产生
A.A
B.B
C.C
D.D
答案
4.下列说法正确的是()
A.HF比HCl稳定是因为HF间能形成氢键
B.相对分子质量越大范德华力越大,所以NH3、PH3、AsH3、SbH3
沸点逐渐升高
C.铜元素的焰色反应为绿色,该现象与电子的跃迁有关
D.标况下,22.4LHF含有分子数为NA(NA代表阿弗加德罗常数)
5.核黄素又称为维生素B2,可促进发育和细胞再生,有利于增进视力,减轻眼睛疲劳。
核黄素分子的结构如图。
有关核黄素的下列说法中,不正确的是()
A.该有机物的分子式为C17H21N4O6
B.酸性条件下加热水解,有CO2生成
C.酸性条件下加热水解,所得溶液加碱后有NH3生成
D.该化合物能发生酯化反应
6.某研究小组以甲苯为主要原料,采用以下路线合成医药中间体F和Y。
已知:
①
②
③CH3COOH+CH3COOH→(CH3CO)2O+H2O
请回答下列问题:
(1)下列有关F的说法正确的是______________。
A.分子式是C7H7NO2BrB.F即能与HCl又能与NaOH应生成盐
C.能发生取代反应和缩聚反应D.1mol的F最多可以和2molNaOH反应
(2)C→D的反应类型是_____。
(3)在合成F的过程中,B→C步骤不能省略,理由是_____________________。
(4)D→E反应所需的试剂是___________________。
(5)写出同时符合下列条件的A的同分异构体的结构简式(写出其中1个)_________________。
①苯环上只有两种不同化学环境的氢原子②分子中含有-CHO
(6)利用已知信息,以X和乙烯为原料可合成Y,请设计合成路线(无机试剂及溶剂任选)。
___________注:
合成路线的书写格式参照如下示例流程图:
7.以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的过程如图所示。
下列叙述不正确的是()
A.过程Ⅰ中的能量转化形式是太阳能→化学能
B.过程Ⅰ中每消耗116gFe3O4转移2mol电子
C.过程Ⅱ的化学方程式为3FeO+H2O
Fe3O4+H2↑
D.铁氧化合物循环制H2具有节约能源、产物易分离等优点
8.下列说法正确的
A.用溴水能鉴别CH3CH==CHCH2OH和CH3CH2CH2CHO
B.用如图所示方法可保护钢闸门不被腐蚀
C.根据核磁共振氢谱不能鉴别1�溴丙烷和2�溴丙烷
D.食用花生油和鸡蛋清都能发生水解反应
9.电动汽车以锂电池提供动力,锂电池技术已经成为汽车研究的前沿科技某锂电池的电池反应为:
xLi+Li3-xNiCoMnO6
Li3NiCoMnO6,下列说法正确的是
A.该电池的充、放电过程互为可逆反应
B.放电时,电池的负极反应为Li-e-=Li+
C.放电过程中,Li+向电池的负极移动
D.该电池可以采用醋酸、乙醇等作为电解质溶液
10.下列说法不正确的是
A.氯化钠可用于配制生理盐水B.二氧化硅可用于制造玻璃
C.海水中的钠元素以单质存在D.氧化镁(熔点2800℃)是优良的耐高温材料
【参考答案】***试卷处理标记,请不要删除
1.无
2.H
解析:
(10分)
(1)2H2S+SO2=3S+2H2O(2分)
(2)4NH3+5O2
4NO+6H2O(2分)湿润的红色石蕊试纸(1分)
(3)第三周期第ⅢA族(1分)2Al+2OH-+2H2O=AlO2-+3H2↑(2分)
(4)2Na2O2+2H2O=4Na++4OH-+O2↑(2分)
3.A
4.C
【解析】
A.HF比HCl稳定是因为F元素的非金属性强,H—F键的键能很大、不易断裂,A不正确;
B.对于组成和结构相似的分子,如果分子间不能形成氢键,则相对分子质量越大范德华力越大,其沸点越高,但是NH3分子之间可以形成氢键,而PH3、AsH3、SbH3等分子是不能形成氢键,氢键比范德化力要强得多,B不正确;
C.铜元素的焰色反应为绿色,该现象与电子在不同能级之间的跃迁有关,C正确;
D.标况下,HF是液体,故无法根据气体摩尔体积计算22.4LHF的物质的量,也无法计算其含有的分子数,D不正确。
本题选C。
5.A
【分析】
根据键线式的特点和碳原子的四价理论知该化合物的分子式是C17H20N4O6,分子中含有的官能团为肽键、羟基等,能发生水解反应、酯化反应等。
【详解】A项、根据键线式的特点和碳原子的四价理论知该化合物的分子式是C17H20N4O6,故A错误;
B项、由结构式可以知该化合物中含有肽键,因此可以发生水解反应,由已知条件可知水解产物有碳酸即水和二氧化碳生成,故B正确;
C项、由结构式可以知该化合物中含有肽键,因此可以发生水解反应,由已知条件可知水解产物有氨气生成,故C正确;
D项、因
该化合物中含有醇羟基,因此可以发生酯化反应,故D正确。
故选A。
【点睛】本题考查有机物的结构与性质,侧重分析与应用能力的考查,注意把握有机物的结构与题给信息分析为解答的关键。
不定项选择题:
本题包括5小题,每小题4分,共计20分。
每小题只有一个或两个选项符合题意。
6.B
(1).BC
(2).氧化反应(3).氨基易被氧化,在氧化反应之前需先保护氨基(4).Br2/FeBr3或Br2/Fe(5).
(6).
由甲苯与A的分子式,结合D的结构简式可知甲苯发生甲基对位的硝化反应生成A,则A为
,A发生信息中反应,硝基被还原为氨基生成B,则B的结构简式为
,结合D的结构可知,B中氨基中1个H原子被取代生成C为
,C被酸性高锰酸钾溶液氧化生成D,对比D、F的结构可知,D与液溴发生取代反应生成E为
,E发生水解反应得到F,可知B→C是为了保护氨基不被氧化,则
(1)A.根据F的结构简式,可知其分子式应为C7H6NO2Br,A错误;
B.F中有氨基与羧基,可以形成内盐,B正确;
C.F中有羧基、溴原子,可以发生取代反应,F中有氨基与羧基,可以发生缩聚反应,C正确;
D.羧基能与氢氧化钠反应,苯环上的溴原子发生水解反应生成酚羟基,所以1molF最多能和3molNaOH反应,D错误,答案选BC;
(2)C→D是C中甲基被酸性高锰酸钾溶液氧化生成-COOH,属于氧化反应;
(3)由于在合成F的过程中,氨基易被氧化,在氧化反应之前需先保护氨基,因此B→C步骤不能省略;
(4)D→E苯环上氢原子被-Br原子取代,反应所需的试剂是:
液溴、Fe;
(5)同时符合下列条件的A的同分异构体:
①苯环上只有两种不同化学环境的氢原子②分子中含有-CHO,符合条件的同分异构体有
、
;
(6)由信息可知,苯甲醛与乙醛在碱性条件下得到
,再发生消去反应得到
,乙烯发生加成反应生成乙醇,乙醇催化氧化得到乙醛,以苯甲醛和乙烯为原料合成Y的路线流程图为
。
7.B
【详解】A.过程Ⅰ利用太阳能将四氧化三铁转化为氧气和氧化亚铁,实现的能量转化形式是太阳能→化学能,选项A正确;
B.过程Ⅰ中四氧化三铁转化为氧气和氧化亚铁,每消耗116gFe3O4,即0.5mol,
Fe由+3价变为+2价,转移
mol电子,选项B错误;
C.过程Ⅱ实现了氧化亚铁与水反应生成四氧化三铁和氢气的转化,反应的化学方程式为3FeO+H2O
Fe3O4+H2↑,选项C正确;
D.根据流程信息可知,铁氧化合物循环制H2具有节约能源、产物易分离等优点,选项D正确。
答案选B。
8.D
【详解】A.CH3CH==CHCH2OH中有碳碳双键和Br2发生加成反应,溴水褪色,CH3CH2CH2CHO中含有醛基,溴水能把醛基氧化成羧基,溴水褪色,故A错误;
B.保护钢闸门不被腐蚀,应让钢闸门作原电池的正极或电解池的阴极,而此图中钢闸门做了原电池的负极,腐蚀速率会加快,故B错误;
C.1�溴丙烷和2�溴丙烷分别有3种、2种位置的H,能用核磁共振氢谱鉴别1�溴丙烷和2�溴丙烷,故C错误;
D.食用花生油成分是油脂,鸡蛋清成分是蛋白质,油脂水解生成高级脂肪酸和甘油,蛋白质水解生成氨基酸,故D正确。
故选D。
9.B
分析:
可充电电池的构成条件和工作原理都与原电池的相似,只是从物质的角度而言可逆向进行,但进行的条件不同,具此可解答如下。
A、对电池充电是在外接电源的情况下,使其逆向进行,而放电是在没有外接电源的情况下自发进行的,二者进行的条件不同,充、放电也不是同时发生的,所以二者不是可逆反应,故A错误;
B、原电池放电时,较活泼的电极或易失电子的物质作负极,发生氧化反应,所以该电池放电时的负极反应为Li-e-=Li+,故B正确;
C、原电池放电过程中,电池内部的阳离子向正极移动,阴离子向负极移动,所以Li+向电池的正极移动,故C错误;
D、醋酸能与金属Li反应,而乙醇是非电解质,所以该电池不能用醋酸、乙醇作电解质溶液,故D错误。
本题答案为B。
点睛:
正确理解可逆反应的含义是解答本题的关键,强调相同的条件,正逆反应同时进行才是可逆反应。
10.C