化学山西大学附属中学学年高一上学期月考试题解析版Word下载.docx
《化学山西大学附属中学学年高一上学期月考试题解析版Word下载.docx》由会员分享,可在线阅读,更多相关《化学山西大学附属中学学年高一上学期月考试题解析版Word下载.docx(14页珍藏版)》请在冰点文库上搜索。
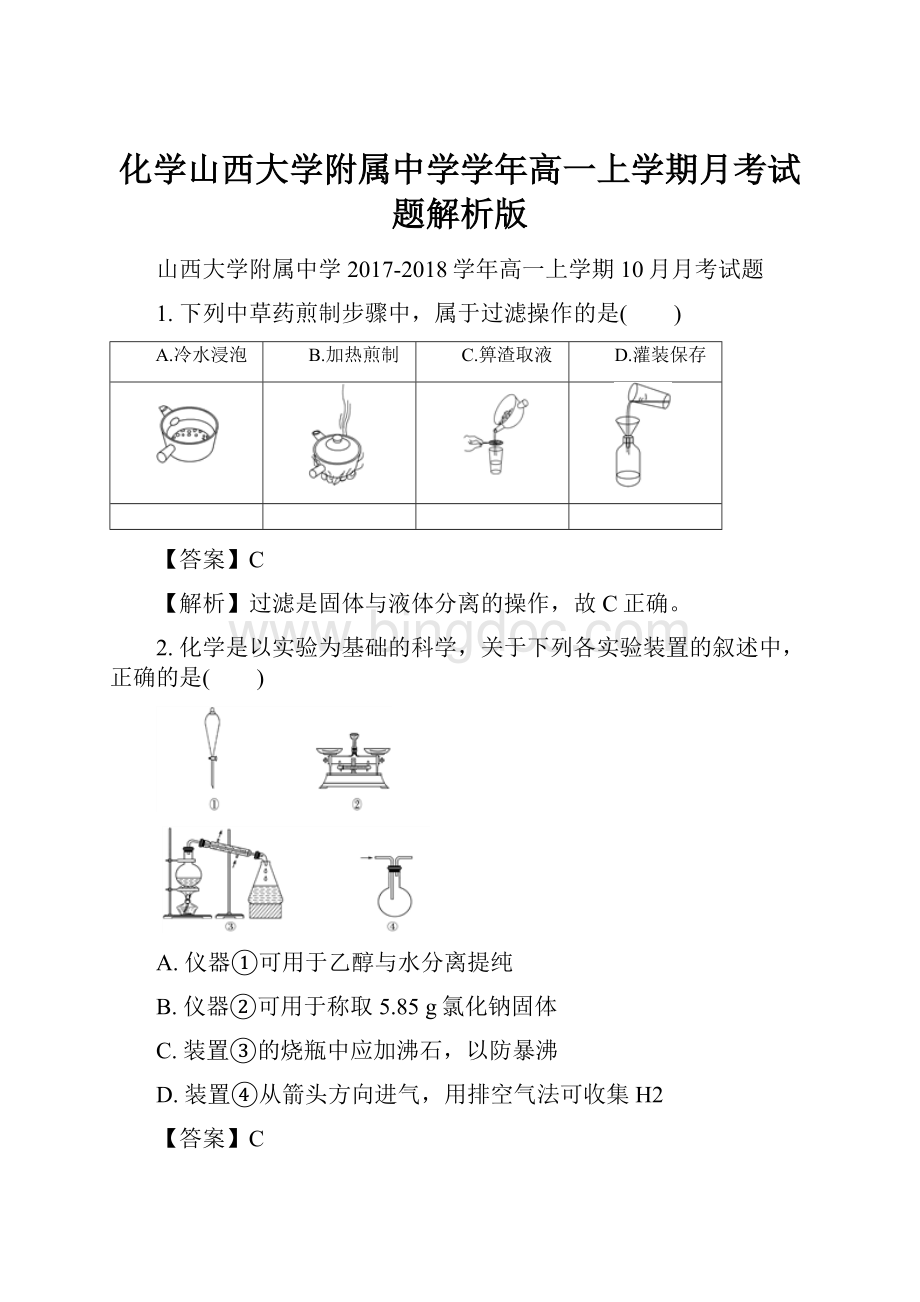
B
分液:
分液漏斗中的液体难以滴下
没有打开分液漏斗活塞,或玻璃塞上凹槽与漏斗口侧面的小孔没有对准
C
蒸馏:
冷凝管破裂
冷凝管没有通水或先加热后通水
D
萃取:
液体静置不分层
加入萃取剂的量较多
【答案】D
4.如图所示的实验操作中,正确的是( )
【答案】A
【解析】A.加入少量水,盖好盖子,将容量瓶倒置,看是否有水渗出.再将瓶塞子旋转180度,再次将容量瓶倒立,故A正确;
B.给试管中的液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试管容积的
,故B错误;
C.用胶头滴管向试管中滴加液体时,不应伸到试管内,应竖直、悬空正放,故C错误;
D.漏斗下端应紧靠烧杯内壁,故D错误;
故选A。
5.下列说法正确的是( )
A.SO2的摩尔质量为64g
B.气体的摩尔体积约为22.4L·
mol-1
C.12g12C中所含碳原子数即为阿伏加德罗常数
D.4gNaOH溶于1L水所得溶液的物质的量浓度为0.1mol·
L-1
【解析】A.SO2的摩尔质量为64g/mol,A错误;
B.标准状况下气体的摩尔体积约为22.4L·
mol-1,B错误;
C.0.012kg12C中所含有的碳原子数即为阿伏加德罗常数,C正确;
D.所得溶液的体积不是1L,不能计算物质的量浓度,D错误,答案选C。
6.如图两瓶体积相等的气体,在同温同压时瓶内气体的关系一定正确的是( )
A.所含原子数相等B.气体密度相等
C.所含质子数相等D.摩尔质量相等
【解析】在同温同压下,两瓶体积相等的气体,其分子数相同。
由于两瓶中的气体都是双原子分子组成的气体,所以其原子数也相同。
由于不知道氮气和氧气的比例如何,所以无法判断两瓶气体的质子数、密度、摩尔质量是否相等。
瓶内气体的关系一定正确的是A,本题选A。
7.下列各物质含少量杂质,除去这些杂质应选用的试剂或操作方法正确的是( )
序号
物质
杂质
除杂应选用的试剂或操作方法
①
KNO3溶液
KOH
加入FeCl3溶液,并过滤
②
FeSO4溶液
CuSO4
加入过量铁粉,并过滤
③
H2
CO2
通过盛NaOH溶液的洗气瓶,再通过盛有浓硫酸的洗气瓶
④
NaNO3固体
CaCO3
溶解、过滤、蒸发
A.①②③④B.①③④C.②③④D.①②③
【解析】KNO3溶液中含有少量KOH,应加入适量的稀硝酸调节溶液的pH=7,用氯化铁除杂会引入杂质,①不正确;
FeSO4溶液中含有少量CuSO4,加入过量铁粉可以把铜置换出来,过滤除去铜和过量铁粉,②正确;
H2含有中少量CO2,通过盛NaOH溶液的洗气瓶除去CO2,再通过盛有浓硫酸的洗气瓶干燥,③正确;
NaNO3固体中含有少量CaCO3,NaNO3可溶而CaCO3不可溶,溶解、过滤、蒸发可以除去杂质并得到纯净的NaNO3固体,④正确。
综上所述,C正确,本题选C。
8.给出下列条件,无法确定该物质摩尔质量的是( )
A.已知气体在标准状况时的密度B.已知物质的体积和质量
C.已知一定量物质的质量和物质的量D.已知物质一个分子的实际质量
【答案】B
A.标况下,气体摩尔体积是22.4L/mol,公式ρ=M/Vm中,密度和气体摩尔体积已知,所以能计算出其摩尔质量,故A不选。
B.公式M="
m/V"
Vm中,已知物质的体积和质量,如果不知气体摩尔体积,无法计算其摩尔质量,故B无法确定。
C.由公式M=m/n可知,质量和物质的量为已知,能计算其摩尔质量,故C不选。
D、单位物质的量的物质所具有的质量叫做摩尔质量,已知物质一个分子的实际质量,在数值上1mol该分子的质量等于其相对分子质量,故D不选。
故选B
9.实验中的下列操作正确的是( )
A.用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中
B.粗盐提纯时,为了加快过滤速率,可以用玻璃棒进行搅拌
C.用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干
D.用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中
10.已知乙醛是无色易流动液体,有刺激性气味。
熔点-121℃,沸点20.8℃,相对密度小于1,可与水和乙醇等一些有机物质互溶。
要从水与乙醛的混合物中将乙醛分离出来,应选用()
A.蒸馏B.分液C.过滤D.蒸发
【解析】水和乙醛相互混溶,但沸点存在差异,可利用蒸馏操作进行分离,故答案为A。
11.下列关于物质的量浓度表述正确的是( )
A.0.2mol·
L-1的硫酸铝溶液中含有Al3+和SO42-的总物质的量为1mol
B.在K2SO4和NaCl的中性混合水溶液中,如果Na+和SO42-的物质的量相等,则K+和Cl-的物质的量浓度一定相同
C.当22.4L氨气溶于水制得1L氨水时,其浓度为1mol·
D.20℃时,0.023mol·
L-1的氢氧化钙饱和溶液100mL加入5g生石灰,冷却到20℃时,其体积小于100mL,它的物质的量浓度仍为0.023mol·
【解析】A.没有提供溶液的体积,无法计算Al3+和SO42-的总物质的量,故A错误;
B.如果Na+和SO42-的物质的量相等,硫酸根离子所带电荷大于钠离子所带电荷,根据溶液中阴阳离子所带电荷相等,所以K+的物质的量浓度大于Cl-的物质的量浓度,故B错误;
C.气体摩尔体积22.4L/mol只有在标况下才能使用,则22.4L氨气的物质的量不一定为1mol,制得1L氨水时,其浓度不一定是1mol/L,故C错误;
D.氢氧化钙饱和溶液100mL加入5g生石灰,生石灰要和水反应生成氢氧化钙,相当原饱和溶液恒温蒸发水分,有晶体析出,同时溶液的体积减小,则温度相同时,同一物质的饱和溶液中溶液的物质的量浓度一定相同,与溶液的体积无关,故D正确;
答案为D。
12.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.在25℃、1.01×
105Pa的条件下,2.24LH2中含有的分子数小于0.1NA
B.1L1mol·
L-1的CaCl2溶液中含Cl-的数目为NA
C.在标准状况下,22.4LSO3的质量约为80g
D.22gCO2与标准状况下11.2LH2O含有相同的分子数
【解析】A.在标准状况下,气体摩尔体积约为22.4L/mol,所以在25℃、1.01×
105Pa的条件下,2.24LH2的物质的量小于0.1mol,含有的分子数小于0.1NA,A正确;
L-1的CaCl2溶液中含Cl-的物质的量为2mol,所以其数目为2NA,B不正确;
C.在标准状况下,SO3不是气体,所以无法计算22.4LSO3的物质的量和质量,C不正确;
D.22gCO2的物质的量为0.5mol,标准状况下11.2LH2O不是气体,其物质的量大于0.5mol,所以它们的分子数不相同,D不正确。
本题选A。
13.用0.2mol·
L-1某金属阳离子Rn+的盐溶液40mL,恰好将20mL0.4mol·
L-1的硫酸盐中的硫酸根离子完全沉淀,则n值为( )
A.1B.2C.3D.4
【解析】溶液中SO42-离子的物质的量为:
20mL×
10-3×
0.4mol•L-1=8×
10-3mol,溶液中Rn+离子的物质的量为:
40mL×
0.2mol•L-1=8×
10-3mol,由反应中恰好将溶液中的Mn+离子完全沉淀为硫酸盐时M的化合价为+n,则SO42-与Rn+反应对应的关系式为:
2Rn+~nSO42-
2
n
8×
10-3mol
8×
10-3mol
解得n=2,故选答案B。
14.在标准状况下,质量为m的气体A与质量为n的气体B的分子数相同,下列说法中不正确的是( )
A.气体A与气体B的相对分子质量比为m∶n
B.同质量气体A与气体B的分子个数比为n∶m
C.同温同压下,A气体与B气体的密度比为n∶m
D.相同状况下,同体积的A气体与B气体的质量比为m∶n
标准状况下,分子数相同的气体A和B,它们的物质的量相同,气体体积相同.A.由m=nM可以知道,分子数相同的气体,相对分子质量之比等于质量之比,即A与B相对分子质量之比为mg:
ng=m:
n,所以A选项是正确的;
B.A与B相对分子质量之比为=m:
n,同质量时由n=m/M可以知道,分子数之比等于1/m:
1/n=n:
m,故B错误;
C.同温同压,气体密度之比等于摩尔质量之比等于相对分子质量之比,即A、B两气体的密度之比为m:
n,故C错误;
D.相同状况下,同体积的A与B的物质的量相同,则质量之比等于相对分子质量之比,即A、B两气体的质量之比为m:
n,所以D选项是正确的.所以C选项是正确的.
15.标准状况下,700L氨气溶于1L水得到密度为0.9g·
cm-3的饱和氨水,则该氨水的物质的量浓度约为( )
A.16.4mol·
L-1B.17.4mol·
L-1C.18.4mol·
L-1D.19.4mol·
令氨气为700L,则水为1L,氨气的物质的量=
=
mol,
氨气的质量=
mol×
17g/mol=
g,水的质量=1L×
1000g/L=1000g,
溶液的体积=
L,
所得氨水的物质的量浓度=
mol÷
L==18.37mol/L,故选C。
16.现有下列仪器:
(1)海水蒸馏是由海水获得淡水的常用方法之一,在实验室里组成一套蒸馏装置肯定需要上述仪器中的一部分,按照实验仪器从下到上、从左到右的顺序,依次是________(填序号);
仪器⑤的冷凝水应从________(填“a”或“b”)口进入。
(2)海带等藻类物质经过处理后,可以得到碘水,欲从碘水中提取碘,需要上述仪器中的________(填序号),该仪器名称为________,向该碘水中加入四氯化碳以提取碘单质的实验操作叫做________。
【答案】
(1).②③⑥⑤
(2).a(3).①(4).分液漏斗(5).萃取
【解析】
(1)蒸馏装置需要的仪器有:
蒸馏烧瓶、单孔塞、酒精灯、冷凝管、牛角管、锥形瓶,故答案为:
②③⑥⑤;
冷凝管的水流方向应为逆流效果好,所以应从a进b出;
(2)从碘水中提取碘,可以采取萃取分液操作,使用的萃取剂是四氯化碳,使用的仪器是分液漏斗。
17.实验室用63%的浓HNO3(其密度为1.4g·
mL-1)配制240mL0.50mol·
L-1稀HNO3,若实验仪器有:
A.10mL量筒 B.50mL量筒 C.托盘天平D.玻璃棒 E.100mL容量瓶 F.250mL容量瓶G.500mL容量瓶 H.胶头滴管 I.200mL烧杯
(1)此浓硝酸的物质的量浓度为________mol·
L-1。
(2)应量取63%的浓硝酸______mL,应选用________(填仪器的字母编号)。
(3)实验时还需选用的仪器有D、I、______(填序号)。
(4)配制过程中,下列操作会使配制的稀硝酸溶液浓度偏高的是(填序号)________。
①量取浓硝酸的量筒用蒸馏水洗涤2~3次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③溶解后未经冷却就移液
④定容时不小心有少量蒸馏水滴到瓶外
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
(1).14.0
(2).8.9(3).A(4).F、H(5).①③
(1)浓硫酸物质的量浓度c=
=14.0mol/L;
(2)由于无240mL容量瓶,故应选用250mL容量瓶,配制出250mL溶液,设需要的浓硝酸的体积为VmL,根据溶液稀释定律C浓V浓=C稀V稀:
14.0mol/L×
VmL=250mL×
0.50mol/L,解得V=8.9mL;
根据“大而近”的原则,根据需要量取的浓硝酸的体积为8.9mL,故应选择10mL量筒,答案为A;
(3)根据配制步骤是计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶可知所需的仪器有10mL量筒、烧杯、玻璃棒、250mL容量瓶和胶头滴管,故还需要的仪器有250mL容量瓶和胶头滴管,故答案为F、H;
(4)①量取浓硝酸的量筒用蒸馏水洗涤2-3次,并把洗涤液转入容量瓶,会导致溶质的量偏多,则浓度偏高,故①正确;
②容量瓶使用时未干燥,对浓度无影响,故②错误;
③溶解后未经冷却就移液,则冷却后溶液体积偏小,浓度偏高,故③正确;
④定容时不小心有少量蒸馏水滴到瓶外,会导致溶质的损失,则浓度偏低,故④错误;
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线是正常的,再加蒸馏水补至刻度线会导致浓度偏低,故⑤错误;
故答案为①③。
18.如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
(1)从氯化钾溶液中得到氯化钾固体,选择装置________(填代表装置图的字母,下同);
除去自来水中的Cl-等杂质,选择装置________。
(2)从油水混合物中分离出植物油,选择装置________,该分离方法的名称为________。
(3)装置A中①的名称是________,进水的方向是从________口进水。
装置B在分液时为使液体顺利滴下,除打开活塞外,还应进行的具体操作是______________________。
(4)海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:
―→
粗盐中含Ca2+、Mg2+、Fe3+、SO
等杂质,需要提纯后才能综合利用。
粗盐提纯的步骤有:
①加入过量的Na2CO3溶液 ②加入过量的BaCl2溶液 ③加入过量的NaOH溶液 ④调节溶液的pH等于7 ⑤溶解 ⑥过滤 ⑦蒸发
正确的操作顺序是________(填选项字母)。
a.⑤②③①⑥④⑦b.⑤①②③⑥④⑦
c.⑤②①③④⑥⑦d.⑤③②①⑥④⑦
(1).D
(2).A(3).B(4).分液(5).冷凝管(6).下(7).将分液漏斗上部的玻璃塞打开(8).ad
A为蒸馏装置,B为萃取和分液装置,C为过滤装置,D为蒸发结晶装置。
(1)从氯化钾溶液中得到氯化钾固体应蒸发结晶,选择装置D;
除去自来水中的Cl-等杂质应蒸馏,选择装置A。
(2)从油水混合物中分离出植物油,因为油和水不相溶,所以选择装置B,该分离方法的名称为分液。
(3)装置A中①的名称是冷凝管,进水的方向是从下口进水。
装置B在分液时为使液体顺利滴下,除打开活塞外,还应进行的具体操作是将分液漏斗上部的玻璃塞打开。
(4)除去粗盐中含Ca2+、Mg2+、Fe3+、SO
等杂质,方法是先溶解,然后依次加入沉淀剂把这些杂质离子沉淀,过滤,最后向滤液加盐酸除去过量的Na2CO3溶液和NaOH溶液。
通常用Na2CO3溶液沉淀Ca2+,用NaOH溶液沉淀Mg2+和Fe3+,用BaCl2溶液沉淀SO
,其关键是把Na2CO3溶液放在BaCl2溶液之后使用,这样可以除去过量的BaCl2,所以提纯的步骤正确的有ad。
19.填写下列空白:
(1)含有6.02×
1023个H的H2O,其物质的量是________;
1L1mol/LNa2SO4溶液中含有______个Na+、______个SO
。
(2)______molH2O中含有的氧原子数与1.5molCO2中含有的氧原子数相等。
(3)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为________。
(4)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为__________。
(5)标准状况下,密度为0.75g·
L-1的NH3与CH4组成的混合气体中,NH3的体积分数为__________,该混合气体对氢气的相对密度为________。
(6)已知agA和bgB恰好完全反应生成0.2molC和dgD,则C的摩尔质量为__________。
(1).0.5mol
(2).1.204×
1024(2NA)(3).6.02×
1023(NA)(4).3(5).17∶16(6).4∶3(7).80%(8).8.4(9).5(a+b-d)g·
(1)6.02×
1023个H的物质的量是1mol,所以含有6.02×
1023个H的H2O的物质的量是0.5mol;
1L1mol/LNa2SO4溶液中含有Na2SO4的物质的量为1mol,所以含有2molNa+,、1molSO
,所含离子数目为1.204×
1024(或2NA)个Na+、6.02×
1023(或NA)个SO
(2)每个CO2分子中有2个O、每个H2O分子中有1个O。
1.5molCO2中含有的氧原子的物质的量为3mol,所以3molH2O中含有的氧原子数与1.5molCO2中含有的氧原子数相等。
(3)NH3和CH4的摩尔质量分别为17g/mol和16g/mol,将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为17∶16。
(4)NH3与CH4分子中H原子数之比为3:
4,要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为4∶3。
L-1的NH3与CH4组成的混合气体,其平均摩尔质量为0.75g·
22.4L/mol=16.8g/mol,则17
,解得
,所以NH3的体积分数为80%,不同气体的密度之比等于其摩尔质量之比,所以该混合气体对氢气的相对密度为
8.4。
(6)已知agA和bgB恰好完全反应生成0.2molC和dgD,由质量守恒定律求得m(C)=(a+b-d)g,则C的摩尔质量为
5(a+b-d)g·
mol-1。